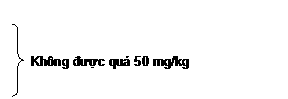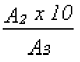Nội dung toàn văn Quy chuẩn kỹ thuật Quốc gia QCVN 4-10:2010/BYT về phụ gia thực phẩm – phẩm màu do Bộ trưởng Bộ Y tế ban hành
QUY CHUẨN KỸ THUẬT QUỐC GIA
QCVN 4-10:2010/BYT
VỀ PHỤ GIA THỰC PHẨM – PHẨM MÀU
National technical regulation
on Food Additives – Colours
HÀ NỘI – 2010
Lời nói đầu
QCVN 4-10 :2010/BYT do Ban soạn thảo quy chuẩn kỹ thuật quốc gia về Phụ gia thực phẩm và chất hỗ trợ chế biến biên soạn, Cục An toàn vệ sinh thực phẩm trình duyệt và được ban hành theo Thông tư số 27/2010/TT-BYT ngày 20 tháng 5 năm 2010 của Bộ trưởng Bộ Y tế.
QUY CHUẨN KỸ THUẬT QUỐC GIA
VỀ PHỤ GIA THỰC PHẨM – PHẨM MÀU
National technical regulation on Food Additives – Colours
I. QUY ĐỊNH CHUNG
1. Phạm vi điều chỉnh
Quy chuẩn kỹ thuật quốc gia (sau đây gọi tắt là Quy chuẩn) này quy định các yêu cầu kỹ thuật và quản lý về chất lượng, vệ sinh an toàn đối với các phẩm màu được sử dụng với mục đích làm phụ gia thực phẩm.
2. Đối tượng áp dụng
Quy chuẩn này áp dụng đối với:
2.1. Tổ chức, cá nhân nhập khẩu, xuất khẩu, sản xuất, buôn bán và sử dụng các phẩm màu làm phụ gia thực phẩm (sau đây gọi tắt là tổ chức, cá nhân).
2.2. Cơ quan quản lý nhà nước có liên quan.
3. Giải thích từ ngữ và chữ viết tắt:
3.1. Phẩm màu: là phụ gia thực phẩm được sử dụng với mục đích tăng cường hoặc khôi phục màu cho sản phẩm thực phẩm.
3.2. JECFA monograph 1 – Vol. 4 (JECFA monographs 1 – Combined compendium of food addiditive specifications; Joint FAO/WHO expert committee on food additives; Volume 4 – Analytical methods, test procedures and laboratory solutions used by and referenced in the food additive specifications; FAO, 2006): Các yêu cầu kỹ thuật đối với phụ gia thực phẩm, Tập 4 Các phương pháp phân tích, quy trình thử nghiệm, dung dịch thử nghiệm được sử dụng (hoặc tham chiếu) trong yêu cầu kỹ thuật đối với phụ gia thực phẩm; JECFA biên soạn; FAO ban hành năm 2006.
3.3. Mã số C.A.S (Chemical Abstracts Service): Mã số đăng ký hóa chất của Hiệp hội Hóa chất Hoa Kỳ.
3.4. TS (test solution): Dung dịch thuốc thử.
3.5. ADI (Acceptable daily intake): Lượng ăn vào hàng ngày chấp nhận được.
3.6. INS (International numbering system): Hệ thống mã số quốc tế về phụ gia thực phẩm.
II. YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ VÀ LẤY MẪU
1. Yêu cầu kỹ thuật và phương pháp thử đối với phẩm màu được quy định tại các phụ lục ban hành kèm theo Quy chuẩn này như sau :
1.1. Phụ lục 1: Quy định kỹ thuật và phương pháp thử đối với curcumin
1.2. Phụ lục 2: Quy định kỹ thuật và phương pháp thử đối với riboflavin
1.3. Phụ lục 3: Quy định kỹ thuật và phương pháp thử đối với tatrazin
1.4. Phụ lục 4: Quy định kỹ thuật và phương pháp thử đối với quinolin
1.5. Phụ lục 5: Quy định kỹ thuật và phương pháp thử đối với sunset yellow FCF
1.6. Phụ lục 6: Quy định kỹ thuật và phương pháp thử đối với carmin
1.7. Phụ lục 7: Quy định kỹ thuật và phương pháp thử đối với carmoisin
1.8. Phụ lục 8: Quy định kỹ thuật và phương pháp thử đối với amaranth
1.9. Phụ lục 9: Quy định kỹ thuật và phương pháp thử đối với ponceau 4R
1.10. Phụ lục 10: Quy định kỹ thuật và phương pháp thử đối với erythrosin
1.11. Phụ lục 11: Quy định kỹ thuật và phương pháp thử đối với red 2G
1.12. Phụ lục 12: Quy định kỹ thuật và phương pháp thử đối với allura red AC
1.13. Phụ lục 13: Quy định kỹ thuật và phương pháp thử đối với indigotin
1.14. Phụ lục 14: Quy định kỹ thuật và phương pháp thử đối với brilliant blue FCF
1.15. Phụ lục 15: Quy định kỹ thuật và phương pháp thử đối với clorophyl
1.16. Phụ lục 16: Quy định kỹ thuật và phương pháp thử đối với clorophyl phức đồng
1.17. Phụ lục 17: Quy định kỹ thuật và phương pháp thử đối với muối Natri, Kali của Clorophyl phức đồng
1.18. Phụ lục 18: Quy định kỹ thuật và phương pháp thử đối với green S
1.19. Phụ lục 19: Quy định kỹ thuật và phương pháp thử đối với caramen
1.20. Phụ lục 20: Quy định kỹ thuật và phương pháp thử đối với brilliant black PN
1.21. Phụ lục 21: Quy định kỹ thuật và phương pháp thử đối với brown HT
1.22. Phụ lục 22: Quy định kỹ thuật và phương pháp thử đối với β-caroten tổng hợp
1.23. Phụ lục 23: Quy định kỹ thuật và phương pháp thử đối với caroten thực vật
1.24. Phụ lục 24: Quy định kỹ thuật và phương pháp thử đối với cao annatto
1.25. Phụ lục 25: Quy định kỹ thuật và phương pháp thử đối với β-Apo-carotenal
1.26. Phụ lục 26: Quy định kỹ thuật và phương pháp thử đối với este methyl (hoặc Ethyl) của acid β-Apo-8′-Carotenoic
1.27. Phụ lục 27: Quy định kỹ thuật và phương pháp thử đối với cao vỏ nho
1.28. Phụ lục 28: Quy định kỹ thuật và phương pháp thử đối với dioxyd titan
1.29. Phụ lục 29: Quy định kỹ thuật và phương pháp thử đối với oxyd sắt
1.30. Phụ lục 30: Quy định kỹ thuật và phương pháp thử đối với fast green FCF
2. Các yêu cầu kỹ thuật quy định trong Quy chuẩn này được thử theo JECFA monograph 1 – Vol. 4, ngoại trừ một số phép thử riêng được mô tả trong các phụ lục. Các phương pháp thử được hướng dẫn trong Quy chuẩn này không bắt buộc phải áp dụng, có thể sử dụng các phương pháp thử khác tương đương.
3. Lấy mẫu theo hướng dẫn tại Thông tư 16/2009/TT-BKHCN ngày 02 tháng 6 năm 2009 của Bộ Khoa học và Công nghệ về hướng dẫn kiểm tra nhà nước về chất lượng hàng hóa lưu thông trên thị trường và các quy định khác của pháp luật có liên quan.
III. YÊU CẦU QUẢN LÝ
1. Công bố hợp quy
1.1. Các phẩm màu phải được công bố phù hợp với các quy định tại Quy chuẩn này.
1.2. Phương thức, trình tự, thủ tục công bố hợp quy được thực hiện theo Quy định về chứng nhận hợp chuẩn, chứng nhận hợp quy và công bố hợp chuẩn, công bố hợp quy ban hành kèm theo Quyết định số 24/2007/QĐ-BKHCN ngày 28 tháng 9 năm 2007 của Bộ trưởng Bộ Khoa học và Công nghệ và các quy định của pháp luật.
2. Kiểm tra đối với phẩm màu
Việc kiểm tra chất lượng, vệ sinh an toàn đối với các phẩm màu phải thực hiện theo các quy định của pháp luật.
IV. TRÁCH NHIỆM CỦA TỔ CHỨC, CÁ NHÂN
1. Tổ chức, cá nhân phải công bố hợp quy phù hợp với các quy định kỹ thuật tại Quy chuẩn này, đăng ký bản công bố hợp quy tại Cục An toàn vệ sinh thực phẩm và bảo đảm chất lượng, vệ sinh an toàn theo đúng nội dung đã công bố.
2. Tổ chức, cá nhân chỉ được nhập khẩu, xuất khẩu, sản xuất, buôn bán và sử dụng các phẩm màu sau khi hoàn tất đăng ký bản công bố hợp quy và bảo đảm chất lượng, vệ sinh an toàn, ghi nhãn phù hợp với các quy định của pháp luật.
V. TỔ CHỨC THỰC HIỆN
1. Giao Cục An toàn vệ sinh thực phẩm chủ trì, phối hợp với các cơ quan chức năng có liên quan hướng dẫn triển khai và tổ chức việc thực hiện Quy chuẩn này.
2. Căn cứ vào yêu cầu quản lý, Cục An toàn vệ sinh thực phẩm có trách nhiệm kiến nghị Bộ Y tế sửa đổi, bổ sung Quy chuẩn này.
3. Trường hợp hướng dẫn của quốc tế về phương pháp thử và các quy định của pháp luật viện dẫn trong Quy chuẩn này được sửa đổi, bổ sung hoặc thay thế thì áp dụng theo văn bản mới.
PHỤ LỤC 1
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CURCUMIN
|
1. Tên khác, chỉ số |
Vàng nghệ, Kurkum INS: 100i ADI = 0 – 3 mg/kg thể trọng. |
|||||||||
|
2. Định nghĩa |
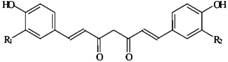
Curcumin được sản xuất bằng cách chiết củ nghệ – thân rễ của cây Curcuma longa L. (Curcuma domestica Valeton) bằng dung môi. Để thu được bột curcumin có hàm lượng cao, dịch chiết được tinh chế bằng phương pháp kết tinh. Sản phẩm thu được chứa các curcumin, thành phần màu chính là 1,7-bis-(4-hydroxy-3-methoxy-phenyl)-hepta-1,6-dien-3,5-dion (tên khác: Curcumin, Diferuloylmethan, CI Natural Yellow 3, CI (1975) 75300) và dẫn chất desmethoxy- và bis-desmethoxy- của nó theo tỷ lệ không cố định. Trong chế phẩm có thể chứa lượng nhỏ dầu và nhựa từ nguyên liệu. Chỉ các dung môi sau đây có thể được sử dụng trong quá trình chiết và tinh chế curcumin: Aceton, methanol, ethanol, iso-propanol, hexan và ethyl acetat. Carbon dioxyd siêu tới hạn cũng có thể được sử dụng trong quá trình chiết. |
|||||||||
|
Tên hóa học |
Các thành phần màu chính:
|
|||||||||
|
Mã số C.A.S. |
|
|||||||||
|
Công thức hóa học |
|
|||||||||
|
Công thức cấu tạo |
|
|||||||||
|
Khối lượng phân tử |
|
|||||||||
|
3. Cảm quan |
Bột tinh thể màu vàng cam. |
|||||||||
|
4. Chức năng |
Phẩm màu. |
|||||||||
|
5. Yêu cầu kỹ thuật |
||||||||||
|
5.1. Định tính |
|
|||||||||
|
Độ tan |
Không tan trong nước và diethyl ether; tan trong ethanol và acid acetic băng. |
|||||||||
|
Các phản ứng màu |
Dung dịch mẫu thử trong ethanol có màu vàng và cho huỳnh quang xanh nhạt. Thêm dung dịch mẫu thử này vào acid sulfuric đặc sẽ có màu đỏ thẫm. |
|||||||||
|
Sắc ký bản mỏng |
Đạt yêu cầu (mô tả trong phần Phương pháp thử). |
|||||||||
|
5.2. Độ tinh khiết |
|
|||||||||
|
Tồn dư dung môi |
|
|||||||||
|
Chì |
Không được quá 2 mg/kg |
|||||||||
|
5.3. Hàm lượng |
Không nhỏ hơn 90% tổng các thành phần màu. |
|||||||||
|
6. Phương pháp thử |
||||||||||
|
6.1. Định tính |
|
|||||||||
|
Các phản ứng màu |
Xử lý dung dịch mẫu thử trong nước hoặc trong ethanol loãng với acid hydrocloric đến khi màu cam bắt đầu xuất hiện. Chia dung dịch sau khi xử lý thành 2 phần, thêm bột (hoặc tinh thể) acid boric vào 1 phần. Màu đỏ hồng sẽ xuất hiện nhanh sau khi thêm, màu sẽ dễ nhận biết hơn khi so với phần không thêm acid boric. Phản ứng có thể tiến hành bằng cách nhúng một mẩu giấy lọc vào dịch mẫu thử tan trong ethanol, làm khô tại 100o, sau đó tẩm ướt mẩu giấy lọc bằng dung dịch acid boric loãng đã thêm vài giọt acid hydrocloric. Để khô, sẽ xuất hiện màu đỏ hồng. |
|||||||||
|
Sắc ký bản mỏng |
Chấm 5 mL dịch thử (0,01 g mẫu thử trong 1 ml ethanol 95%) trên 1 bản mỏng sắc ký (cellulose vi tinh thể; 0,1 mm). Khai triển sắc ký trong bình chứa hỗn hợp dung môi pha động 3-methyl-1-butanol/ethanol/nước/dung dịch amoniac (4:4:2:1), để dung môi khai triển trên bản mỏng 10-15 cm từ vạch xuất phát. Kiểm tra, quan sát dưới ánh sáng thường và đèn UV: Dưới ánh sáng thường và UV có 2 hoặc 3 vết màu vàng với Rf trong khoảng 0,2 – 0,4. Dưới đèn UV có các vết với Rf khoảng 0,6 và 0,8 Các vết đều có huỳnh quang màu vàng dưới đèn UV. |
|||||||||
|
6.2 Độ tinh khiết |
|
|||||||||
|
Chì |
Xác định bằng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|||||||||
|
6.3. Định lượng |
|
|||||||||
|
|
Cân 0,08 g mẫu thử (chính xác đến mg), chuyển vào bình định mức 200 ml và hoà tan bằng lắc với ethanol, định mức đến vạch bằng ethanol. Dùng pipet hút 1 ml dung dịch và cho vào bình định mức 100 ml, định mức đến vạch bằng ethanol. Xác định độ hấp thụ quang tại 425 nm, cuvet đo dày 1 cm. Tính tỷ lệ tổng hàm lượng chất màu trong mẫu thử theo công thức:
Trong đó: A = độ hấp thụ của dung dịch mẫu thử W = Khối lượng mẫu thử 1607 = Độ hấp thụ riêng của dung dịch curcumin chuẩn trong ethanol tại 425 nm. Việc xác định độ hấp thụ quang phải tiến hành ngay khi pha xong dung dịch, bởi vì màu của dung dịch có thể nhạt dần theo thời gian. |
|||||||||
PHỤ LỤC 2
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI RIBOFLAVIN
|
1. Tên khác, chỉ số |
Vitamin B2, Lactoflavin INS: 101i ADI = 0 – 0,5 mg/kg thể trọng. |
|
2. Định nghĩa |
|
|
Tên hóa học |
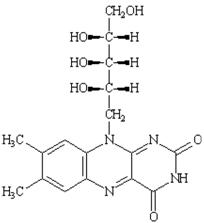
Riboflavin; 3,10-dihydro-7,8-dimethyl-10-[(2S,3S,4R)-2,3,4,5-tetrahydroxypentyl]benzo-[g]pteridin-2,4-dion; 7,8-dimethyl-10-(1′-Dribityl) isoalloxazin. |
|
Mã số C.A.S. |
83-88-5 |
|
Công thức hóa học |
C17H20N4O6 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
376,37 |
|
3. Cảm quan |
Bột tinh thể màu vàng đến vàng cam, có mùi nhẹ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Rất khó tan trong nước, thực tế không tan trong cồn, ether, aceton và cloroform; rất dễ tan trong dung dịch kiềm loãng. |
|
Quang phổ |
Sử dụng dung dịch mẫu thử trong nước, đã chuẩn bị trong phần Định lượng, xác định độ hấp thụ quang (A) tại các bước sóng 267 nm, 375 nm, 444 nm. Tỷ số A375/A267 nằm trong khoảng 0,31 và 0,33. Tỷ số A444/A267 nằm trong khoảng 0,36 và 0,39. |
|
Góc quay cực riêng |
[a]20,D: trong khoảng -115o và -140o. |
|
Phản ứng màu |
Đạt yêu cầu (mô tả trong phần Phương pháp thử). |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô |
Không được quá 1,5%. |
|
Tro sulfat |
Không được quá 0,1%. |
|
Các chất màu phụ |
Đạt yêu cầu (mô tả trong phần Phương pháp thử). |
|
Các amin thơm bậc nhất |
Không được quá 100 mg/kg tính theo anilin. |
|
Chì |
Không được quá 2 mg/kg. |
|
5.3. Hàm lượng C17H20N4O6 |
Không được thấp hơn 98%. |
|
6. Phương pháp thử |
|
|
6.1 Định tính |
|
|
Góc quay cực riêng |
Sấy khô mẫu tại 100 oC trong 4 gờ. Cân 50 mg và hòa tan trong dung dịch natri hydroxyd 0,05 N không có carbonat và pha loãng đến đủ 10 ml cũng bằng dung dịch này. Đo độ quay quang của dung dịch trong 30 phút kể từ khi pha dung dịch. |
|
Phản ứng màu |
Hòa tan khoảng 1 mg mẫu vào 100 ml nước. Dung dịch có màu vàng xanh nhạt khi cho ánh sáng truyền qua và có huỳnh quang xanh vàng đậm với ánh sáng phản xạ. Màu sẽ bị mất khi thêm acid vô cơ hoặc kiềm vô cơ. |
|
6.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô |
Sấy tại 105 oC, trong 4 giờ |
|
Tro sulfat |
– Thử theo JECFA monograph 1 – vol.4 – Mẫu thử: cân 2 g |
|
Các chất màu phụ |
Chuẩn bị dung dịch chuẩn không có lumiflavin cho thử nghiệm bằng cách pha loãng 3 ml dung dịch kali dicromat 0,1 N với nước đến đủ 1000 ml. Cho một ít cloroform qua cột nhôm oxyd để loại hết ethanol. Lấy 10 ml cloroform này, thêm 35 mg mẫu, lắc trong 5 phút và lọc. Mật độ màu của dịch lọc không được đậm hơn mật độ màu của 10 ml chuẩn khi quan sát trong dụng cụ chứa cùng loại |
|
Chì |
Thử theo hướng dẫn tại JECFA monograph 1 – vol.4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong Phụ lục 1: Các phương pháp thử chung phần các phương pháp phân tích công cụ |
|
6.3. Định lượng |
|
|
|
Tiến hành định lượng trong môi trường ít ánh sáng. Phân tán 65,0 mg mẫu thử trong 5 ml nước trong bình định mức 500 ml màu nâu, cần đảm bảo rằng toàn bộ mẫu thử đã bị tẩm ướt, hòa tan trong 5 ml dung dịch natri hydroxyd 2 N. Ngay khi mẫu tan hoàn toàn, thêm 100 ml nước và 2,5 ml acid acetic băng và pha loãng bằng nước đến đủ 500 ml. Lấy 20,0 ml dung dịch này, thêm 3,5 ml dung dịch natri acetat 1,4% (kl/tt) và pha loãng với nước đến đủ 200 ml. Đo độ hấp thụ quang (A) tại cực đại hấp thụ 444 nm. % Riboflavin = [(A×5000) / (328×W)] × 1,367 trong đó A = độ hấp thụ của dung dịch mẫu thử tại 444 nm W = Khối lượng mẫu thử, tính bằng g. |
PHỤ LỤC 3
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI TARTRAZIN
|
1. Tên khác, chỉ số |
CI Food Yellow 4, FD&C Yellow No. 5; Số CI (1975): 19140 INS: 102 ADI = 0 – 7,5 mg/kg thể trọng. |
|
2. Định nghĩa |
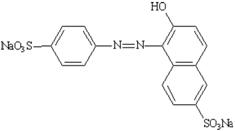
Chủ yếu gồm Trinatri 5-hydroxy-1-(4-sulfonphenyl)-4-(4-sulfonphenylazo)-H-pyrazol-3-carboxylat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
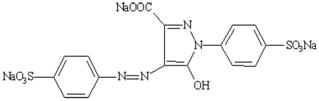
Trinatri 5-hydroxy-1-(4-sulfonphenyl)-4-(4-sulfonphenylazo)-H-pyrazol-3-carboxylat |
|
Mã số C.A.S. |
1934-21-0 |
|
Công thức hóa học |
C16H9N4Na3O9S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
534,37 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu cam nhạt. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của các chất màu |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 1%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% (tổng các acid Tetrahydroxysuccinic; acid 4-Hydrazinbenzensulfonic; acid 4-Aminobenzensulfonic; acid 5-Oxo-1-(4-sulfophenyl)-2-pyrazolin-3-carboxylic; acid 4,4′-Diazoaminodi (acid benzensulfonic). |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4, Các phương pháp thử chung phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; chiều cao của tuyến dung môi ~ 12 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient 2 đến 100% với tốc độ tăng cố định 2%/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong Phụ lục 1: Các phương pháp thử chung) như sau: Cân 0,6 – 0,7 g mẫu thử; Đệm 15 g natri hydro tartrat; Mỗi ml TiCl3 0,1 N tương đương với 13,56 mg các chất màu (D). |
PHỤ LỤC 4
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI QUINOLIN
1. Tên khác, chỉ số |
CI food yellow 13, CI (1975) No. 47005, INS: 104 ADI = 0 – 10 mg/kg thể trọng. |
|||||||||||||||||||||
2. Định nghĩa |
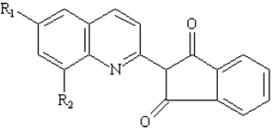
Chế phẩm thu được bằng cách sulfonat hoá 2-(2-quinolyl)-1,3-indandion hoặc hỗn hợp chứa khoảng hai phần ba 2-(2-quinolyl)-1,3-indandion và một phần ba 2-[2-(6-methyl-quinolyl)]1,3-indandion; Chế phẩm chứa hỗn hợp muối natri của các disulfonat (chủ yếu), các monosulfonat and các trisulfonat của các hợp chất nêu trên và các chất màu phụ cùng với natri clorid và/hoặc natri sulfat là các thành phần chính không tạo mầu. Quinolin có thể chuyển thành dạng màu nhôm tương ứng, trong trường hợp này áp dụng quy chuẩn chung cho dạng màu nhôm của các phẩm màu. |
|||||||||||||||||||||
Tên hóa học |
Dinatri 2-(1,3-dioxo-2-indanyl)-6,8-quinolin sulfat; dinatri 2-(2-quinolyl)-indan-1,3-dion disulfonat (thành phần chính) |
|||||||||||||||||||||
Mã số C.A.S. |
8004-72-0 (acid disulfonic không methyl hóa) |
|||||||||||||||||||||
Công thức hóa học |
C18H9NNa2O8S2 (thành phần màu chính) |
|||||||||||||||||||||
Công thức cấu tạo |
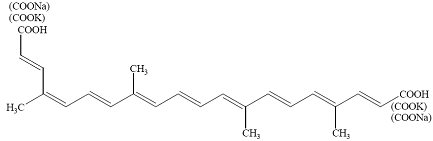
Thành phần màu chính
6 muối: R1 = SO3Na, R2 = H 8 muối: R1, R2 = SO3H |
|||||||||||||||||||||
Khối lượng phân tử |
Thành phần màu chính: 477,38 |
|||||||||||||||||||||
3. Cảm quan |
Bột hoặc hạt nhỏ màu vàng. |
|||||||||||||||||||||
4. Chức năng |
Phẩm màu. |
|||||||||||||||||||||
5. Yêu cầu kỹ thuật |
||||||||||||||||||||||
5.1. Định tính |
|
|||||||||||||||||||||
Độ tan |
Tan trong nước, ít tan trong ethanol |
|||||||||||||||||||||
Định tính các chất màu |
Phải có phản ứng đặc trưng của các chất màu. |
|||||||||||||||||||||
5.2. Độ tinh khiết |
|
|||||||||||||||||||||
Giảm khối lượng khi sấy tại 135o |
Không được quá 30% cùng với clorid và sulfat tính theo muối natri. |
|||||||||||||||||||||
Chất không tan trong nước |
Không được quá 0,2%. |
|||||||||||||||||||||
Chì |
Không được quá 2 mg/kg. |
|||||||||||||||||||||
Kẽm |
Không được quá 50 mg/kg. |
|||||||||||||||||||||
Các chất màu phụ |
Tổng hàm lượng 2 chất 2-(2-quinolyl)-1,3-indandion và 2-[2-(6-methylquinolyl)]-1,3-indandion Không được quá 4 mg/kg |
|||||||||||||||||||||
Các hợp chất hữu cơ ngoài các thành phần màu |
Tổng hàm lượng các chất 2-methylquinolin, acid 2-methylquinolinsulfonic, acid phtalic, 2,6-dimethylquinolin, acid 2,6-dimethylquinolin sulfonic Không được quá 0,5% |
|||||||||||||||||||||
Các amin thơn bậc nhất không sulfonat hóa |
Không được quá 0,01% tính theo anilin. |
|||||||||||||||||||||
Chất có thể chiết bằng ether |
Không được quá 0,2%. |
|||||||||||||||||||||
5.3. Hàm lượng |
Không nhỏ hơn 70% tổng các thành phần màu. Đối với chế phẩm quinolin vàng sản xuất từ 2-(2-quinolyl)-1,3-indandion sẽ có các thành phần sau: – Không nhỏ hơn 80% dinatri 2-(2-quinolyl)-indan- 1,3-diondisulfonat; – Không được quá 15% natri 2-(2-quinolyl)-indan-1,3-dionmonosulfonat; – Không được quá 7% trinatri 2-(2-quinolyl)-indan-1,3- diontrisulfonat; |
|||||||||||||||||||||
6. Phương pháp thử |
||||||||||||||||||||||
6.1. Độ tinh khiết |
|
|||||||||||||||||||||
Chì |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4, Các phương pháp thử chung phần các phương pháp phân tích công cụ. |
|||||||||||||||||||||
Các chất màu phụ |
Thử giới hạn của 2-(2-quinolyl)-1,3-indandion và 2-[2-(6-methylquinolyl)]-1,3-indandion. Sử dụng thiết bị và ether có chất lượng theo mô tả trong chuyên luận xác định chất có thể chiết bằng ether và tiến hành chiết như sau: Rửa dịch chiết 2 lần mỗi lần với 25 ml nước cất. Cho ether bay hơi để dịch chiết còn khoảng 5 ml, sau đó cho vào tủ sấy tại nhiệt độ 105o để đuổi hết ether. Hoà tan cặn còn lại trong cloroform và pha loãng đến chính xác 10 ml. Xác dịnh độ hấp thụ quang của dung dịch này tại bước sóng hấp thụ cực đại (khoảng 420 nm) sử dụng cloroform làm dung dịch đối chứng. Giá trị độ hấp thụ quang = 0,27 tương ứng với giới hạn của 2-(2-quinolyl)-1,3-indandion là 4 mg/kg. 2-[2-(6-methylquinolyl)]-1,3-indandion được đánh giá như 2-(2-quinolyl)-1,3-indandion. |
|||||||||||||||||||||
Các hợp chất hữu cơ ngoài các thành phần màu |
Các hợp chất hữu cơ ngoài các thành phần màu trong quinolin chỉ có trong chế phẩm sản xuất từ 2-(2-quinolyl)-1,3-indandion. Xác định bằng phương pháp sắc ký lỏng, với các điều kiện như sau: Thiết bị: Sắc ký lỏng phân giải cao có bộ điều khiển gradien nồng độ pha động. Detector: Detector UV cho HPLC có thể đo độ hấp thụ quang tại 254 nm. Cột: Nucleosil, 250X4 mm, 7 mm. Hệ dung môi: A: Đệm acetat pH 4,6:nước (1:10). Đệm acetat bao gồm dung dịch NaOH 1M : acid acetic 1 M : nước (5:10:35). B: (A):methanol (20:80). Nồng độ mẫu 1%(m/v) trong dung môi A. Điều kiện gradient nồng độ pha động:
Tốc độ dòng: 1 ml/phút |
|||||||||||||||||||||
6.2. Định lượng |
|
|||||||||||||||||||||
|
|
Tiến hành theo hướng dẫn trong chuyên luận Xác định tổng hàm lượng bằng phương pháp quang phổ (JECFA monograph 1 – Vol. 4). Dung môi: Đệm photphat pH 7 Pha loãng dung dịch A: từ 10 ml pha đến 250 ml |
|||||||||||||||||||||
|
|
Độ hấp thụ riêng (a): 86,35 Bước sóng hấp thụ cực đại: 415 nm Riêng đối với chế phẩm quinolin sản xuất từ 2-(2-quinolyl)-1,3-indandion xác định tỷ lệ % của di-, mono-, trisulfonat: Sử dụng điều kiện HPLC mô tả trong chuyên luận xác định các hợp chất hữu cơ ngoài thành phần màu, với nồng độ dung dịch mẫu thử trong dung môi HPLC A là 0,05% thay cho 1%. Biểu thị kết quả theo tỷ lệ % tổng các thành phần màu có trong chế phẩm. |
|||||||||||||||||||||
PHỤ LỤC 5
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI SUNSET YELLOW FCF
|
1. Tên khác, chỉ số |
CI Food Yellow 3, FD&C Yellow No. 6; Số CI (1975): 15985 INS: 110 ADI = 0 – 2,5 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 6-hydroxy-5-(4-sulfonphenylazo)-2-naphthalen-6-sulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
dinatri 6-hydroxy-5-(4-sulfonphenylazo)-2-naphthalen-6-sulfonat. |
|
Mã số C.A.S. |
2783-94-0 |
|
Công thức hóa học |
C16H10N2Na2O7S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
452,38 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ cam. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của các chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 5%. Trong đó không được quá 2% các chất màu khác ngoài trinatri 2-hydroxy-1-(4-sulfonphenylazo)naphthalen-3,6-disulfonat. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid 4-amino-1-benzensulfonic; Acid 3-hydroxy-2,7-naphthalendisulfonic; Acid 6-hydroxy-2-naphthalensulfonic; Acid 7-hydroxy-1,3-naphthalendisulfonic; Acid 4,4′-diazoaminodibenzensulfonic; Acid 6,6′-dioxy-2-naphthalensulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; chiều cao của tuyến dung môi ~ 17 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient 2 đến 100% với tốc độ tăng cố định 4%/phút, tiếp theo rửa giải tại 100%. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,5 – 0,6 g mẫu thử; Đệm 10 g natri citrat; Mỗi ml TiCl3 0,1 N tương đương với 11,31 mg các chất màu (D). |
PHỤ LỤC 6QUY YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CARMIN |
|
1. Tên khác, chỉ số |
Cochineal carmin, CI Natural Red 4, CI (1975) No. 75470, INS 120 ADI cho cả nhóm carmin là 0 – 5 mg/kg thể trọng tính theo amoni carminat, các muối Ca, K, Na quy ra tương đương. |
2. Định nghĩa |
Chế phẩm thu được bằng cách chiết từ phẩm yên chi chứa xác khô của rệp son cái (Dactylopius coccus Costa) với nước; Chất màu chính là một phức chelat nhôm ngậm nước của acid carminic, trong phức này tỷ lệ phân tử giữa nhôm và acid carminic là 1/2. Trong chế phẩm thương mại, chất màu chính kết hợp với cation amoni; calci; kali hoặc natri, ở dạng tự do hay kết hợp, các cation này luôn dư. Trong chế phẩm có thể chứa protein từ xác côn trùng nguyên liệu, có thể chứa muối carminat và lượng dư ít cation nhôm. |
Tên hóa học |
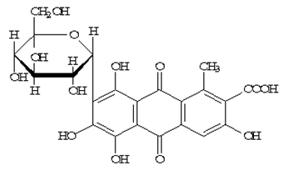
Phức chelat nhôm ngậm nước của acid carminic (7-beta-D-glucopyranosyl-3,5,6,8-tetrahydroxy-1-methyl-9,10-dioxo-anthracen-2-carboxylic acid) |
Mã số C.A.S. |
1390-65-4 (carmin) 1260-17-9 (acid carminic) |
Công thức hóa học |
Acid carminic C22H20O13 |
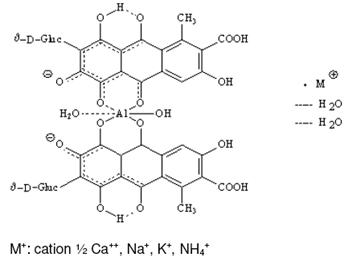
Công thức cấu tạo |
Acid carminic
Phức nhôm của acid carminic
|
Khối lượng phân tử |
Acid carminic: 492,39 |
3. Cảm quan |
Dạng bột hoặc mảnh vụn màu đỏ tới đỏ đậm |
4. Chức năng |
Phẩm màu |
5. Yêu cầu kỹ thuật |
|
5.1. Định tính |
|
Độ tan |
Độ tan của chế phẩm carmin phụ thuộc vào bản chất của cation có mặt trong chế phẩm. Chế phẩm chứa chủ yếu cation amoni (muối amoni carminat) tan tốt trong nước tại pH 3,0 và pH 8,5. Chế phẩm chứa chủ yếu cation calci (muối calci carminat) ít tan trong nước tại pH 3,0 nhưng tan tốt tại pH 8,5. |
Phản ứng màu |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
5.2. Độ tinh khiết |
|
Giảm khối lượng khi làm khô |
Không được quá 20%. |
Tro toàn phần |
Không được quá 12%. |
Protein |
Không được quá 25%. |
Chất không tan trong dung dịch amoniac loãng |
Không được quá 1%. |
Chì |
Không được quá 2 mg/kg. |
Yêu cầu về vi sinh vật |
Salmonella: Âm tính. |
5.3. Hàm lượng C22H20O13 |
Không thấp hơn 50% C22H20O13 tính theo chế phẩm đã làm khô. |
6. Phương pháp thử |
|
6.1 Đính tính |
|
Phản ứng màu |
– Kiềm hóa nhẹ dung dịch mẫu thử bằng cách thêm 1 giọt dung dịch natri hydroxyd (hoặc kali hydroxyd) 10%. Dung dịch chuyển sang màu tím. – Thêm một ít tinh thể natri dithionit (Na2S2O4) vào các dung dịch mẫu thử trung tính, đã kiềm hóa, đã acid hóa. Các dung dịch này không bị mất màu. – Làm khô lượng nhỏ mẫu thử trên đĩa sứ. Để nguội hoàn toàn, nhỏ 1-2 giọt thuốc thử acid sulfuric vào cặn còn lại trên đĩa. Màu của cặn không thay đổi. – Acid hóa dung dịch mẫu thử trong nước bằng dung dịch thuốc thử acid hydrocloric, thể tích thuốc thử bằng 1/3 thể tích dịch thử, cho thêm rượu amylic, lắc đều. Tách lấy lớp rượu amylic và rửa 2-4 lần với đồng thể tích nước cất để loại hòan toàn acid hydrocloric. Pha loãng phần rượu amylic với ether dầu hoả (40-60 0) đồng thể tích hoặc thể tích ether dầu hoả gấp đôi, lắc vài lần với một ít nước cất để loại hết màu. Thêm, nhỏ từng giọt dung dịch urani acetat 5%, lắc đều sau mỗi lần thêm. Dung dịch chuyển sang màu xanh lục ngọc đặc trưng. |
6.2 Độ tinh khiết |
|
Giảm khối lượng khi làm khô |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – sấy tại 135 oC trong 3 giờ. |
Tro toàn phần |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – chuyên luận xác định tro, cân 1 g mẫu. |
Protein |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – chuyên luận xác định Nitơ phi amoni X 6,25 |
Chất không tan trong dung dịch amoniac loãng |
Cân 0,25 g (chính xác đến mg) mẫu thử đã được làm khô, hoàn tan trong 2,5 ml dung dịch amoniac loãng (160 ml dung dịch thuốc thử amoniac đặc, thêm nước cất đến 500 ml) và pha loãng với nước cất đến 100 ml, thu được dung dịch trong. Lọc dung dịch này qua phễu thuỷ tinh xốp. Rửa phễu với dung dịch amoniac 0,1% và làm khô đến khối lượng không đổi tại 105o. |
Chì |
Xác định bằng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
6.3. Định lượng |
|
|
|
Cân 100 mg (chính xác đến mg) mẫu thử, hoà tan vào 30 ml dung dịch acid hydrocloric 2N sôi, làm nguội. Chuyển toàn bộ dung dịch sang bình định mức 1000 ml, pha loãng và định mức tới vạch bằng nước cất, lắc đều. Xác định độ hấp thụ quang của dung dịch tại bước sóng hấp thụ cực đại khoảng 494 nm, sử dụng mẫu trắng là nước cất, cuvet đo có độ dày 1 cm. Tính hàm lượng % acid carminic trong mẫu thử theo công thức: (100 × A × 100) / (1,39 × W) trong đó: A = độ hấp thụ quang của dung dịch mẫu thử; W = Khối lượng mẫu thử,tính bằng mg; 1,39 = độ hấp thụ quang của dung dịch acid carminic nồng độ 100 mg/1000 ml; Nếu độ hập thụ quang đo được không nằm trong khoảng giá trị 0,65 – 0,75, chuẩn bị mẫu thử khác và hiệu chỉnh khối lượng mẫu thử thích hợp. |
PHỤ LỤC 7
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CARMOISIN
|
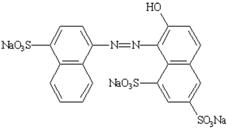
1. Tên khác, chỉ số |
CI Food Red 3, Azorubine; CI (1975): 14720 INS: 122 ADI = 0 – 4 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 4-hydroxy-3-(4-sulfon-1-naphthylazo)-1-naphthalensulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
dinatri 4-hydroxy-3-(4-sulfon-1-naphthylazo)-1-naphthalensulfonat. |
|
Mã số C.A.S. |
3567-69-9 |
|
Công thức hóa học |
C20H12N2Na2O7S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
502,44 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 1%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid 4-Amino-1-naphthalensulfonic và acid 4-hydroxy-1-naphthalensulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1 Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; chiều cao của tuyến dung môi ~ 17 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient từ 2% đến 100% với tốc độ tăng cố định 2%/phút. |
|
6.3. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,5 – 0,6 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 12,56 mg các chất màu (D). |
PHỤ LỤC 8
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI AMARANTH
|
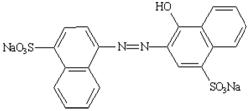
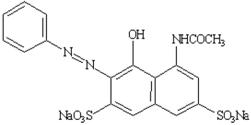
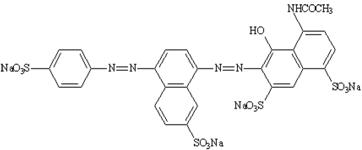
1. Tên khác, chỉ số |
CI Food Red 9, Naphtol Rot S.; CI (1975): 16185 INS: 123 ADI = 0 – 0,5 mg/kg thể trọng |
|
2. Định nghĩa |
Chủ yếu gồm trinatri 3-hydroxy-4-(4-sulfon-1-naphthylazo)-2,7-naphthalendisulfonat và các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
trinatri 3-hydroxy-4-(4-sulfon-1-naphthylazo)-2,7-naphthalendisulfonat |
|
Mã số C.A.S. |
915-67-3 |
|
Công thức hóa học |
C20H11N2Na3O10S3 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
604,48 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu nâu đỏ hoặc nâu đỏ sẫm. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 3%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid 4-amino-1-naphthalensulfonic; acid 3-hydroxy-2,7-naphthalendisulfonic; acid 6-hydroxy-2-naphthalensulfonic; acid 7-hydroxy-1,3-naphthalendisulfonic và acid 7-hydroxy-1,3,6- naphthalen-trisulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1 Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 3; chiều cao của tuyến dung môi ~ 17 cm, sau 1 giờ khai triển. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient 2 đến 100% với tốc độ tăng cố định 4%/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,7 – 0,8 g mẫu thử; Đệm 10 g natri citrat; Mỗi ml TiCl3 0,1 N tương đương với 15,11 mg các chất màu (D). |
PHỤ LỤC 9
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI PONCEAU 4R
|
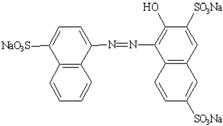
1. Tên khác, chỉ số |
CI Food Red 7, Cochineal Red A ; New Cochineal; CI (1975): 16255 INS: 124 ADI = 0 – 4 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm trinatri d-2-hydroxy-1-(4-sulfon-1-naphthylazo)-6,8-naphthalendisulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Trinatri-2-hydroxy-1-(4-sulfon-1-naphthylazo)-6,8-naphthalendisulfonat |
|
Mã số C.A.S. |
2611-82-7 |
|
Công thức hóa học |
C20H11N2Na3O10S3.1,5H2O |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
631,51 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 20% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 1%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid 4-amino-1-naphthalensulfonic; acid 7-hydroxy-1,3-naphthalendisulfonic; acid 3-hydroxy-2,7-naphthalensulfonic; acid 6-hydroxy-2-naphthalensulfonic và acid 7-hydroxy-1,3,6-naphthalentrisulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 3; chiều cao của tuyến dung môi ~ 17 cm, sau 1 giờ khai triển. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient 2 đến 100% với tốc độ tăng cố định 2%/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,7 – 0,8 g mẫu thử; Đệm 10 g natri citrat; Mỗi ml TiCl3 0,1 N tương đương với 15,78 mg các chất màu (D). |
PHỤ LỤC 10
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI ERYTHROSIN
|
1. Tên khác, chỉ số |
CI Food Red 14, FD&C Red No. 3; CI (1975): 45430 INS 127 ADI = 0 – 0,1 mg/kg thể trọng |
|||
|
2. Định nghĩa |
Chủ yếu là muối dinatri 9-(o-carboxyphenyl)-6-hydroxy-2,4,5,7-tetraiodo-3-isoxanthon monohydrat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|||
|
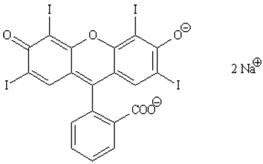
Tên hóa học |
Muối dinatri 9-(o-carboxyphenyl)-6-hydroxy-2,4,5,7-tetraiodo-3-isoxanthon monohydrat |
|||
|
Mã số C.A.S. |
16423-68-0 |
|||
|
Công thức hóa học |
C20H6I4Na2O5.H2O |
|||
|
Công thức cấu tạo |
|
|||
|
Khối lượng phân tử |
897,88 |
|||
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ. |
|||
|
4. Chức năng |
Phẩm màu. |
|||
|
5. Yêu cầu kỹ thuật |
||||
|
5.1. Định tính |
|
|||
|
Độ tan |
Tan trong nước và trong ethanol |
|||
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|||
|
5.2. Độ tinh khiết |
|
|||
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 13% cùng với clorid và sulfat tính theo muối natri. |
|||
|
Iod vô cơ |
Không được quá 0,1% tính theo natri iodid. |
|||
|
Chất không tan trong nước |
Không được quá 0,2%. |
|||
|
Kẽm |
Không được quá 50 mg/kg. |
|||
|
Chì |
Không được quá 2 mg/kg. |
|||
|
Các chất màu phụ |
Không được quá 4% (không bao gồm Fluorescein). |
|||
|
Fluorescein |
Không được quá 20 mg/kg. |
|||
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,2% Tri iodoresorcinol Không được quá 0,2% acid 2-(2,4-dihydroxy-3,5-di-iodobenzoyl) benzoic |
|||
|
Các chất có thể chiết bằng ether |
Không được quá 0,2% đối với dung dịch mẫu thử pH <> |
|||
|
5.3. Hàm lượng |
Không được thấp hơn 87% tổng các chất màu. |
|||
|
6. Phương pháp thử |
||||
|
6.1. Độ tinh khiết |
|
|||
|
Iod vô cơ |
Cân 1,0 g mẫu thử vào một cốc có mỏ 100 ml. Thêm 75 ml nước cất, dùng máy khuấy từ khuấy cho tan hoàn toàn. Cho điện cực đặc trưng cho iod và một điện cực so sánh vào dung dịch và đặt máy đo thế ở thang đo thích hợp. Đọc thế của hệ (mV). Dùng buret thêm dung dịch bạc nitrat 0,001 M, đầu tiên mỗi lần thêm 0,5 ml, khi gần đến điểm tương đương (nhận biết bằng sự thay đổi điện thế sau mỗi lần thêm) giảm còn 0,1 ml/lần, để ổn định và đọc điện thế của hệ sau mỗi lần thêm (mV). Tiến hành chuẩn độ đến khi thêm dung dịch bạc nitrat 0,001 M mà không làm thay đổi điện thế dung dịch nhiều. Vẽ đường biểu thị sự phụ thuộc giữa điện thế dung dịch (mV) vào thể tích dung dịch bạc nitrat 0,001 M thêm vào. Điểm tương đương được xác định là điểm mà thể tích dung dịch bạc nitrat 0,001 M thêm vào tương ứng với độ dốc của đường đồ thị lớn nhất. Hàm lượng natri iodid trong mẫu được tính = độ chuẩn x 0,015%. |
|||
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|||
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 5; chiều cao của tuyến dung môi ~ 17 cm. Chú ý: Không để bản mỏng sắc ký trực tiếp ra ngoài sánh sáng mặt trời |
|||
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký cột với các điều kiện hấp thụ như sau: Tri-iodoresorcinol: 0,079 mgL-1cm-1 tại bước sóng 233 nm, trong môi trường acid. Acid 2-(2,4-dihydroxy-3,5-di-iodobenzoyl) benzoic: 0,047 mgL-1cm-1 tại bước sóng 348 nm, trong môi trường kiềm. |
|||
|
Fluorescein |
Nguyên tắc: Fluorescein được tách khỏi mẫu thử bằng sắc ký lớp mỏng (TLC) và so sánh với sắc ký đồ của Fluorescein chuẩn tại nồng độ tương ứng với giới hạn quy định. Dung môi: Methanol + nước + dung dịch amoniac (khối lượng riêng ~ 0,890) (500 ml + 400 ml + 100 ml). Chuẩn bị mẫu: Cân 1,0 g mẫu thử, hòa tan trong khoảng 50 ml dung môi và pha loãng đến đủ 100 ml. Chuẩn: Cân chính xác lượng Fluorescein (đã tinh chế bằng cách kết tinh lại trong ethanol) tương đương với 1 g x hàm lượng các chất màu trong mẫu (xác định trong phần định lượng). Hòa tan trong nước (hoặc trong nước có 10 ml dung dịch amoniac có khối lượng riêng ~ 0,890 nếu sử dụng acid không có Fluorescein), pha loãng và định mức đến đủ 100 ml. Tiến hành pha loãng theo các bước liên tiếp như sau: Hút 1ml pha loãng đến đủ 100 ml bằng nước. Hút 1ml pha loãng đến đủ 100 ml bằng nước. Hút 20 ml pha loãng đến đủ 100 ml bằng dung môi. Dung môi sắc ký: n-Butanol + nước + dung dịch amoniac (khối lượng riêng ~ 0,890) + ethanol (100 ml + 44 ml + 1 ml + 22,5 ml). Tiến hành: Lần lượt chấm cạnh nhau 25 mL dung dịch thử và dung dịch chuẩn trên cùng 1 bản mỏng cellulose. Khai triển trong hệ dung môi sắc ký trong 16 giờ. Để khô bản mỏng. Soi dưới đèn UV và so sánh huỳnh quang của vết thử với vết chuẩn. Mật độ huỳnh quang của vết thử không được quá vết chuẩn. Chú ý: không để bản mỏng ra ánh sáng mặt trời trực tiếp. |
|||
|
6.2. Định lượng |
|
|||
|
|
Cân 1 g (chính xác đến mg) mẫu thử, hòa tan trong 250 ml nước, chuyển vào một cốc 500 ml sạch, thêm 8,0 ml acid nitric 1,5 N, khuấy đều. Lọc qua phễu lọc thủy tinh xốp (độ xốp 3, đường kính 5 cm), chứa sẵn đũa thủy tinh và đã cân bì. Rửa cặn bằng acid nitric 0,5% đến khi dịch rửa không bị đục khi thử với dung dịch bạc nitrat (TS), sau đó với 30 ml nước cất. Sấy tại nhiệt độ 135±5 oC đến khối lượng không đổi. Cẩn thận phá cặn bằng đũa thủy tinh,để nguội trong bình hút ẩm và cân.
Xác định Chất không tan trong acid hydrocloric trong màu nhôm erythrosin Hóa chất, thuốc thử: Acid hydrocloric đặc Acid hydrocloric 0,5% (tt/tt) Dung dịch amoniac loãng (pha loãng 10 ml dung dịch amoniac có khối lượng riêng =0,890 bằng nước đến đủ 100 ml). Tiến hành: Cân khoảng 5 g (chính xác đến mg) mẫu thử vào cốc 500 ml. Thêm 250 ml nước và 60 ml acid hydrocloric đặc. Đun sôi để hòa tan nhôm trong khi đó erythrosin chuyển về dạng acid tự do, không tan trong acid. Lọc qua phễu lọc thủy tinh xốp số 4 đã cân bì. Rửa cặn với một lượng nhỏ acid hydrocloric 0,5% nóng, sau đó với nước cất nóng. Loại bỏ dịch rửa acid, lấy phễu thủy tinh xốp ra và rửa phễu bằng dung dịch amoniac loãng đến khi dịch rửa không có màu. Sấy tại 135 oC đến khối lượng không đổi. Cân phễu và tính khối lượng cặn còn lại và tính hàm lượng % so với khối lượng mẫu đã lấy. |
|||
PHỤ LỤC 11
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI RED 2G
|
1. Tên khác, chỉ số |
CI Food Red 10, Azogeranine; CI (1975): 18050 INS: 128 ADI = 0 – 1 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 8-acetamido-1-hydroxy-2-phenylazo-3,6-naphthalendisulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 8-acetamido-1-hydroxy-2-phenylazo-3,6-naphthalendisulfonat |
|
Mã số C.A.S. |
3734-67-6 |
|
Công thức hóa học |
C18H13N3Na2O8S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
509,43 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 20% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 2%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,3% tổng các acid 5-acetamido-4-hydroxy-2,7-naphthalen-2,7-disulfonic và acid 5-Amino-4-hydroxy-2,7-naphthalen-2,7-disulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 80% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; chiều cao của tuyến dung môi ~ 17 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật HPLC với các điều kiện như sau: HPLC rửa giải gradient 2 đến 100% với tốc độ tăng cố định 2%/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,6 – 0,7 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 12,74 mg các chất màu (D). |
PHỤ LỤC 12
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI ALLURA RED AC
|
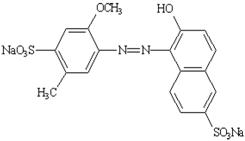
1. Tên khác, chỉ số |
CI Food Red 17, FD&C Red No. 40; CI (1975): 16035 INS: 129 ADI = 0 – 7 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 6-hydroxy-5-(2-methoxy-5-methyl-4-sulfon-phenylazo)-2-naphthalen-sulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 6-hydroxy-5-(2-methoxy-5-methyl-4-sulfon-phenylazo)-2-naphthalen-sulfonat |
|
Mã số C.A.S. |
25956-17-6 |
|
Công thức hóa học |
C18H14N2Na2O8S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
496,43 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu đỏ sẫm. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 3%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,3% Natri 6-hydroxy-2-naphtalen sulfonat; Không được quá 0,2% acid 4-amino-5-methoxy-2-methyl-benzen-sulfonic; Không được quá 1,0% dinatri 6,6′-oxybis(2-naphthalen-sulfonat); |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1 Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; chiều cao của tuyến dung môi ~ 17 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký lỏng dưới các điều kiện như sau: HPLC rửa giải gradient từ 0% đến 18% với tốc độ tăng cố định 1%/phút; 18 đến 62% với tốc độ tăng cố định 7%/phút, sau đó rửa giải tại 100%, tốc độ dòng 0,6 ml/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,5 – 0,6 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 12,41 mg các chất màu (D). |
PHỤ LỤC 13
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI INDIGOTIN
|
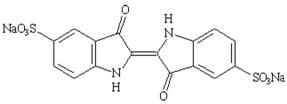
1. Tên khác, chỉ số |
Indigocarmin; CI Food Blue 1, FD&C Blue No. 2; CI (1975): 73015 INS: 132 ADI = 0 – 5 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 3,3′ -dioxo-[delta2,2′-biindolin]-5,5′-disulfonat và dinatri 3,3′-dioxo-[delta2,2′-biindolin]-5,7′-disulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 3,3′ -dioxo-[delta2,2′-biindolin]-5,5′-disulfonat |
|
Mã số C.A.S. |
860-22-0 (đồng phân 5,5′) |
|
Công thức hóa học |
C16H8N2Na2O8S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
466,36 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu xanh lam. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 1% (không bao gồm dinatri 3,3′-dioxo-[delta2,2′-biindolin]-5,7′-disulfonat). |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid isatin-5-sulfonic; acid 5-sulfoanthranilic và acid anthranilic |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. Không được quá 18% dinatri 3,3′-dioxo-[delta2,2′-biindolin]-5,7′-disulfonat. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 3; Chiều cao tuyến dung môi ~ 17 cm. Chú ý 1: Đồng phân 5,7′ được tách ra là một vùng màu xanh lớn ngay trước vết chính màu xanh. Không tính vùng này vào khi xác định các chất màu phụ. Chú ý 2: 15 ml dung dịch natri hydro carbonat sử dụng trong quy trình chung được thay thế bằng dung dịch acid hydrocloric 0,05 N để tránh sự phân hủy xảy ra khi indigo sulfon hóa trong môi trường kiềm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký lỏng với các điều kiện như sau: HPLC rửa giải gradient từ 2 đến 100%, sau đó tiếp tục rửa giải tại 100%. |
|
Các chất có thể chiết bằng ether |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Cân 2 g mẫu thử thay cho hướng dẫn cân 5 g mẫu trong phần các phương pháp chung. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 1,0 – 1,1 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 23,32 mg các chất màu (D). Xác định đồng phân bằng sắc ký giấy: Tiến hành theo các điều kiện hướng dẫn cho phần xác định hàm lượng các chất màu phụ. Cắt vết sắc ký tương ứng của đồng phân trên sắc ký đồ, theo hướng dẫn cắt vết màu phụ. Chiết vào dung môi và đo hấp thụ quang tại Smax của nó. Tiến hành đo mẫu trắng song song tại cùng điều kiện. Sử dụng 0,1 ml dung dịch mẫu thử làm chuẩn, chấm lên bản giấy hình chữ nhật 18 cm x 0,7 cm. Hàm lượng (%) đồng phân trong mẫu được tính như sau % = [A / As] x 20% x [D / 100] Trong đó: A là độ hấp thụ (đã hiệu chỉnh với mẫu trắng) của đồng phân. As là độ hấp thụ (đã hiệu chỉnh với mẫu trắng) của chuẩn. D là hàm lượng tổng chất màu trong mẫu. Xác định đồng phân bằng HPLC: Đồng phân 5,7′ được tách bằng HPLC với điều kiện để tách các chất màu phụ nêu trên và định lượng. |
PHỤ LỤC 14
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI BRILLIANT BLUE FCF
|
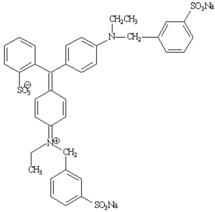
1. Tên khác, chỉ số |
CI Food Blue 2, FD&C Blue No. 1; CI (1975): 42900 INS: 133 ADI = 0 – 1 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 3-[N-ethyl-N-[4-[[4-[N-ethyl-N-(3-sulfonbenzyl)-amino] phenyl] (2-sulfonphenyl)methylen]-2,5-cyclohexadien-1-yliden] amonimethyl] benzensulfonat và các đồng phân của nó cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 3-[N-ethyl-N-[4-[[4-[N-ethyl-N-(3-sulfonbenzyl)-amino] phenyl] (2-sulfonphenyl)methylen]-2,5-cyclohexadien-1-yliden] amonimethyl] benzensulfonat. Dinatri I-[4-(N-ethyl-3-sulfonatobenzylamino)phenyl]-I- [4-(N-ethyl-3-sulfonatobenzyliminio)cyclohexa-2,5-dienyli-den]toluen-2-sulfonat (Tên hóa học khác). |
|
Mã số C.A.S. |
3844-45-9 |
|
Công thức hóa học |
C37H34N2Na2O9S3 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
792,86 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu xanh lam. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Crom |
Không được quá 50 mg/kg. |
|
Các chất màu phụ |
Không được quá 6%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 1,5% tổng các acid 2-; 3- và 4-formylbenzensulfonic. Không được quá 0,3% acid 3-[[N-ethyl-N-(4-sulfophenyl) amino] methyl] benzensulfonic. |
|
Leuco base |
Không được quá 5%. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện sau: Dung môi khai triển là dung môi số 4; Khai triển dung môi trong 20 giờ. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký cột với các điều kiện hấp thụ như sau: acid 3-formylbenzensulfonic: 0,0495 mgL-1cm-1 tại bước sóng 246 nm, trong HCl loãng. acid 3-[[N-ethyl-N-(4-sulfophenyl) amino] methyl] benzensulfonic: 0,078 mgL-1cm-1 tại bước sóng 277 nm, trong dung dịch amoniac loãng. |
|
Leuco base |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Cân 120 ± 5 mg mẫu thử và tiến hành theo hướng dẫn trong chuyên luận xác định Leuco base trong chất màu nhóm Triarylmethan sulfon hóa; Độ hấp thụ riêng (a) = 0,164 mgL-1cm-1 tại bước sóng ~ 630 nm; tỷ số = 0,9706. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 1,8 – 1,9 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 39,65 mg các chất màu (D). |
PHỤ LỤC 15
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CHLOROPHYLL
1. Tên khác, chỉ số |
Magnesium chlorophyll, Magnesium phaeophytin; Clorophyllin; C.I. Natural Green 3; C.I. (1975): 75810; INS 140 ADI “không giới hạn” . |
||||||||||||
2. Định nghĩa |
Thu được bằng cách chiết cỏ, cỏ linh lăng, tầm ma và các nguyên liệu thực vật khác với dung môi; Sản phẩm sau khi đã loại dung môi ở dạng kết hợp với magnesi, có thể loại hoàn toàn hoặc 1 phần từ clorophyll để thu được phaeophytin tương ứng; Thành phần màu chính là các phaeophytin và magnesi clorophyll. Sản phẩm chiết sau khi loại dung môi chứa các chất màu khác như carotenoid, sáp và chất béo có nguồn gốc từ nguyên liệu. Chỉ được sử dụng những dung môi sau để chiết: aceton, dicloromethan, methanol, ethanol, propan-2-ol và hexan. |
||||||||||||
Tên hóa học |
Các chất màu chính là: Phytyl (132R,17S,18S)-3-(8-ethyl-132-methoxycarbonyl-2,7,12,18-tetramethyl-13′-oxo-3-vinyl-131-132-17,18-tetrahydrocyclopenta [at]-prophylrin-17-yl) propionat (Pheophytin a), hoặc phức magnesi (Clorophyll a). Phytyl (132R,17S,18S)-3-(8-ethyl-7-formyl-132-methoxycarbonyl-2,12,18-trimethyl-13′-oxo-3-vinyl-131-132-17,18-tetrahydro-cyclopenta [at]-prophylrin-17-yl) propionat, (Pheophytin b), hoặc phức magnesi (Clorophyll b). |
||||||||||||
Mã số C.A.S. |
Phaeophytin a, phức magnesi: 479-61-8 Phaeophytin b, phức magnesi: 519-62-0 |
||||||||||||
Công thức hóa học |
Phức magnesi phaeophytin a (Clorophyll a): C55H72MgN4O5 Phaeophytin a: C55H74N4O5 Phức magnesi phaeophytin b (Clorophyll a): C55H70MgN4O6 Phaeophytin b: C55H72N4O6 |
||||||||||||
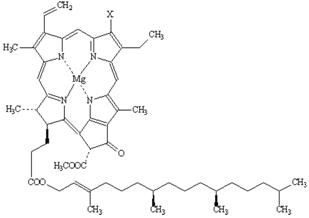
Công thức cấu tạo |
Trong đó: X = CH3 đối với các hợp chất “a” X = CHO đối với các hợp chất “b”. Mất Mg sẽ chuyển dạng từ clorophyll thành phaeophytin |
||||||||||||
Khối lượng phân tử |
Phức magnesi phaeophytin a (Clorophyll a): 893,51 Phaeophytin a: 871,22 Phức magnesi phaeophytin (Clorophyll a): 907,49 Phaeophytin : 885,20 |
||||||||||||
3. Cảm quan |
Chất rắn dạng sáp có màu từ xanh oliu đến xanh lục thẫm tùy thuộc vào lượng magnesi kết hợp. |
||||||||||||
4. Chức năng |
Phẩm màu. |
||||||||||||
5. Yêu cầu kỹ thuật |
|||||||||||||
5.1. Định tính |
|
||||||||||||
Độ tan |
Không tan trong nước; tan trong cồn, diethyl ether; cloroalkan, hydrocarbon và dầu không bay hơi. |
||||||||||||
Sắc ký lớp mỏng |
Đạt yêu cầu (mô tả trong phần phương pháp thử) |
||||||||||||
5.2. Độ tinh khiết |
|
||||||||||||
Dung môi tồn dư |
Aceton, methanol, ethanol, propan-2-ol, hexan: Không được quá 50 mg/kg, đơn chất hoặc kết hợp. Dicloromethan: Không được quá 10 mg/kg |
||||||||||||
Arsen |
Không được quá 3 mg/kg. (Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Phương pháp II). |
||||||||||||
Chì |
Không được quá 5 mg/kg. (Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ). |
||||||||||||
5.3. Hàm lượng |
Tổng hàm lượng các phaeophytin và các phức magnesi của nó không thấp hơn 10%. |
||||||||||||
6. Phương pháp thử |
|||||||||||||
6.1. Định tính |
|
||||||||||||
Sắc ký lớp mỏng |
Chấm dung dịch mẫu thử 1/20 trong cloroform lên bản mỏng Silica 60C thành 1 vạch dài 2 cm. Sau khi bản mỏng khô, khai triển bản mỏng trong hệ dung môi gồm 50% hexan, 45% |
||||||||||||
|
|
cloroform và 5% ethanol (thông thường cloroform với độ tinh khiết thuốc thử đã chứa sẵn 2% ethanol để làm ổn định. 5% ethanol là không tính đến lượng ethanol có sẵn này) đến khi tuyến dung môi đạt 15 cm cách điểm xuất phát. Để dung môi bay hơi, sau đó quan sát các vết riêng biệt và xác định vết tương ứng với cấu tử quan tâm thông qua Rf và màu. Giá trị Rf gần đúng và màu của các vết như sau: phaeophytin a: 0,77; màu xám/nâu phaeophytin b: 0,75; màu vàng/nâu Clorophyll a: 0,50; màu xanh lam/xanh lục Clorophyll b: 0,63; màu vàng/xanh lục Ngoài ra còn quan sát thấy các vết của b-caroten tại Rf 0,81 và xanthophyll tại Rf 0,47 và 0,23. |
||||||||||||
6.2. Độ tinh khiết |
|
||||||||||||
Dung môi tồn dư |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Xác định bằnh Sắc ký khí hoặc bằng phương pháp cất cuốn (chuyên luận Xác định dung môi tồn dư) hoặc phân tích không gian hơi (chuyên luận Thử giới hạn dung môi tồn dư). |
||||||||||||
Arsen |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Phương pháp II. |
||||||||||||
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ). |
||||||||||||
6.1. Định lượng |
Cân khoảng 100 mg (chính xác đến mg) mẫu thử, hòa tan trong diethyl ether đến đủ 100 ml. Lấy 2 ml dung dịch này, pha loãng với diethyl ether vừa đủ 25 ml. Độ hấp thụ quang của mẫu tại nồng độ này khi đo tại bước sóng 660,4 nm không được vượt quá 0,7 so với thang đo độ hấp thụ. Đo độ hấp thụ quang (A) của dung dịch này trong cuvet 1 cm so với mẫu trắng là diethyl ether tại bước sóng 660,4 nm; 642,0 nm; 667,2 nm; 654,4 nm. (các bước sóng này lần lượt là cực đại hấp thụ trong diethyl ether của clorphyll a; clorophyll b; phaeophtin a và đồng phaeophytin b, tương ứng). Ngoài ra đo thêm tại bước sóng 649,8 nm và 628,2 nm. Phần dung dịch đã pha loãng còn lại, thêm vào 1 tinh thể acid oxalic, hòa tan và lắc đều. Đo lại độ hấp thụ quang của dung dịch tại các bước sóng đã cho. “dA” là sự chênh lệch độ hấp thụ quang của dung dịch đo tại cùng bước sóng trước và sau khi thêm acid oxalic. Tính nồng độ từng chất (mmol/L) theo các phương trình sau: Clorophyll a = 17,7 d A (660,4 nm) + 7,15 d A (642,0 nm) Clorophyll b = 19,4 d A (642,0 nm) – 2,92 d A (660,4 nm) Phaeophytin a = -4,89 A (649,8 nm) + 0,0549 A (628,2 nm) +18,7 A (667,2 nm) + 0,0575 A (654,4 nm) – clorophyll a Phaeophytin b = -71,0 A (649,8 nm) + 2,51 A (628,2 nm) – 13,5 A (667,2 nm) + 84,3 A (654,4 nm) – clorophyll b Chuyển từ mmol/L sang hàm lượng % theo phương trình sau:
|
||||||||||||
|
|
|||||||||||||
PHỤ LỤC 16
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CHLOROPHYLL PHỨC ĐỒNG
1. Tên khác, chỉ số |
Copper chlorophyllin, copper phaeophytin C.I. Natural Green 3; C.I. (1975) No. 75810; INS: 141i ADI = 0 – 15 mg/kg thể trọng. |
|||
2. Định nghĩa |
Thu được khi thêm muối đồng hữu cơ vào sản phẩm thu được khi chiết cỏ, cỏ linh lăng, tầm ma và các nguyên liệu thực vật khác với dung môi; Sản phẩm sau khi đã loại dung môi chứa các chất màu khác như carotenoid cũng như sáp và chất béo. Chất màu chính là đồng phaeophytin. Chỉ được sử dụng những dung môi sau để chiết: aceton, dicloromethan, methanol, ethanol, propan-2-ol và hexan. |
|||
Tên hóa học |
Chất màu chính ở dạng acid của nó là [Phytyl (132R, 17S, 18S)-3-(8-ethyl-132-methoxycarbonyl-2,7,12,18-tetramethyl-13-oxo-3-vinyl-131, 132,17,18-tetrahydroxypenta[at]-prophyrin-17-yl) propionat] đồng II (Đồng phaeophytin a) [Phytyl (132R, 17S, 18S)-3-(8-ethyl-7-formyl-132-methoxycarbonyl-2,12,18-trimethyl-13-oxo-3-vinyl-131, 132,17,18-tetrahydroxypenta[at]-prophyrin-17-yl) propionat] đồng II (Đồng phaeophytin b). |
|||
Mã số C.A.S |
65963-40-8 |
|||
Công thức hóa học |
Đồng phaeophytin a (dạng acid): C55H72CuN4O5 Đồng phaeophytin b (dạng acid): C55H70CuN4O6 |
|||
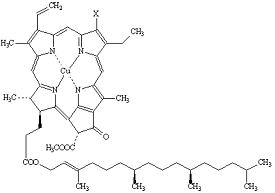
Công thức cấu tạo |
Trong đó: X = CH3 đối với hợp chất “a” X = CHO đối với hợp chất “b” |
|||
|
Khối lượng phân tử |
Đồng phaeophytin a: 932,75 Đồng phaeophytin b: 943,73 |
|||
3. Cảm quan |
Chất rắn dạng sáp có màu từ xanh lục đến xanh lục thẫm tùy thuộc vào nguồn nguyên liệu. |
|||
4. Chức năng |
Phẩm màu. |
|||
5. Tính chất |
||||
5.1. Định tính |
|
|||
Độ tan |
Không tan trong nước; tan trong cồn, diethyl ether; cloroalkan, hydrocarbon và dầu không bay hơi. |
|||
Quang phổ |
A (1%, 1 cm) của mẫu thử trong cloroform, đo tại 405 nm không được thấp hơn 54. |
|||
Sắc ký lớp mỏng |
Đạt yêu cầu (mô tả trong phần phương pháp thử). |
|||
5.2. Độ tinh khiết |
|
|||
Dung môi tồn dư |
Aceton, methanol, ethanol, propan-2-ol, hexan: Không được quá 50 mg/kg, đơn chất hoặc hợp chất. Dicloromethan: Không được quá 10 mg/kg. |
|||
Đồng tự do có thể ion hóa |
Không được quá 200 mg/kg. |
|||
Đồng tổng số |
Không được quá 8% tính theo tổng số đồng phaeophytin. |
|||
Arsen |
Không được quá 3 mg/kg. |
|||
Chì |
Không được quá 5 mg/kg. |
|||
5.3. Hàm lượng |
Không thấp hơn 10% tổng số đồng phaeaphytin. |
|||
6. Phương pháp thử |
||||
5.1. Định tính |
|
|||
Sắc ký lớp mỏng |
Chấm dung dịch mẫu thử 1/20 trong cloroform lên bản mỏng Silica 60C thành 1 vạch dài 2 cm. Sau khi bản mỏng khô, khai triển bản mỏng trong hệ dung môi gồm 50% hexan, 45% cloroform và 5% ethanol (thông thường cloroform với độ tinh khiết thuốc thử đã chứa sẵn 2% ethanol để làm ổn định. 5% ethanol là chưa tính đến lượng ethanol có sẵn này) đến khi tuyến dung môi đạt 15 cm cách điểm xuất phát. Để dung môi bay hơi, sau đó quan sát các vết riêng biệt và xác định vết tương ứng với cấu tử quan tâm thông qua Rf và màu. Giá trị Rf gần đúng và màu của các vết như sau: Đồng phaeophytin a: 0,5; màu xanh lục Đồng phaeophytin b: 0,73; màu vàng/xanh lục Ngoài ra còn quan sát thấy các vết của b-caroten tại Rf 0,81 và xanthophyll tại Rf 0,47 và 0,23. |
|||
5.2. Độ tinh khiết |
|
|||
Dung môi tồn dư |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Xác định bằnh Sắc ký khí hoặc bằng phương pháp cất cuốn (chuyên luận Xác định dung môi tồn dư) hoặc phân tích không gian hơi (chuyên luận Thử giới hạn dung môi tồn dư). |
|||
Đồng tự do có thể ion hóa |
Cân khoảng 1 g (chính xác đến mg) mẫu thử và hòa tan trong 20 ml dầu lạc, đun nóng nhẹ cho tan hoàn toàn. Thêm chính xác 200 ml nước, khuấy bằng máy khuấy từ, và điều chỉnh tới pH 3,0 bằng cách thêm cẩn thận acid hydrocloric 0,5 N (tránh thêm quá nhanh). Để yên hỗn hợp trong 10 phút. Nếu cần, điều chỉnh lại tới pH 3,0 bằng cách thêm cẩn thận acid hydrocloric 0,5 N. Chuyển sang phễu tách và để yên 20 phút. Lọc lớp nước qua giấy lọc Whatman No. 50, bỏ 10 ml dịch lọc đầu. Dùng dung dịch này để phân tích đồng bằng quang phổ hấp thụ nguyên tử – JECFA monograph 1-Vol. 4. |
|||
Đồng tổng số |
Cân khoảng 0,1 g (chính xác đến mg) mẫu thử, cho vào đĩa silica, nung ở nhiệt độ không quá 500 ºC, tới khi loại đi toàn bộ than; làm ẩm tro bằng một hoặc hai giọt acid sulfuric đặc và tro hóa lại. Hòa tan tro bằng cách đun sôi 3 lần, mỗi lần với 5 ml acid hydrocloric 10% (kl/kl), lọc dịch acid thu được sau mỗi lần thêm acid qua cùng một phễu giấy lọc nhỏ vào bình định mức 100 ml. Để nguội, và thêm nước tinh khiết tới vạch. Dùng dung dịch này để phân tích đồng bằng quang phổ hấp thụ nguyên tử – xem JECFA monograph 1-Vol. 4. |
|||
Arsen |
– Thử theo hướng dẫn tại JECFA monograph 1 – Vol.4 – Phương pháp II. |
|||
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|||
6.3. Định lượng |
Cân khoảng 100 mg (chính xác đến mg) mẫu thử, hòa tan trong diethyl ether đến đủ 100 ml. Lấy 2 ml dung dịch này, pha loãng với diethyl ether vừa đủ 25 ml. Độ hấp thụ quang của mẫu tại nồng độ này khi đo tại bước sóng 660,4 nm không được vượt quá 0,7 so với thang đo độ hấp thụ. Đo độ hấp thụ quang (A) của dung dịch này trong cuvet 1 cm so với mẫu trắng là diethyl ether tại bước sóng 667,2 nm; 654,4 nm; 649,8 nm và 628,2 nm. (hai bước sóng sau là cực đại hấp thụ trong diethyl ether của đồng phaeophtin a và đồng phaeophytin b, tương ứng). |
|||
|
|
Tính nồng độ từng chất (mmol/L) theo các phương trình sau: Đồng phaeophytin a = 45,6 A (649,8 nm) – 2,75 A (628,2 nm) + 3,10 A (667,2 nm) – 35,4 A (654,4 nm) Đồng phaeophytin b = -8,46 A (649,8 nm) + 20,7 A (628,2 nm) – 1,69 A (667,2 nm) + 5,13 A (654,4 nm)
|
|||
PHỤ LỤC 17
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI MUỐI NATRI, KALI CỦA CLOROPHYL PHỨC ĐỒNG
1. Tên khác, chỉ số |
Natri đồng clorophyllin; kali đồng clorophyllin Chlorophyllins, C.I. (1975) No. 75810; INS 141ii ADI = 0 -15 mg/kg thể trọng. |
2. Định nghĩa |
Muối kiềm của đồng Clorophyllin thu được khi thêm đồng vào sản phẩm thu được khi xà phòng hóa dịch chiết dung môi từ cỏ, cỏ linh lăng, tầm ma và các nguyên liệu thực vật khác; quá trình xà phòng hóa có thể loại các nhóm ester methyl và cyclophytol và có thể tách đôi một phần vòng pentenyl; sau khi thêm đồng vào clorophyllin đã tinh chế, nhóm acid bị trung tính hóa tạo thành dạng muối của kali và/hoặc natri; sản phẩm thương mại có thể ở dạng dung dịch nước hoặc bột khô. Chỉ được sử dụng những dung môi sau để chiết: aceton, dicloromethan, methanol, ethanol, propan-2-ol và hexan. |
Tên hóa học |
Chất màu chính ở dạng acid của nó là 3-(10-Carboxylato-4-ethyl-1,3,5,8-tetramethyl-9-oxo-2-vinylphorbin-7-yl) propionat, phức đồng (Đồng clorophyllin a) 3-(10-carboxylato-4-ethyl-3-formyl-1,5,8-trimethyl-9-oxo-2-vinylphorbin-7-yl) propionat, phức đồng (Đồng clorophyllin b) Tùy thuộc vào mức độ thủy phân vòng cyclopentenyl có thể tách đôi với sản phẩm thu được với chức carboxyl thứ ba. |
Công thức hóa học |
Đồng clorophyllin a (dạng acid): C34H32CuN4O5 Đồng clorophyllin b (dạng acid): C34H30CuN4O6 |
Công thức cấu tạo |
Trong đó: X = CH3 đối với hợp chất “a” X = CHO đối với hợp chất “b” M = Kali và/hoặc natri |
Khối lượng phân tử |
Đồng clorophyllin a: 640,20 Đồng clorophyllin b: 654,18 Mỗi chất có thể tăng tới 18 Dalton nếu vòng cyclopentenyl tách đôi. |
3. Cảm quan |
Dung dịch màu lá cây sẫm hoặc bột xanh lá cây sẫm tới xanh lam/đen. |
4. Chức năng |
Phẩm màu. |
5. Yêu cầu kỹ thuật |
|
5.1. Định tính |
|
Độ tan |
Tan trong nước; rất khó tan trong cồn thấp độ, keton và diethyl ether; không tan trong cloroalkan, hydrocarbon và một số dầu không bay hơi. |
Quang phổ |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
Đồng |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
Natri |
Phải có phản ứng đặc trưng của natri. |
Kali |
Phải có phản ứng đặc trưng của kali. |
5.2. Độ tinh khiết |
|
Phẩm màu kiềm |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
Dung môi tồn dư |
Aceton, methanol, ethanol, propan-2-ol, hexan: Không được quá 50 mg/kg, đơn chất hoặc kết hợp. Dicloromethan: Không được quá 10 mg/kg |
Đồng tự do có thể ion hóa |
Không được quá 200 mg/kg. |
Đồng tổng số |
Không được quá 8% tính theo đồng phaeophytin tổng số. |
Arsen |
Không được quá 3 mg/kg. |
Chì |
Không được quá 5 mg/kg. |
5.3. Hàm lượng |
Không thấp hơn 95% đồng Clorophyllin tổng số sau khi sấy khô tại 100 ºC trong 1 giờ. |
6. Phương pháp thử |
|
6.1 Định tính |
|
Quang phổ |
A (1%, 1 cm) của mẫu thử (đã sấy khô ở 100 ºC trong 1 giờ), đo tại 405 nm trong dung dịch đệm phosphat pH 7,5 không được nhỏ hơn 540. |
Đồng |
Hòa tan tro sulfat của mẫu thử (Cân 1 g mẫu, Phương pháp I) trong 10 ml acid hydrocloric loãng (TS) bằng cách làm nóng trong bể cách thủy. Lọc nếu dung dịch đục, và pha loãng với nước tới 10 ml. Sử dụng dung dịch này là dung dịch thử cho các phép thử sau: Cho dung dịch amoniac (TS) vào 5 ml dung dịch thử để kiềm hóa. Dung dịch phải xuất hiện màu xanh lam. Cho 0,5 ml dung dịch natri diethyldithiocarbamat 1/1000 vào 5 ml dung dịch thử. Dung dịch phải xuất hiện tủa nâu. |
Natri |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Chuẩn bị dung dịch được mô tả trong chuyên luận Định tính đồng. |
Kali |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Chuẩn bị dung dịch được mô tả trong chuyên luận định tính đồng. |
6.2 Độ tinh khiết |
|
Phẩm màu kiềm |
Lấy 5 ml dung dịch mẫu thử 0,5% trong nước vào ống nghiệm, thêm 1 ml acid hydrocloric 1 N và 5 ml diethyl ether. Lắc kỹ và để phân lớp. Màu của lớp ether không được đậm hơn màu xanh lá cây nhạt. |
Dung môi tồn dư |
Xác định bằnh Sắc ký khí hoặc bằng phương pháp cất cuốn (chuyên luận Xác định dung môi tồn dư) hoặc phân tích không gian hơi (chuyên luận Thử giới hạn dung môi tồn dư). (Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4) |
Đồng tự do có thể ion hóa |
Cân khoảng 1 g (chính xác đến mg) mẫu thử và hòa tan trong 20 ml dầu lạc, đun nóng nhẹ. Thêm chính xác 200 ml nước, khuấy bằng máy khuấy từ, và điều chỉnh tới pH 3,0 bằng cách thêm cẩn thận acid hydrocloric 0,5 N (tránh thêm quá nhanh). Để yên hỗn hợp trong 10 phút. Nếu cần, điều chỉnh lại tới pH 3,0 bằng cách thêm cẩn thận acid hydrocloric 0,5 N. Chuyển sang phễu tách và để yên 20 phút. Lọc lớp nước qua giấy lọc Whatman No. 50, bỏ 10 ml dịch lọc đầu. Dùng dung dịch này để phân tích đồng bằng quang phổ hấp thụ nguyên tử (xem JECFA monograph 1-Vol. 4). |
Đồng tổng số |
Cân khoảng 0,1 g (chính xác đến mg) mẫu thử, cho vào đĩa silica, nung ở nhiệt độ không quá 500 ºC, tới khi loại đi toàn bộ than; làm ẩm tro bằng một hoặc hai giọt acid sulfuric đặc và tro hóa lại. Hòa tan tro bằng cách đun sôi 3 lần, mỗi lần với 5 ml acid hydrocloric 10% (kl/kl), lọc dịch acid thu được sau mỗi lần thêm acid qua cùng một phễu giấy lọc nhỏ vào bình định mức 100 ml. Để nguội, và thêm nước tinh khiết tới vạch. Dùng dung dịch này để phân tích đồng bằng quang phổ hấp thụ nguyên tử (xem JECFA monograph 1-Vol. 4). |
Arsen |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4- Phương pháp II |
Chì |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
6.3. Định lượng |
|
|
|
Cân khoảng 1 g (chính xác đến mg) mẫu thử, đã sấy khô trước ở 100 ºC trong 1 giờ, sau đó hòa tan trong 20 ml dung dịch đệm phosphat (pH 7,5) và pha loãng tới 1000 ml bằng nước cất. Lấy 10 ml dung dịch này và pha loãng tới 100 ml bằng dung dịch đệm phosphat (pH 7,5). Đo mật độ quang của dung dịch này (0,001% kl/tt) bằng máy quang phổ thích hợp, sử dụng cuvet đo 1 cm và độ rộng khe 0,10 mm ở 403-406 nm, ghi cực đại trong khoảng đó. Hàm lượng (%) natri đồng clorophyllin được tính theo công thức theo công thức sau: Mật độ quang ´ 104 ————————————– 565 ´ khối lượng mẫu thử (g) Quy ước: natri đồng clorophyllin tinh khiết 100% có độ hấp thụ riêng là 565. |
PHỤ LỤC 18
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI GREEN S
|
1. Tên khác, chỉ số |
CI food green 4, food green S; CI (1975): 44090 INS: 142 ADI “không xác định”. |
|
2. Định nghĩa |
Chủ yếu gồm natri N-[4-][[4-(dimethylamino) phenyl] (2-hydroxy-3,6 disulfo-1-naphtalenyl) methylen]-2,5-cyclohexadien-1-ylidenen-N-methylmetanamini và các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Natri N-[4-[[4-(dimethylamino) phenyl](2-hydroxy-3,6 disulfo-1- naphtalenyl) methylen]-2,5-cyclohexadien-1-yliden]-N methylmetanamini; hoặc Natri 5-[4-dimethylamino-l-(4-dimethyliminiocyclohexa-2,5-dienyliden) benzyl]-6-hydroxy-7-sulfonat-naphtalen-2-sulfonat. |
|
Mã số C.A.S. |
860-22-0 |
|
Công thức hóa học |
C27H25N2NaO7S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
576,63 |
|
3. Cảm quan |
Dạng bột hoặc hạt màu xanh lục đậm. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, khó tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 20% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Crom |
Không được quá 50 mg/kg. |
|
Các chất màu phụ |
Không được quá 1%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,1% rượu 4, 4’-bis (dimethylamino) benzhydric. Không được quá 0,1% 4, 4’-bis (dimethylamino) benzophenon, Không được quá 0,2% acid 3-Hydroxynaphtalen-2,7-disulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Leuco base |
Không được quá 5,0%. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 80% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng điều kiện như sau: Dung môi khai triển là dung môi số 2, chiều cao từ vạch xuất phát tới tuyến dung môi khoảng 17 cm. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký lỏng với điều kiện như sau: HPLC rửa giải gradient 2% đến 100% với tốc độ tăng cố định 2%/phút. |
|
Leuco base |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Cân chính xác 110 ± 5 mg mẫu và tiến hành theo hướng dẫn trong chuyên luận thử Leuco base trong chất màu Triarylmethan sulfon hóa. Độ hấp thụ riêng (a)=0,1725 mgL-1cm-1 tại bước sóng khoảng 634 nm. Tỷ số = 0,9600. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 1,4 – 1,5 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 28,83 mg các chất màu (D). |
PHỤ LỤC 19
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CARAMEN
|
1. Tên khác, chỉ số |
Chất màu caramel được chia thành bốn loại. Tên khác và chỉ số của mỗi loại như sau: Loại I: Caramel thường, caramel caustic; INS No. 150a Loại III: Caramel amoni; INS No. 150c Loại IV: Caramel amoni sulfit, INS No. 150d ADI đối với nhóm I “Không xác định”; ADI đối với nhóm III = 0-160 mg/kg thể trọng ADI đối với loại IV 0-200 mg/kg thể trọng (0-150 mg/kg thể trọng đối với dạng rắn) |
||||||
|
2. Định nghĩa |
Là các hỗn hợp phức tạp, trong đó một số ở dạng tổ hợp keo, sản xuất bằng cách đun nóng riêng carbohydrat hoặc cùng với sự có mặt của acid, kiềm hoặc muối loại thực phẩm; tùy theo hóa chất dùng khi sản xuất phân loại như sau: Loại I: sản xuất bằng cách đun nóng riêng carbohydrat hoặc cùng với sự có mặt của acid, kiềm; không dùng hợp chất amoni hoặc sulfit. Loại III: sản xuất bằng cách đun nóng riêng carbohydrat hoặc cùng với sự có mặt của acid, kiềm; cùng với hợp chất amoni; không dùng hợp chất sulfit. Loại IV: sản xuất bằng cách đun nóng riêng carbohydrat hoặc cùng với sự có mặt của acid, kiềm; cùng với cả hợp chất sulfit và hợp chất amoni. Trong tất cả các trường hợp, nguyên liệu carbohydrat có sẵn ở dạng thương phẩm là các chất làm ngọt dinh dưỡng loại thực phẩm có chứa glucose, fructose và/hoặc polyme của chúng. Các acid và kiềm là acid sulfuric hoặc citric thực phẩm và natri, kali hoặc calci hydroxyd hoặc hỗn hợp của chúng loại thực phẩm. Hợp chất amoni được dùng là một hoặc bất kì một chất nào sau đây: amoni hydroxyd, amoni carbonat và amoni hydro carbonat, amoni phosphat, amoni sulfat, amoni sulfit và amoni hydrosulfit. Dùng hợp chất sulfit là một hoặc bất kì một chất nào sau đây: acid sulfurơ, kali, natri và amoni sulfit và amoni hydro sulfit. Có thể dùng tác nhân chống nổi bọt loại thực phẩm để trợ giúp quá trình sản xuất. |
||||||
|
3. Cảm quan |
Chất ở dạng rắn hoặc lỏng, màu nâu sẫm tới đen có mùi đường cháy. |
||||||
|
4. Chức năng |
Phẩm màu |
||||||
|
5. Yêu cầu kỹ thuật |
|||||||
|
5.1. Định tính |
|
||||||
|
Độ tan |
Có thể trộn lẫn với nước |
||||||
|
Định tính tạp màu |
Phải có phản ứng đặc trưng của tạp màu. |
||||||
|
Phân loại |
Loại I: Không được quá 50 % chất màu là loại liên kết bởi celulose DEAE và không quá 50% chất màu là loại liên kết bởi celulose phosphoryl. Loại III: Không được quá 50% chất màu là loại liên kết bởi celulose DEAE và hơn 50% chất màu là loại liên kết bởi celulose phosphoryl. Loại IV: Hơn 50% chất màu là loại liên kết bởi celulose DEAE và tỉ số độ hấp thụ không quá 50. Xem mô tả trong phần PHƯƠNG PHÁP THỬ. |
||||||
|
5.2. Độ tinh khiết |
Chú ý: Giới hạn arsen và chì áp dụng cho tất cả các nhóm caramel và được tính dựa trên chế phẩm nguyên dạng: Các giới hạn và khoảng khác áp dụng đối với mỗi loại riêng theo chỉ dẫn, nếu không có chỉ dẫn riêng, được tính dựa trên chế phẩm rắn. |
||||||
|
Hàm lượng chất rắn |
Loại I: 62-77% Loại III: 53-83% Loại IV: 40-75% |
||||||
|
Cường độ màu |
Loại I: 0,01-0,12 Loại III: 0,08-0,36 Loại IV: 0,10-0,60 |
||||||
|
Nitơ toàn phần |
Loại I: Không được quá 0,1% Loại III: 1,3 -6,8% Loại IV: 0,5-7,5% |
||||||
|
Lưu huỳnh toàn phần |
Loại I: Không được quá 0,3% Loại III: Không được quá 0,3% Loại IV: 1,4-10,0% |
||||||
|
Lưu huỳnh dioxyd |
Loại I: – Loại III: – Loại IV: Không được quá 0,5% |
||||||
|
Nitơ amoniac |
Loại I: – Loại III: Không được quá 0,4% Loại IV: Không được quá 2,8% |
||||||
|
4-Methylimidazol (MEI)
|
Loại I: – Loại III: Không được quá 300 mg/kg & không được quá 200 mg/kg tính theo chất màu tương đương Loại IV: Không được quá 1000 mg/kg & không được quá 250 mg/kg tính theo chất màu tương đương |
||||||
|
2-Acetyl-4-tetrahydroxy- butylimidazol (THI)
|
Loại I: – Loại III: Không được quá 40 mg/kg & không được quá 25 mg/kg tính theo chất màu tương đương. Loại IV: – |
||||||
|
Arsen |
Không được quá 1 mg/kg |
||||||
|
Chì |
Không được quá 2 mg/kg |
||||||
|
6. Phương pháp thử |
|
||||||
|
6.1. Định tính |
|
||||||
|
Phân loại/ Chất màu liên kết bởi celulose DEAE |
Trong chỉ tiêu này chất màu liên kết bởi celulose DEAE được định nghĩa là phần trăm độ hấp thụ giảm đi của dung dịch chất màu caramel ở 560 nm sau khi xử lí với celulose DEAE. Thuốc thử riêng : Celulose DEAE (diethylaminoethyl) có dung lượng 0,7 mE/g, như Cellex D của Bio-Rad hoặc Celulose DEAE có dung lượng cao hơn hoặc thấp hơn tương ứng với lượng chất cao hơn hoặc thấp hơn. Tiến hành: Pha dung dịch chất màu caramel có độ hấp thụ xấp xỉ 0,5 tại 560 nm bằng cách cho một lượng chất màu caramel thích hợp vào bình định mức 100 ml, cùng với acid hydrocloric 0,025 N. Pha loãng tới vạch bằng acid hydrocloric 0,025 N và ly tâm hoặc lọc, nếu dung dịch vẩn đục. Lấy 20 ml dung dịch chất màu caramel, thêm 200 mg celulose DEAE, trộn kỹ trong ít phút, ly tâm hoặc lọc, và thu lấy lớp dung dịch trong phía trên. Xác định độ hấp thụ của dung dịch chất màu caramel và lớp dung dịch phía trên trong cóng đo 1 cm ở 560 nm, bằng máy quang phổ thích hợp, ngay trước đó đã chuẩn hóa với mẫu trắng là acid hydrocloric 0,025 N. Tính phần trăm chất màu liên kết bởi celulose DEAE theo công thức:
Trong đó: A1 là độ hấp thụ của dung dịch chất màu caramel ở 560 nm A2 là độ hấp thụ của lớp dung dịch phía trên sau khi xử lí với Celulose DEAE ở 560 nm. |
||||||
|
Phân loại/ Chất màu liên kết bởi celulose phosphoryl
|
Trong chỉ tiêu này chất màu liên kết bởi celulose phosphoryl được định nghĩa là phần trăm độ hấp thụ giảm đi của dung dịch chất màu caramel ở 560 nm sau khi xử lí với celulose phosphoryl. Thuốc thử riêng: Celulose phosphoryl dung lượng 0,85 mE/g, như Cellex P ở Bio-Rad hoặc Celulose phosphoryl dung lượng cao hơn hoặc thấp hơn tương ứng với lượng chất cao hơn hoặc thấp hơn. Tiến hành: Cho khoảng 200-300 mg chất màu caramel vào bình định mức 100 ml, pha loãng tới vạch bằng acid hydrocloric 0,025 N và ly tâm hoặc lọc, nếu dung dịch vẩn đục. Lấy 40 ml dung dịch chất màu caramel, thêm 2,0 g celulose phosphoryl, lắc kỹ trong ít phút. Ly tâm hoặc lọc, và thu lấy lớp dung dịch trong phía trên. Xác định độ hấp thụ của dung dịch chất màu caramel và lớp dung dịch phía trên trong cóng đo 1 cm ở 560 nm, bằng máy quang phổ thích hợp, ngay trước đó đã chuẩn hóa với mẫu trắng là acid hydrocloric 0,025 N. Tính phần trăm chất màu liên kết bởi celulose phosphoryl theo công thức:
Trong đó: A1 là độ hấp thụ của dung dịch chất màu caramel ở 560 nm A2 là độ hấp thụ của lớp dung dịch phía trên sau khi xử lí với Celulose phosphoryl ở 560 nm. |
||||||
|
Phân loại/ Hệ số độ hấp thụ
|
Trong chỉ tiêu này tỉ số độ hấp thụ được định nghĩa là độ hấp thụ của chất màu caramel ở 280 nm chia cho độ hấp thụ của chất màu caramel ở 560 nm. Tiến hành: Cho khoảng 100 mg chất màu caramel vào bình định mức 100 ml cùng với nước, pha loãng tới vạch bằng nước, lắc đều và ly tâm, nếu dung dịch vẩn đục. Lấy 5,0 ml dung dịch trong này cho vào bình định mức 100 ml, pha loãng tới vạch bằng nước, và lắc đều. Xác định độ hấp thụ của dung dịch 0,1% trong cóng đo 1 cm ở 560 nm và của dung dịch pha loãng 1:20 ở 280 nm, bằng máy quang phổ thích hợp, ngay trước đó đã chuẩn hóa với mẫu trắng là nước. (Máy quang phổ thích hợp là máy có bộ đơn sắc hóa cho độ rộng dải 2 nm hoặc nhỏ hơn và tỷ lệ ánh sáng lạc là 0,5% hoặc nhỏ hơn.) Tính tỉ số độ hấp thụ của chất màu caramel bằng cách chia giá trị độ hấp thụ của chất màu caramel ở 280 nm nhân 20 (hệ số pha loãng) cho giá trị độ hấp thụ ở 560 nm. |
||||||
|
6.2. Độ tinh khiết |
|
||||||
|
Hàm lượng chất rắn |
Hàm lượng chất rắn của chất màu Caramel được xác định bằng cách làm khô mẫu thử với chất mang gồm có cát thạch anh tinh khiết qua được rây số 40 nhưng không qua được cỡ rây số 60 đã được chuẩn bị bằng cách rửa với acid hydrocloric, rửa hết acid, sấy và nung. Trộn 30,0 g cát đã chuẩn bị được cân chính xác với 1,5-2,0 g chất màu caramel được cân chính xác và làm khô tới khối lượng không đổi ở 60oC dưới áp suất giảm 50 mmHg (6,7 kPa). Ghi khối lượng cuối cùng của caramel và cát. Tính % chất rắn theo công thức sau: % chất rắn = Trong đó: m3 = khối lượng cuối cùng của caramel thêm cát (g) m2 = khối lượng cát (g) m1 = khối lượng caramel thêm vào ban đầu (g) Tính toán trên cơ sở chất rắn Hàm lượng nitơ toàn phần, lưu huỳnh toàn phần, nitơ amoni, lưu huỳnh dioxyd, 4-MEI và THI được biểu thị theo chất rắn. Xác định nồng độ (Ci) của mỗi tạp chất theo nguyên trạng; nồng độ (CS) theo chất rắn được tính theo công thức:
|
||||||
|
Cường độ màu |
Trong chỉ tiêu này cường độ màu được định nghĩa là độ hấp thụ của dung dịch 0,1% (kl/tt) của chất màu caramel rắn trong nước ở 610 nm trong cóng đo 1 cm. Tiến hành: Cho khoảng 100 mg chất màu caramel vào bình định mức 100 ml cùng nước, pha loãng tới vạch bằng nước, lắc đều và ly tâm, nếu dung dịch vẩn đục. Xác định độ hấp thụ (A610) của dung dịch trong này trong cóng đo 1 cm ở 610 nm bằng máy quang phổ thích hợp, ngay trước đó đã chuẩn hóa với mẫu trắng là nước. Tính cường độ màu của chất màu caramel theo công thức sau:
Xác định % chất rắn như mô tả ở phần Hàm lượng chất rắn. Tính toán trên cơ sở chất màu tương đương: Khi có thêm các giới hạn đối với 4-MEI và THI được biểu thị theo chất màu tương đương thì các nồng độ trước hết được tính trên cơ sở chất rắn như chỉ dẫn trong phần “Tính trên cơ sở vào chất rắn”, và sau đó biểu thị theo chất màu tương đương theo công thức:
Trong đó: CS = nồng độ trên chất rắn. Như vậy hàm lượng được biểu thị bằng một sản phẩm có cường độ màu là 0,1 đơn vị độ hấp thụ. |
||||||
|
Nitơ toàn phần |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4- Xác định theo chỉ dẫn trong phần Xác định Nitơ (Phương pháp Kjeldahl) sử dụng Phương pháp II |
||||||
|
Lưu huỳnh toàn phần
|
Lấy một chén lớn nhất có thể cho vừa lò nung điện, cho vào đó 1-3 g MgO hoặc một lượng tương đương Mg(NO3)2·6H2O (6,4 – 19,2 g), 1 g đường saccarose đã làm thành bột, và 50 ml HNO3. Thêm 5-10 g chất màu caramel. Cho cùng một lượng thuốc thử vào một chén khác để làm mẫu trắng. Cô trên hơi nước sôi tới khi thành khối nhão. Đặt chén vào lò nung nguội (25 ºC) và đun nóng từ từ tới khi toàn bộ khói NO2 bay hết. Để nguội, hòa tan và trung tính hóa bằng HCl (1+2,5), thêm dư 5 ml. Lọc, đun nóng tới sôi, và thêm 5 ml dung dịch BaCl2·2H2O 10% từng giọt một. Cô tới 100 ml, để yên qua đêm, lọc, rửa, nung, và cân BaSO4. Hiệu chỉnh kết quả đối với BaSO4 thu được trong mẫu trắng và ghi ở dạng mg S/100 g. Các dụng cụ thương mại dùng để phân tích lưu huỳnh toàn phần như thiết bị phân tích theo qui trình đốt cháy Leco/chuẩn độ cũng có thể sử dụng và được khuyên dùng với lượng mẫu thử khoảng 200 mg. |
||||||
|
Lưu huỳnh dioxyd
|
Thiết bị Sử dụng thiết bị Monier-Williams cải tiến (có ở 5GA Scientific, Inc., Bloomfield, N.J., Mỹ) để xác định acid sulfurơ, hoặc dụng cụ thiết kế như trình bày ở hình. Bộ dụng cụ gồm một bình cất đáy tròn ba cổ 1000 ml có ống nối thủy tinh vuốt thon chuẩn 24/40. Gắn kèm một sinh hàn Allihn 30 cm hồi lưu ở một cổ phía ngoài của bình, và đầu kia của sinh hàn nối với một ống Tygon hoặc silicon ¼ inch (được đun sôi trước với dung dịch acid hydrocloric 1/20 và rửa bằng nước) tới bộ ống hấp thụ (có nối hình cầu 35/20 hoặc tương đương). Nối cổ giữa của bình với bình gạn hình trụ 125 ml, và gắn một đoạn ống tới ống chữ U ngắn cắm qua một nắp cao su trên cổ của bình gạn. Gắn một ống vào bằng thủy tinh, cong dài, tới gần đáy bình, vào cổ ngoài khác của bình, và nối ống vào một bình rửa-khí 250 ml một đoạn ống. Bình rửa khí lại nối bằng một ống tới chai (bom khí) nitơ.
Nghiền 4,5 g pyrogalol (acid pyrogalic) với 5 ml nước trong một cối nhỏ, và cho khối nhão sang bình rửa khí. Tiếp tục nghiền phần còn lại, và chuyển toàn bộ sang bình với 2 lần 5 ml nước. Cho khí nitơ đi từ chai khí tới bình để đuổi hết không khí, và sau đó thêm vào bình qua phễu cuống dài dung dịch được làm nguội của 65 g kali hydroxyd trong khoảng 85 ml nước. Lắp đầu bình vào, và sục bong bóng nitơ qua đó để đuổi hết không khí khỏi không gian phía trên. Kẹp chặt ống ở cả hai vị trí của chai, và nối nó tới ống đầu vào của bình cất. Bình rửa khí phải được chuẩn bị như mô tả, với dung dịch pyrogalol mới pha trong ngày làm. Thêm lần lượt vào mỗi ống hấp thụ hình chữ U như sau: hai đũa thủy tinh 8 mm chiều dài khoảng 25 mm, 10 ml hạt thủy tinh 3 mm ở đầu ra, 10,0 ml dung dịch hydrogen peroxyd 3%, và 1 giọt đỏ methyl (TS). Lắp tất cả các phần của thiết bị, và kiểm tra xem có kín không bằng cách thổi nhẹ vào trong ống gắn với cổ bình gạn. Khi thổi, đóng khóa bình gạn. Để yên vài phút; nếu mức chất lỏng trong ống chữ U vẫn ngang bằng, đóng tất cả các khớp nối và thử lại. Nếu hệ thống khít thì tiến hành theo chỉ dẫn dưới đây. Tiến hành: Phân tán khoảng 25 g mẫu thử, cân chính xác, trong 300 ml nước vừa đun sôi để nguội, và chuyển khối nhão sang bình qua một phễu lỗ rộng dùng nước. Pha loãng tới khoảng 400 ml bằng nước, và khóa bình gạn lại. Thêm 90 ml acid hydrocloric 4 N vào bình gạn, và cho acid vào bình bằng cách thổi nhẹ vào ống ở cổ bình gạn. Khóa bình gạn. Mở kẹp ống ở cả hai vị trí của bình rửa khí, và bắt đầu thổi khí nitơ với tốc độ đều đặn bọt khí. Đun nóng bình cất bằng bếp áo để đun hồi lưu trong khoảng 20 phút. Khi đạt được sự hồi lưu ổn định, cấp điện đun tiếp hồi lưu trong 1,75 giờ. Tắt nước trong sinh hàn, và tiếp tục đun tới khi khớp nối phía đầu vào của ống chữ U thứ nhất xuất hiện hơi ngưng đọng và hơi ấm. Bỏ bình gạn và tắt bếp. Khi khớp nối đầu trên của sinh hàn nguội, tháo khớp nối và tráng vào ống chữ U thứ hai, để lại ống nối với khớp ra của ống chữ U thứ nhất nhưng ngắt khỏi đầu vào của ống chữ U thứ hai. Quay ống nối tới khi đầu hở của nó gần chạm đầu vào của ống chữ U thứ nhất. Thêm 1 giọt đỏ methyl vào ống chữ U thứ nhất, và chuẩn độ bằng natri hydroxyd 0,1 N tới khi có màu vàng sáng, lắc nhẹ. Sau khi chuẩn độ ống chữ U thứ nhất, tháo ống nối, lắp nó với ống chữ U thứ hai ở đầu ra, và chuẩn độ tương tự. Ghi tổng lượng dung dịch hai lần chuẩn độ là Vt (ml). Tiến hành làm một mẫu trắng, thể tích dung dịch natri hydroxyd 0,1 N là Vo. Tính phần trăm lưu huỳnh dioxyd trong mẫu thử theo công thức:
Trong đó m là khối lượng của mẫu thử (g) |
||||||
|
Nitơ amoniac
|
Cho 25 ml acid sulfuric 0,1 N vào bình hứng 500 ml, và lắp với thiết bị cất gồm ống nối bầu Kjeldahl và một sinh hàn có đầu ra ngập phía dưới bề mặt dung dịch trong bình hứng. Cho khoảng 2 g chất màu caramel, cân chính xác, vào trong bình Kjeldahl cổ dài 800 ml, và thêm vào bình 2 g magnesi oxyd (không có carbonat), 200 ml nước, và vài viên đá bọt. Lắc bình để trộn đều hỗn hợp trong bình, và lắp nhanh bình với thiết bị cất. Đun nóng bình tới sôi, thu lấy khoảng 100 ml dịch cất vào bình hứng. Rửa đầu ra của ống sinh hàn với vài ml nước, cho dịch rửa vào bình hứng, sau đó thêm 4 hoặc 5 giọt chỉ thị đỏ methyl (500 mg đỏ methyl trong 100 ml alcol), và chuẩn độ bằng natri hydroxyd 0,1 N, ghi thể tích là Vt (ml). Tiến hành làm một mẫu trắng, thể tích dung dịch natri hydroxyd 0,1 N để trung tính là Vo. Tính phần trăm nitơ amoniac trong mẫu thử theo công thức: Nitơ amoniac Trong đó m là khối lượng của mẫu thử (g) |
||||||
|
4-Methylimidazol
|
Ghi chú: Cần thông tin về một phương pháp tốt hơn. Dùng các nguyên vật liệu và thuốc thử sau (thuốc thử phải là loại ACS hoặc tương đương). Nguyên vật liệu: Bông thủy tinh loại Pyrex, cột sắc ký 22 ´ 300 mm và khoá PTFE (như Kimax 17800); cốc polypropylen 150 ml (như Nalge 1201); bình đáy tròn 250 ml (như Pyrex 4320); phễu rót bột 75 mm; thìa gạt (spatula) 5 cm; máy cất quay chân không, bếp đĩa kín, nồi cách thủy, pipet Pasteur dùng một lần; bình định mức 5 ml. Thuốc thử: Aceton; Celit 545; methylen clorid; natri hydroxyd; và tetrahydrofuran. Tiến hành: Sau khi trộn kỹ mẫu thử chất màu caramel bằng cách lắc hoặc khuấy, cân 10,00 g hỗn hợp vào cốc polypropylen 150 ml. Polypropylen được coi là tốt hơn thủy tinh vì bề mặt kị nước dễ chuyển toàn lượng mẫu thử. Thêm vào đó 5,0 g dung dịch NaOH 3,0 N và lắc kỹ để đảm bảo pH của mẫu thử lớn hơn 12. Thêm 20 g Celit 545 vào cốc trên, và trộn đều tới khi hỗn hợp gần khô lại. Quá trình này khoảng 2 tới 3 phút. Với mẫu thử có hàm lượng nước quá cao, hỗn hợp chất màu caramel-Celit 545 có thể quá ướt. Trong trường hợp này, trộn 5,00 g hỗn hợp chất màu caramel với 2,5 g NaOH 3,0 N và 15 g Celit 545 và tiến hành phân tích. Một nút bông thủy tinh Pyrex được đặt ở phía dưới cột sắc kí 22 ´ 300 mm với khóa PTFE. Hỗn hợp chất màu caramel-Celit 545 được cho vào cột qua phễu 75 mm. Hỗn hợp trong cột được nhồi bằng cách gõ nhẹ cột theo phương thẳng đứng khoảng 10 cm trên một bề mặt có lót. Khi nhồi tốt, hỗn hợp chất màu caramel-Celit 545 phải chiếm xấp xỉ 250 mm phía dưới cột. Cẩn thận khi tiến hành để tránh nhồi lỏng quá hoặc chặt quá. Cột nhồi lỏng quá methylen clorid sẽ rửa giải quá nhanh và không chiết hoàn toàn. Cột nhồi quá chặt dẫn tới dung môi rửa giải khó tiếp cận một số vùng chất nhồi. Điều này cũng dẫn đến việc chiết không hoàn toàn. Mở khóa, dùng cốc rót methylen clorid vào cột. Khi dung môi tới nút bông thủy tinh, đóng khoá và để dung môi tương tác với hỗn hợp trong cột 5 phút. Sau đó mở khóa và để cột được rửa giải tiếp với methylen clorid tới khi thu được 200 ml vào bình đáy tròn 250 ml. Lấy 1,00 ml dung dịch chuẩn nội 2 MEI (50,0 mg 2 MEI/50,0 ml methylen clorid) thêm vào dịch rửa giải đã thu được. 2 MEI được tách tốt khỏi 4 MEI trong điều kiện sắc kí khí lỏng đã dùng và không thấy có trong chất màu caramel. Sau đó, loại dung môi khỏi dịch rửa giải bằng cất quay áp suất giảm ở 45-50 kPa và bình cầu đáy tròn được duy trì ở 35 oC trong nồi cách thủy. Cắn của dịch chiết được chuyển hoàn toàn sang bình định mức 5 ml bằng pipet Pasteur dùng một lần, bằng cách rửa bình cầu nhiều lần mỗi lần với một lượng nhỏ (khoảng 0,75 ml) tetrahydrofuran hoặc aceton. Cả hai dung môi được dùng với kết quả như nhau. Sau khi trộn kĩ hỗn hợp bằng cách lắc ngược bình nhiều lần, được dịch chiết dùng cho phân tích GLC. Dịch chiết sau khi chuẩn bị phải phân tích càng sớm càng tốt, bởi mẫu chỉ ổn định trong vòng 1 ngày sau khi chuẩn bị. Phân tích GLC được tiến hành bằng thiết bị sắc ký khí với detector ngọn lửa hydro. Cột thủy tinh 1 m ´ 6 mm đường kính ngoài ( 4 mm đường kính trong), thêm 7,5% Carbowax 20M + 2% KOH trên 90/100 mesh Anakrom ABS. Các thông số GLC như sau: khí mang nitơ 50 ml/phút; hydro 50 ml/phút; oxy 80 ml/phút; bộ phận tiêm mẫu 200 oC; cột đẳng nhiệt 180 oC; detector 250 oC; thể tích mẫu 5 µL. Tất cả quá trình định lượng tiến hành dùng kĩ thuật chuẩn nội. |
||||||
|
2-Acetyl-4-tetrahydroxy-butylimidazol (THI)
|
Ghi chú: Cần thông tin về một phương pháp tốt hơn. THI được chuyển thành dẫn xuất 2,4-dinitrophenylhydrazon (THI-DNPH) của nó. Dẫn chất này được tách khỏi thuốc thử dư và tạp carbonyl bằng HPLC dùng cột RP-8, xác định bằng đo độ hấp thụ ở bước sóng 385 nm. Tiến hành: Cân chính xác chất màu caramel (200-250 mg), sau đó hòa tan trong nước (3 ml). Chuyển toàn lượng dung dịch sang phần phía trên của cột tổ hợp. Bắt đầu rửa giải bằng nước, và toàn bộ lượng nước qua các cột khoảng 100 ml. Sau đó tháo cột phía trên. Rửa giải cột phía dưới bằng HCl 0,5 N. Bỏ 10,0 ml dịch rửa giải ban đầu, sau đó thu lấy 35 ml. Cô dung dịch này tới khô ở 40 oC và 15 torr. Hòa tan cặn đặc sệt trong methanol không có carbonyl (250 µL) và thuốc thử 2,4-dinitrophenylhydrazin (250 µL). Chuyển hỗn hợp phản ứng sang lọ có nắp là tấm đệm và bảo quản 5 giờ ở nhiệt độ phòng. Tiêm 5 µL (cũng có thể từ 1 tới 25 µL) vào cột HPLC LiChrosorb RP-8 (10 µm). Pha động gồm MeOH/ H3PO4 0,1 M 50/50 (tt/tt). Điều chỉnh thành phần pha động nếu đặc tính của cột thay đổi, tuỳ thuộc nhà sản xuất. (Rất nên sử dụng chất nhồi LiChrosorb RP-8, 10 µm, cột 250 ( 4 mm “Vertex” của nhà sản xuất Knauer, Bad Homburg, F.R.G.). Với tốc độ pha động 2 ml/phút và kích cỡ cột 250 ( 4,6 mm, THI-DNPH rửa giải sau khoảng 6,3±0,1 phút. Phát hiện ở 385 nm và đo chiều cao của pic. Hàm lượng được tính dựa vào đường chuẩn của THI-DNPH trong methanol. Nguyên vật liệu: Thuốc thử – 2,4,-Dinitrophenylhydrazin hydroclorid: 2,4-dinitrophenylhydrazin thương mại (5 g) cho vào acid hydrocloric đặc (10 ml) trong bình nón 100 ml, và lắc nhẹ tới khi base tự do (màu đỏ) chuyển thành hydroclorid (màu vàng). Thêm vào đó ethanol (100 ml), lắc và đun nóng trên cách thủy sôi tới khi tất cả chất rắn hòa tan. Sau khi kết tinh ở nhiệt độ phòng, hydroclorid được lọc, rửa bằng ether, sấy ở nhiệt độ phòng và bảo quản trong bình hút ẩm. Trong khi bảo quản, hydroclorid dần chuyển thành base tự do. Sau đó, có thể loại bằng cách rửa với dimethoxyethan. Thuốc thử được chuẩn bị bằng cách trộn 0,5 g 2,4-dinitrophenylhydrazin hydroclorid trong 15 ml methanol 5% trong dimethoxyethan trong 30 phút. Bảo quản trong tủ lạnh và kiểm tra định kỳ bằng HPLC. – Nhựa trao đổi cation (mạnh): Dowex 50 AG x 8, H+, 100-200 mesh. – Nhựa trao đổi cation (yếu): Amberlite CG AG 50 I, H+, (100-200 mesh). (Để lắng hai hoặc ba lần trước khi sử dụng). – Methanol, không có carbonyl tự do: Methanol được chuẩn bị theo Y. Peleg và C.H. Mannheim, J. Agr. Fd. Chem, 18 (1970) 176, bằng cách xử lý với thuốc thử Girard P. – Dimethoxyethan: Nếu không tinh khiết, dimethoxyethan được tinh chế bằng cách cất từ 2,4-dinitrophenylhydrazin với sự có mặt của acid và cất lại từ natri hydroxyd. Ngay trước khi sử dụng cho qua cột nhôm trung tính để loại peroxyd. Thiết bị: Cột tổ hợp: tương tự như đã mô tả trong J. Agr. Fd. Chem. 22 (1974) 110. Cột phía trên (150 ( 12,5 mm, chiều cao nhồi tối đa 9 cm, hoặc 200 ( 10 mm, chiều cao nhồi tối đa 14 cm, với mao quản đầu ra có 1 mm đường kính trong) nhồi chất trao đổi cation acid yếu, chiều cao chất nhồi lần lượt khoảng 50-60, hoặc 80-90 mm. Cột phía dưới (chiều dài tổng 175 mm, đường kính trong 10 mm, với đầu ra mao quản và khoá Teflon) nhồi với chất trao đổi cation acid mạnh chiều cao chất nhồi 60 mm. Bình đựng dung môi, dùng phễu nhỏ giọt (100 ml) khóa Teflon. Tất cả các phần được nối bằng khớp nối thủy tinh mài chuẩn (14,5 mm). HPLC: với cột qui định ở trên và detector UV có khả năng đo ở 385 nm. Chuẩn hóa: Hòa tan THI-DNPH trong methanol tuyệt đối không có carbonyl (khoảng 100 mg/L; nồng độ của THI: 47,58 ng/µL). Dung dịch này pha loãng 10 lần với methanol (4,7 ng THI/µL). Dung dịch chuẩn THI-DNPH ổn định ít nhất 20 tuần nếu bảo quản trong tủ lạnh.
|
||||||
|
Arsen
|
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Phương pháp II. |
||||||
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
||||||
PHỤ LỤC 20
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI BRILLIANT BLACK PN
|
1. Tên khác, chỉ số |
CI food Black 1, Black PN; CI (1975): 28440 INS: 151 ADI = 0 – 1 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm tetranatri 4-acetamido-5-hydroxy-6-[7-sulfon-4-(4-sulfon-phenylazo)-1-naphthylazo]-1,7-naphthalen-disulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
tetranatri 4-acetamido-5-hydroxy-6-[7-sulfon-4-(4-sulfon-phenylazo)-1-naphthylazo]-1,7-naphthalen-disulfonat. |
|
Mã số C.A.S. |
2519-30-4 |
|
Công thức hóa học |
C28H17N5Na4O14S4 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
867,69 |
|
3. Cảm quan |
Dạng bột hoặc tinh thể màu đen |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 20% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 4%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,8% tổng các acid 4-Acetamido-5-hydroxy-1,7-naphthalendisulfonic; acid 4-Amino-5-hydroxy-1,7-naphthalendisulfonic; acid 8-Amino-2-naphthalensulfonic; acid Sulfanilic và acid 4,4′-Diazoamino-di(benzensulfuric) |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 80% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng các điều kiện sau: Dung môi khai triển: Sắc ký đồ (i): số 1 Sắc ký đồ (ii): số 4 Chiều cao tuyến dung môi: Sắc ký đồ (i): 17 cm Sắc ký đồ (ii): 17 cm.) |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký lỏng, với các điều kiện như sau: HPLC rửa giải gradient từ 2 đến 100%, tốc độ tăng cố định 2%/phút (tuyến tính). |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 0,6 – 0,7 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 10,86 mg các chất màu (D). |
PHỤ LỤC 21
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI BROWN HT
|
1. Tên khác, chỉ số |
CI food Brown 3, Choccolat brown HT; CI (1975): 20285 INS: 155 ADI = 0 – 1,5 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 4,4′- (2,4-dihydroxy-5-hydroxymethyl-1,3-phenylen-bisazo) di-1-naphthalen-sulfonat cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 4,4′- (2,4-dihydroxy-5-hydroxymethyl-1,3-phenylen-bisazo) di-1-naphthalen-sulfonat. |
|
Mã số C.A.S. |
4553-89-3 |
|
Công thức hóa học |
C27H18N4Na2O9S2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
652,57 |
|
3. Cảm quan |
Dạng bột hoặc tinh thể màu nâu. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, không tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135 oC |
Không được quá 30% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2%. |
|
Chì |
Không được quá 2 mg/kg. |
|
Các chất màu phụ |
Không được quá 10%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,7% acid 4-Aminonaphthalen-1-sulfonic. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,2%. |
|
5.3. Hàm lượng |
Không được thấp hơn 70% tổng các chất màu |
|
6. Phương pháp thử |
|
|
6.1 Độ tinh khiết |
|
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng các điều kiện sau: Pha chuẩn theo cách sau: Pha loãng 1,0 ml dung dịch chế phẩm 1% với nước đến đủ 100 ml, lắc đều. Lấy 0,10 ml dung dịch này vào ống nghiệm, thêm 5,0 ml dung dịch nước:aceton (1:1 – tt/tt) và sau đó thêm 14,9 ml dung dịch natri hydrocarbonat 0,05 N, lắc đều. Xác định độ hấp thụ của chuẩn – As. Dung môi khai triển: Số 6. Thời gian khai triển: ~ 14 giờ. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký lỏng, với các điều kiện như sau: HPLC rửa giải gradient từ 2 đến 100%, tốc độ tăng cố định 2%/phút. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng quang phổ (trong JECFA monograph 1-Vol. 4) với các điều kiện như sau: Đệm: Đệm phosphat pH 7; Pha loãng dung dịch A: 10 ml pha loãng đến đủ 250 ml. Độ hấp thụ riêng (a): 40,3 Bước sóng cực đạt hấp thụ: ~ 460 nm. |
PHỤ LỤC 22
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI β-CAROTEN TỔNG HỢP
|
1. Tên khác, chỉ số |
CI food Orange 5; CI (1975): 40800 INS: 160ai ADI = 0 – 5 mg/kg thể trọng. |
|
2. Định nghĩa |
Quy chuẩn này áp dụng với chế phẩm chủ yếu gồm tất cả các đồng phân trans (Z) của b-caroten với lượng nhỏ các carotenoid khác; Các dạng pha loãng và ổn định được chuẩn bị từ b-caroten đáp ứng quy chuẩn này gồm dung dịch hoặc huyền phù của b-caroten trong dầu, mỡ thực phẩm, nhũ tương và bột có thể phân tán trong nước; Các chế phẩm này có thể có tỷ số giữa các đồng phân cis/trans khác nhau; Phương pháp phân tích đối với chất màu gốc không thích hợp để định lượng hoặc xác định độ tinh khiết của các chế phẩm ổn định (các phương pháp này có thể được các nhà sản xuất cung cấp). |
|
Tên hóa học |
b-caroten; b,b-caroten |
|
Mã số C.A.S. |
7235-40-7 |
|
Công thức hóa học |
C40H56 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
536,88 |
|
3. Cảm quan |
Tinh thể hoặc bột tinh thể màu đỏ đến đỏ nâu, nhạy cảm với oxy và ánh sáng do vậy phải bảo quản trong bao bì tránh ánh sáng và môi trường khí trơ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Không tan trong nước, thực tế không tan trong ethanol, ít tan trong dầu thực vật, tan trong cloroform. |
|
Quang phổ |
Xác định độ hấp thụ quang (A) của dung dịch mẫu thử C (xem phần Định lượng) tại các bước sóng 455 nm, 483 nm Tỷ số A455/A483 nằm trong khoảng 1,14 và 1,19. Xác định độ hấp thụ quang (A) của dung dịch mẫu thử C tại bước sóng 455 nm và của dung dịch mẫu thử B 340 nm Tỷ số A455/A340 không được thấp hơn 15. |
|
Carotenoid |
Đạt yêu cầu (mô tả trong phần phương pháp thử) |
|
Phản ứng Carr-Price |
Dung dịch mẫu thử trong cloroform chuyển thành màu xanh lam khi thêm dư dung dịch thuốc thử Carr-Price (TT). |
|
5.2. Độ tinh khiết |
|
|
Tro sulfat |
Không được quá 0,1%. |
|
Các chất màu phụ |
Các carotenoid khác ngoài b-caroten: không được quá 3% tổng các chất màu. |
|
Chì |
Không được quá 2 mg/kg. |
|
5.3. Hàm lượng |
Không được thấp hơn 96% tổng chất màu, thể hiện dưới dạng –β caroten. |
|
6. Phương pháp thử |
|
|
6.1. Định tính |
|
|
Carotenoid |
Màu của dung dịch mẫu thử trong aceton sẽ mất sau khi thêm dung dịch natri nitrit 5% và dung dịch acid sulfuric 1 N, lắc đều. |
|
6.2. Độ tinh khiết |
|
|
Tro sulfat |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Phương pháp I, cân 2 g mẫu thử |
|
Các chất màu phụ |
Các carotenoid khác ngoài b-caroten Cân 80 mg mẫu, hòa tan trong 100 ml cloroform. Chấm 400 mL dung dịch này lên bản mỏng (silicagel 0,25 mm), chấm cách đáy bản mỏng 2 cm. Ngay sau khi chấm tiến hành khai triển sắc ký trong buồng đã bão hòa hệ dung môi gồm 95 phần dicloromethan và 5 phần diethyl ether, tránh ánh sáng, đến khi chiều cao tuyến dung môi cách vết chấm khoảng 15 cm. Lấy bản mỏng ra, để khô dung môi tại nhiệt độ phòng, đánh dấu vết màu chính và các vết màu phụ (các carotenoid khác). Cạo phần silicagel hấp phụ chất màu chính, cho vào một ống ly tâm 100 ml có nút thủy tinh, thêm 40,0 ml cloroform (dung dịch 1). Cạo phần silicagel hấp phụ các carotenoid khác, cho vào một ống ly tâm 50 ml có nút thủy tinh, thêm 20,0 ml cloroform (dung dịch 2). Lắc cả hai ống trong 10 phút và ly tâm trong 5 phút. Lấy 10,0 ml dung dịch 1 pha loãng với cloroform đến đủ 50,0 ml (dung dịch 3). Sử dụng thiết bị đo quang thích hợp, xác định độ hấp thụ quang của dung dịch 2 và dung dịch 3 tại bước sóng 464 nm, sử dụng cloroform làm mẫu trắng và đo trong cuvet 1 cm. Tính kết quả: Tính hàm lượng (%) tổng các carotenoid khác ngoài b-caroten theo công thức sau:
Trong đó: A2 = độ hấp thụ quang của dung dịch 2 A3 = độ hấp thụ quang của dung dịch 3 |
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
6.2. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận định lượng tổng chất màu bằng phương pháp quang phổ trong JECFA monograph 1-Vol. 4, với các điều kiện như sau: W = 0,08 g V1 = V2 = V3 = 100 ml v1 = v2 = 5 ml A1%1cm = 2500 lmax ~ 456 nm. |
PHỤ LỤC 23
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CAROTEN THỰC VẬT
|
1. Tên khác, chỉ số |
b-Caroten tự nhiên; caroten tự nhiên; hỗn hợp các caroten; CI food Orange 5; Số CI (1975): 75130, Số CI (1975): 40800 (đối với b-caroten). INS 160aii ADI “chấp nhận được” có nghĩa là mức sử dụng không vượt quá mức thông thường có trong thực vật. |
|
2. Định nghĩa |
Các caroten (thực vật) thu được bằng cách chiết cà rốt (Daucus carota), dầu cọ (Elaeis guinensis), khoai lang (Ipomoea batatas) và các thực vật ăn được khác với dung môi hữu cơ, sau đó tinh chế. Chất màu chính là a– và b-caroten, trong đó chủ yếu là b-caroten. Ngoài ra còn có lượng nhỏ g– và d-caroten cùng các thành phần màu khác. Bên cạnh các thành phần màu, chế phẩm còn có thể chứa dầu, mỡ, sáp tự nhiên có nguồn gốc từ nguyên liệu. Chỉ những dung môi sau dây được sử dụng để chiết caroten: aceton, methanol, ethanol, propan-2-ol, hexan, carbon dioxyd và dầu thực vật. Chế phẩm thương mại chủ yếu tồn tại dưới dạng dung dịch hoặc huyền phù trong dầu thực vật thực phẩm. Dạng này dễ sử dụng và giúp cải thiện tính bền của caroten dễ bị oxy hóa. |
|
Họ |
Carotenoid |
|
Mã số C.A.S. |
7235-40-7 |
|
Công thức hóa học |
C40H56 (-β caroten) |
|
Công thức cấu tạo |
All-trans-b-caroten |
|
Khối lượng phân tử |
536,88 (b-caroten) |
|
3. Cảm quan |
Dạng rắn hoặc dạng lỏng màu đỏ nâu đến nâu hoặc cam đến cam sẫm. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Không tan trong nước. |
|
Quang phổ |
Dung dịch mẫu thử trong n-hexan (1/200.000) có cực đại hấp thụ tại vùng 440 – 457 nm và 470 – 486 nm. |
|
Phản ứng màu |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
|
5.2. Độ tinh khiết |
|
|
Dung môi tồn dư |
Không được quá 50 mg/kg đơn chất hoặc tổng của aceton, hexan, methanol, ethanol, propan-2-ol. |
|
Chì |
Không được quá 2 mg/kg. |
|
5.3. Hàm lượng |
Hàm lượng caroten (tính theo b-caroten) không được thấp hơn hàm lượng được công bố. |
|
6. Phương pháp thử |
|
|
6.1 Định tính |
|
|
Phản ứng màu |
Chấm lên tấm giấy lọc dung dịch mẫu thử trong toluen (~ 400 mg b-caroten/ml), phun hoặc nhỏ dung dịch antimon triclorid 20% trong toluen lên vết mẫu trên giấy lọc, sau 2 – 3 phút màu của vết chuyển thành xanh lam. |
|
6.2 Độ tinh khiết |
|
|
Chì |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
6.3. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận định lượng tổng chất màu bằng phương pháp quang phổ trong JECFA monograph 1-Vol. 4, với các điều kiện như sau: W = Lượng mẫu thử đủ để đo hấp thụ quang (g) V1 = V2 = V3 = 100 ml v1 = v2 = 5 ml A1%1cm = 2500 lmax = 440 – 457 nm. |
PHỤ LỤC 24
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CAO ANNATTO
|
1. Tên khác, chỉ số |
Annatto F; Orlean; Terre orellana; R. Orange; Số CI (1975): 75120 (Natural Orange 4). INS 160bii ADI = 0 – 12 mg/kg thể trọng đối với Bixin; ADI = 0 – 0,6 mg/kg thể trọng đối với Norbixin và các muối của nó Màu Bixin và Norbixin được chế từ cao Annatto (bixin được chiết bằng dung môi, norbixin được chiết bằng dung môi; bixin xử lý với nước; norbixin xử lý với kiềm, kết tủa acid; và norbixin xử lý với kiềm, không kết tủa acid) đều áp dụng ADI đối với Bixin và Norbixin. |
|
2. Định nghĩa |
Norbixin xử lý với kiềm, kết tủa acid được sản xuất bằng cách loại bỏ vỏ của hạt cây Annatto (Bixa orellana L.) bằng dung dịch kiềm. Bixin bị thủy phân thành norbixin trong dung dịch kiềm nóng, sau đó acid hóa để kết tủa norbixin. Lọc tủa, làm khô và nghiền thu được dạng bột, hạt. Norbixin xử lý kiềm chứa nhiều thành phần màu, các thành phần màu chính (chiếm tỷ lệ lớn) là cis-norbixin, ngoài ra còn có lượng nhỏ trans-norbixin và các sản phẩm phân hủy nhiệt của norbixin là sản phẩm phụ của quá trình chế biến. Chế phẩm thương mại dùng cho công nghiệp thực phẩm thường được bào chế sẵn với các chất mang thích hợp với chất lượng dùng cho thực phẩm. |
|
Tên hóa học |
cis-Norbixin: acid 6,6′-Diapo-Ψ,Ψ-carotendioic Muối dikali cis-Norbixin: Dikali 6,6′-diapo-Ψ,Ψ-carotendioat Muối dinatri cis-Norbixin: Dinatri 6,6′-diapo-Ψ,Ψ-carotendioat |
|
Mã số C.A.S. |
cis-Norbixin: 542-40-5 Muối dikali cis-Norbixin: 33261-80-2 Muối dinatri cis-Norbixin: 33261-81-3 |
|
Công thức hóa học |
C24H28O4; C24H26K2O4; C24H26Na2O4 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
380,5 (acid); 456,7 (muối dikali); 424,5 (muối dinatri) |
|
3. Cảm quan |
Bột màu đỏ nâu sẫm đến đỏ tím. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong dung dịch kiềm, ít tan trong ethanol. |
|
Hấp thụ UV-VIS |
Dung dịch mẫu thử 0,5% trong dung dịch kali hydroxyd có cực đại hấp thụ tại khoảng 453 và 482 nm. |
|
Sắc ký lớp mỏng |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
|
5.2. Độ tinh khiết |
|
|
Arsen |
Không được quá 3 mg/kg. |
|
Chì |
Không được quá 2 mg/kg. |
|
Thủy ngân |
Không được quá 1 mg/kg. |
|
5.3. Hàm lượng |
Tổng các chất màu không thấp hơn 35% (tính theo norbixin) |
|
6. Phương pháp thử |
|
|
6.1 Định tính |
|
|
Sắc ký lớp mỏng |
Hoạt hóa bản mỏng (VD: LK6D SILICA GEL 60 A (chiều dày lớp pha tĩnh: 250 μm, cỡ bản mỏng: 5 x 20 cm)) trong 1 giờ tại 110o. Pha dung dịch mẫu thử 5% trong ethanol (95%) và chấm 10 μL lên bản mỏng. Để khô và khai triển sắc ký trong hệ dung môi gồm n-butanol/ methyl ethyl keton/dung dịch amoniac 10% (3/2/2 – tt/tt/tt) đến khi chiều cao của tuyến dung môi so với vết chấm khoảng 10 cm. Lấy bản mỏng ra và để khô. Vết bixin và norbixin có màu vàng với giá trị Rf tương ứng khoảng 0,50 đến 0,45. Phun dung dịch natri nitrit 5%, tiếp theo phun acid sulfuric 0,5 M vết sẽ mất màu ngay. |
|
6.2 Độ tinh khiết |
|
|
Arsen |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật ICP-AES / AAS-hydrid. Hoặc xác định theo chuyên luận thử giới hạn Arsen – phương pháp II. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4. |
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật AAS ICP-AES thích hợp với mức hàm lượng đã định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4. |
|
Thủy ngân |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật AAS hóa hơi lạnh. Lựa chọn cỡ mẫu thử phù hợp với mức hàm lượng quy định. |
|
6.3. Định lượng |
|
|
|
Tiến hành theo hướng dẫn trong chuyên luận định lượng tổng chất màu bằng phương pháp quang phổ trong JECFA monograph 1-Vol. 4 – quy trình 1, với các điều kiện như sau: Dung môi: dung dịch KOH 0,5% Đo độ hấp thụ quang tại lmax ~ 482 nm. Độ hấp thụ riêng A1%1cm = 2870. |
PHỤ LỤC 25
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI β-APO-CAROTENAL
|
1. Tên khác, chỉ số |
CI food Orange 6; Số CI (1975): 40820 INS 160e ADI = 0 – 5 mg/kg thể trọng. |
|
2. Định nghĩa |
Là chế phẩm chủ yếu gồm đồng phân all trans (Z) của b-apo-8’-carotenal với lượng nhỏ các carotenoid khác; Các dạng pha loãng và ổn định được chuẩn bị từ b-apo-8’-carotenal đáp dứng quy chuẩn này gồm dung dịch hoặc huyền phù của b-apo-8’-carotenal trong dầu, mỡ thực phẩm, nhũ tương và bột phân tán trong nước; Các chế phẩm này có thể có tỷ số giữa các đồng phân cis/trans khác nhau; Phương pháp phân tích đối với chất màu gốc không thích hợp để định lượng hoặc xác định độ tinh khiết của các dạng ổn định chế phẩm (các phương pháp thích hợp sẽ được các nhà sản xuất cung cấp). |
|
Tên hóa học |
b-apo-8’-Carotenal, 8’-apo-b-carotenal |
|
Mã số C.A.S. |
1107-26-2 |
|
Công thức hóa học |
C30H40O |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
416,65 |
|
3. Cảm quan |
Tinh thể hoặc bột tinh thể màu tím đậm có ánh kim, nhạy cảm với oxy và ánh sáng do vậy phải bảo quản trong bao bì tránh ánh sáng và trong môi trường khí trơ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Không tan trong nước, khó tan trong ethanol, ít tan trong dầu thực vật, tan trong cloroform. |
|
Quang phổ |
Xác định độ hấp thụ quang (A) của dung dịch mẫu thử (xem phần Định lượng) tại các bước sóng 461 nm và 488 nm Tỷ số A488/A461 nằm trong khoảng 0,80 và 0,84. |
|
Carotenoid |
Đạt yêu cầu (mô tả trong phần phương pháp thử). |
|
Phản ứng Carr-Price |
Dung dịch mẫu thử trong cloroform chuyển thành màu xanh lam khi thêm dư dung dịch thuốc thử Carr-Price (TT). |
|
5.2. Độ tinh khiết |
|
|
Tro sulfat |
Không được quá 0,1%. |
|
Các chất màu phụ |
Không được quá 3% tổng các chất màu. Xem hướng dẫn trong phần phương pháp thử. |
|
Chì |
Không được quá 2 mg/kg. |
|
5.3. Hàm lượng |
Không được thấp hơn 96% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
5.1. Định tính |
|
|
Carotenoid |
Màu của dung dịch mẫu thử trong aceton sẽ mất sau khi thêm dung dịch natri nitrit 5% và dung dịch acid sulfuric 1 N, lắc đều. |
|
6.2. Độ tinh khiết |
|
|
Tro sulfat |
– Thử theo hướng dẫn tại JECFA monograph 1 – Vol.4 – Phương pháp I, cân 2 g mẫu thử |
|
Các chất màu phụ |
Cân 80 mg mẫu, hòa tan trong 100 ml cloroform. Chấm 400 mL dung dịch này lên bản mỏng cách đáy 2 cm (silicagel 0,25 mm), bản mỏng đã được xử lý trước như sau: nhúng bản mỏng vào bể chứa dung dịch KOH 3% trong methanol sao cho thấm ướt đều, để khô ngoài không khí trong 5 phút và hoạt hóa bằng cách sấy trong tủ sấy tại 110 oC trong 1 giờ, để nguội và giữ trong bình hút ẩm chứa CaCl2. Ngay sau khi chấm tiến hành khai triển sắc ký trong buồng đã bão hòa hệ dung môi gồm n-hexan/cloroform/ethyl acetat (70/20/10), tránh ánh sáng, đến khi chiều cao tuyến dung môi cách vết chấm khoảng 10 cm. Lấy bản mỏng ra, để khô dung môi tại nhiệt độ phòng, đánh dấu vết màu chính và các vết màu phụ (các carotenoid khác). Cạo phần silicagel hấp phụ chất màu chính, cho vào một ống ly tâm 100 ml có nút thủy tinh, thêm 40,0 ml cloroform (dung dịch 1). Cạo phần silicagel hấp phụ các carotenoid khác, cho vào một ống ly tâm 50 ml có nút thủy tinh, thêm 20,0 ml cloroform (dung dịch 2). Lắc cả hai ống trong 10 phút và ly tâm trong 5 phút. Lấy 10,0 ml dung dịch 1 pha loãng với cloroform đến đủ 50,0 ml (dung dịch 3). Sử dụng thiết bị đo quang phổ thích hợp, xác định độ hấp thụ quang của dung dịch 2 và dung dịch 3 tại bước sóng 474 nm, sử dụng cloroform làm mẫu trắng và đo trong cuvet 1 cm. Tính kết quả: Tính hàm lượng (%) tổng các carotenoid khác ngoài b-apo-8’carotenal theo công thức sau:
Trong đó: A2 = độ hấp thụ quang của dung dịch 2 A3 = độ hấp thụ quang của dung dịch 3 |
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
6.3. Định lượng |
|
|
|
Cân khoản 80 mg (chính xác đến mg) mẫu thử. Tiến hành theo hướng dẫn trong chuyên luận định lượng tổng chất màu bằng phương pháp quang phổ trong JECFA monograph 1-Vol. 4, với các điều kiện như sau: Độ hấp thụ riêng (a) = 2640 lmax ~ 461 nm. |
PHỤ LỤC 26
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI ESTER METHYL (HOẶC ETHYL) CỦA ACID β-APO-8’-CAROTENOIC
|
1. Tên khác, chỉ số |
CI food Orange 7; Số CI (1975): 40825 INS 160f ADI = 0 – 5 mg/kg thể trọng. |
|
2. Định nghĩa |
Là chế phẩm chủ yếu gồm đồng phân all trans (Z) của Ethyl ester của acid b-apo-8’-carotenoic với lượng nhỏ các carotenoid khác; Các dạng pha loãng và ổn định được chuẩn bị từ Ethyl ester của acid b-apo-8’-carotenoic đáp ứng quy chuẩn này gồm dung dịch hoặc huyền phù của Ethyl ester của acid b-apo-8’-carotenoic trong dầu, mỡ thực phẩm, nhũ tương và bột có thể phân tán trong nước; Các chế phẩm này có thể có tỷ số giữa các đồng phân cis/trans khác nhau; Phương pháp phân tích đối với chất màu gốc không thích hợp để định lượng hoặc xác định độ tinh khiết của các dạng ổn định của chế phẩm (các phương pháp này sẽ được các nhà sản xuất cung cấp). |
|
Tên hóa học |
Ethyl ester của acid b-apo-8’-carotenoic; Ethyl 8’-apo-b-caroten-8’-oat |
|
Mã số C.A.S. |
1109-11-1 |
|
Công thức hóa học |
C32H44O2 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
460,70 |
|
3. Cảm quan |
Tinh thể hoặc bột tinh thể màu đỏ đến đỏ tím, nhạy cảm với oxy và ánh sáng do vậy phải bảo quản trong bao bì tránh ánh sáng và môi trường khí trơ. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Không tan trong nước, rất khó tan trong ethanol, khó tan trong dầu thực vật, tan trong cloroform. |
|
Quang phổ |
Xác định độ hấp thụ quang (A) của dung dịch mẫu thử (xem phần Định lượng) tại các bước sóng 449 nm, 475 nm Tỷ số A475/A449 nằm trong khoảng 0,82 và 0,86. |
|
Carotenoid |
Đạt yêu cầu (mô tả trong phần phương pháp thử). |
|
Phản ứng Carr-Price |
Dung dịch mẫu thử trong cloroform chuyển thành màu xanh lam khi thêm dư dung dịch thuốc thử Carr-Price (TT). |
|
5.2. Độ tinh khiết |
|
|
Tro sulfat |
Không được quá 0,1%. |
|
Các chất màu phụ |
Không được quá 3% tổng các chất màu. |
|
Chì |
Không được quá 2 mg/kg. |
|
5.3. Hàm lượng |
Không được thấp hơn 96% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
5.1. Định tính |
|
|
Carotenoid |
Màu của dung dịch mẫu thử trong aceton sẽ mất sau khi thêm liên tiếp dung dịch natri nitrit 5% và dung dịch acid sulfuric 1 N, lắc đều. |
|
6.2. Độ tinh khiết |
|
|
Tro sulfat |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Phương pháp I, cân 2 g mẫu thử |
|
Các chất màu phụ |
Các carotenoid khác ngoài Ethyl ester của acid b-apo-8’-carotenoic: Cân 80 mg mẫu, hòa tan trong 100 ml cloroform. Chấm 400 mL dung dịch này lên bản mỏng cách đáy 2 cm (silicagel 0,25 mm), bản mỏng đã được sử lý trước như sau: nhúng bản mỏng vào bể chứa dung dịch KOH 3% trong methanol sao cho thấm ướt đều, để khô ngoài không khí trong 5 phút và hoạt hóa bằng cách sấy trong tủ sấy tại 110 oC trong 1 giờ, để nguội và giữ trong bình hút ẩm chứa CaCl2. Ngay sau khi chấm tiến hành khai triển sắc ký trong buồng đã bão hòa hệ dung môi gồm n-hexan/cloroform/ethyl acetat (70/20/10), tránh ánh sáng, đến khi chiều cao tuyến dung môi cách vết chấm khoảng 10 cm. Lấy bản mỏng ra, để khô dung môi tại nhiệt độ phòng, đánh dấu vết màu chính và các vết màu phụ (các carotenoid khác). Cạo phần silicagel hấp phụ chất màu chính, cho vào một ống ly tâm 100 ml có nút thủy tinh, thêm 40,0 ml cloroform (dung dịch 1). Cạo phần silicagel hấp phụ các carotenoid khác, cho vào một ống ly tâm 50 ml có nút thủy tinh, thêm 20,0 ml cloroform (dung dịch 2). Lắc cả hai ống trong 10 phút và ly tâm trong 5 phút. Lấy 10,0 ml dung dịch 1 pha loãng với cloroform đến đủ 50,0 ml (dung dịch 3). Sử dụng thiết bị đo quang phổ thích hợp, xác định độ hấp thụ quang của dung dịch 2 và dung dịch 3 tại bước sóng 455 nm, sử dụng cloroform làm mẫu trắng và đo trong cuvet 1 cm. Tính kết quả: Tính hàm lượng (%) tổng các carotenoid khác ngoài Ethyl ester của acid b-apo-8’-carotenoic theo công thức sau:
Trong đó: A2 = độ hấp thụ quang của dung dịch 2 A3 = độ hấp thụ quang của dung dịch 3 |
|
Chì |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. – Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
6.2. Định lượng |
|
|
|
Cân khoản 80 mg (chính xác đến mg) mẫu thử. Tiến hành theo hướng dẫn trong chuyên luận định lượng tổng chất màu bằng phương pháp quang phổ trong JECFA monograph 1-Vol. 4, với các điều kiện như sau: Độ hấp thụ riêng (a) = 2550 lmax ~ 449 nm. |
PHỤ LỤC 27
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI CAO VỎ NHO
1. Tên khác, chỉ số |
Enociania, Eno, Grape skin extract. INS 163 (ii) ADI = 0-2,5 mg /kg thể trọng. |
2. Định nghĩa |
Chế phẩm thu được từ dịch chiết nước của vỏ hoặc bã nho sau khi đã ép hết nước quả; chứa các thành phần thông thường của nước ép quả nho như: anthocyanin, acid tartric, tanin, các đường, khoáng chất,…, nhưng tỷ lệ thành phần khác so với trong nước ép quả. Trong quá trình chiết, lưu huỳnh dioxyd được cho vào và hầu hết lượng đường chiết được bị lên men biến thành rượu (alcol); Dịch chiết được cô đặc bằng cách làm bay hơi trong chân không, trên thực tế trong quá trình này toàn bộ lượng alcol đã bị loại đi; một lượng nhỏ lưu huỳnh dioxyd có thể còn dư lại. |
Tên hóa học |
Các chất màu chính là anthocyanin, glucosid của các anthocyanidin (các muối 2-phenylbenzopyrylium) như peonidin, malvidin, delphinidin và petunidin. |
Công thức hóa học |
Peonidin : C16H13O6 X Malvidin : C17H15O7 X Delphinidin : C15H11O7 X Petunidin : C16H13O7 X X : Gốc acid |
Công thức phân tử |
Peonidin : R = OCH3 ; R’= H Malvidin : R, R’= OCH3 Delphinidin : R, R’= OH Petunidin : R = OCH3 ; R’= OH X : Gốc acid |
3. Cảm quan |
Chất lỏng, miếng, bột hoặc bột nhão màu đỏ tía, có mùi đặc trưng nhẹ. |
4. Chức năng |
Phẩm màu |
5. Yêu cầu kỹ thuật |
|
5.1. Định tính |
|
Độ tan |
Tan trong nước |
Quang phổ |
Dịch chiết ở pH 3 cho cực đại hấp thụ tại ~ 525 nm |
Phản ứng màu |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
5.2. Độ tinh khiết |
|
Lưu huỳnh dioxyd |
Không được quá 0,005% với mỗi chỉ số màu. |
Các chất màu kiềm |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
Các chất màu acid khác |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
Chì |
Không được quá 2 mg/kg |
5.3. Hàm lượng |
Cường độ màu không được dưới mức công bố. |
6. Phương pháp thử |
|
6.1 Định tính |
|
Phản ứng màu |
Thêm 0,1 g mẫu vào 50 ml nước và lắc kỹ. Lọc nếu cần, dung dịch có màu đỏ đến đỏ tía và chuyển sang màu da trời hoặc màu xanh lá sẫm khi thêm dung dịch natri hydroxyd (TT). |
6.2. Độ tinh khiết |
|
Lưu huỳnh dioxyd |
Cất 1 g mẫu với 100 ml nước và 25 ml dung dịch acid phosphoric (2 /7) trong một bình cất với ống Wagner (Hình 1). Cho 25 ml dung dịch chì acetat (1/50) đã pha trước vào một bình hấp thụ. Nhúng phần thấp nhất của ống ngưng ngập vào dung dịch chì acetat trong bình hấp thụ. Cất đến khi chất lỏng trong bình hấp thụ được khoảng 100 ml và rửa phần đuôi ống cất bằng một lượng nhỏ nước. Thêm 5 ml dung dịch acid hydrocloric và 1 ml dung dịch hồ tinh bột (TT) vào dịch cất rồi chuẩn độ bằng dung dịch iod 0,01 N. Mỗi ml dung dịch iod 0,01 N tương ứng với 0,3203 mg SO2
Hình 1 : Ống Wagner
|
Các chất màu kiềm |
Cho 1 g mẫu vào 100 ml dung dịch natri hydroxyd (1/100) và lắc đều. Lấy 30 ml dung dịch này và chiết với 15 ml ether. Lắc dịch chiết ether này hai lần mỗi lần với 5 ml dung dịch acid acetic loãng (TT). Dịch chiết acid acetic không được có màu. |
Các chất màu acid khác |
Thêm 1 ml dung dịch amoniac (TT) và 10 ml nước vào 1 g mẫu và theo chỉ dẫn trong phần sắc ký, chấm 0,002 ml dung dịch lên bản sắc ký và làm khô. Dùng dung môi khai triển là hỗn hợp pyridin và amoniac (TT) (2:1, theo thể tích),để dung môi khai triển được 15 cm từ vết chấm. Sau khi làm khô bản mỏng dưới ánh sáng thường, không được xuất hiện vết ở tuyến dung môi. Nếu có bất cứ vết nào thì vết đó phải mất màu ngay khi phun bản mỏng với dung dịch thiếc (II) clorid (SnCl2) trong acid hydrocloric (2/5). |
Chì |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4). Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4: các phươgn pháp thử chung phần các phương pháp phân tích dụng cụ. |
6.3. Định lượng |
|
|
|
Trong điều kiện không có phương pháp định lượng, có thể dùng phương pháp đo cường độ màu như sau: Chuẩn bị khoảng 200 ml dung dịch đệm pH 3 acid citric-Na2HPO4 : trộn 159 thể tích dung dịch acid citric 2,1% và 41 thể tích dung dịch Na2HPO4 0,16% rồi chỉnh pH về 3 bằng dung dịch acid citric hoặc dung dịch Na2HPO4. Cân chính xác một lượng thích hợp mẫu thử sao cho mật độ quang đo được trong khoảng từ 0,2 đến 0,7 và thêm dung dịch đệm pH 3 acid citric-dinatri hydrophosphat đến vừa đủ 100 ml. Đo độ hấp thụ A của dung dịch trong một cuvet đo 1 cm, ở bước sóng cực đại hấp thụ 525 nm, dùng dung dịch đệm pH 3 acid citric-dinatri hydrophosphat làm mẫu trắng. Chỉ số màu = m = Khối lượng mẫu thử (g) |
PHỤ LỤC 28
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI TITAN DIOXYD
1. Tên khác, chỉ số |
Titania, CI pigment white 6, CI (1975) No. 77891 Titanium dioxide INS 171 ADI “không giới hạn”. |
2. Định nghĩa |
Titan dioxyd được sản xuất bằng xử lý sulfat hoặc xử lý clorid. Các điều kiện xử lý xác định dạng của sản phẩm cuối cùng (cấu trúc tinh thể anatase hoặc rutil). Trong quy trình sulfat, acid sulfuric được dùng để phân hủy ilmenit (FeTiO3) hoặc ilmenit và xỉ titan. Sau một loạt các bước tinh chế, titan dioxyd phân lập lần cuối được rửa bằng nước, nung, và nghiền mịn. Trong quy trình clorid, khí clo phản ứng với khoáng chứa titan dưới điều kiện khử tạo thành titan tetra clorid khan, chất này được tinh chế và chuyển thành titan dioxyd bằng oxy hóa có nhiệt trực tiếp hoặc bằng phản ứng với luồng hơi nước trong pha hơi. Có thể cho acid hydrocloric đặc phản ứng với khoáng chứa titan tạo thành dung dịch titan tetraclorid, sau đó tinh chế và chuyển thành titan dioxyd bằng thủy phân. Titan dioxyd được lọc, rửa và nung. Chế phẩm Titan dioxyd thương mại có thể được bao một lượng nhỏ nhôm oxyd và/hoặc silic dioxyd để nâng cao đặc tính kỹ thuật của sản phẩm. |
Mã số C.A.S. |
13463-67-7 |
Công thức hóa học |
TiO2 |
Khối lượng phân tử |
79,88 |
3. Cảm quan |
Bột trắng tới hơi ngà |
4. Chức năng |
Phẩm màu |
5. Yêu cầu kỹ thuật |
|
5.1. Định tính |
|
Độ tan |
Không tan trong nước, acid hydrocloric, acid sulfuric loãng và các dung môi hữu cơ. Hòa tan chậm trong acid hydrofluoric và acid sulfuric đặc nóng. |
Phản ứng màu |
Đạt yêu cầu (mô tả trong phần Phương pháp thử) |
5.2. Độ tinh khiết |
|
|
Mất khối lượng khi làm khô |
Không được quá 0,5%. Sấy ở 105 °C trong 3 giờ. |
|
Mất khối lượng khi nung |
Không được quá 1,0% so với chế phẩm khô. Nung ở 800 °C |
|
Nhôm oxyd và/ hoặc silic dioxyd |
Không được quá 2%, một chất hoặc cả hai chất |
|
Các chất tan trong acid |
Không được quá 0,5%; Không được quá 1,5% đối với chế phẩm chứa nhôm oxyd hoặc silic dioxyd. |
|
Tạp chất tan trong nước |
Không được quá 0,5%. |
|
Các tạp chất tan trong acid hydrocloric 0,5 N |
|
|
Antimon |
Không được quá 2 mg/kg |
|
Arsen |
Không được quá 1 mg/kg |
|
Cadmi |
Không được quá 1 mg/kg |
|
Chì |
Không được quá 10 mg/kg |
Thủy ngân |
Không được quá 1 mg/kg |
5.3. Định lượng |
Không được nhỏ hơn 99,0 % tính theo chế phẩm khô (không tính nhôm oxyd và silic dioxyd) |
6. Phương pháp thử |
|
6.1 Định tính |
|
|
Phản ứng màu |
Thêm 5 ml acid sulfuric vào 0,5 g mẫu thử, đun nóng nhẹ tới khi xuất hiện khói của acid sulfuric, rồi để nguội. Pha loãng cẩn thận tới khoảng 100 ml với nước và lọc. Thêm vài giọt hydrogen peroxyd vào 5 ml dịch lọc trong; xuất hiện ngay màu đỏ cam. |
6.2. Độ tinh khiết |
|
|
Các chất tan trong acid
|
Tạo hỗn dịch 5 g mẫu thử trong 100 ml acid hydrocloric 0,5 N và đun trên nồi cách thủy sôi 30 phút, thỉnh thoảng khuấy. Lọc qua phễu lọc sứ với giấy lọc sợi thủy tinh. Rửa ba lần, mỗi lần bằng 10 ml acid hydrocloric 0,5 N, gộp dịch lọc và dịch rửa, cô cạn rồi nung nóng đỏ tối tới khối lượng không đổi. |
|
Tạp chất tan trong nước |
Tiến hành theo chỉ dẫn ở phần các chất tan trong acid (bên trên), dùng nước thay cho acid hydrocloric 0,5 N. |
Các tạp chất tan trong acid hydrocloric 0,5 N |
|
|
Antimon, arsen, cadmi và chì
|
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4: các phương pháp thử chung. Chuyển 10,0 g mẫu thử vào cốc 250 ml, thêm 50 ml acid hydrocloric 0,5 N, đậy bằng mặt kính đồng hồ và đun tới sôi trên bếp điện phẳng (bếp điện kín). Đun sôi nhẹ trong 15 phút, chuyển dịch treo vào chai ly tâm 100 tới 150 ml, ly tâm 10 tới 15 phút, hoặc tới khi các chất không tan lắng xuống. Gạn dịch chiết ở lớp trên qua giấy lọc Whatman No. 4 hoặc tương đương, thu dịch lọc vào bình định mức 100 ml, cố gắng giữ lại trong lọ được phần không tan càng nhiều càng tốt. Thêm 10 ml nước nóng vào cốc ban đầu, rửa mặt kính đồng hồ bằng nước, và cho vào chai ly tâm. Dùng đũa thủy tinh khuấy để tạo hỗn dịch rồi ly tâm. Gạn qua cùng tờ giấy lọc trên, thu dịch rửa vào bình định mức chứa dịch chiết ban đầu. Làm lặp lại quá trình rửa hai lần nữa. Cuối cùng rửa giấy lọc bằng 10 tới 15 ml nước nóng. Để nguội hỗn hợp trong bình tới nhiệt độ phòng, pha loãng tới vạch bằng nước, lắc đều. Xác định antimon, cadimi và chì, dùng kỹ thuật AAS/ICP-AES phù hợp với mức qui định. Xác định arsen dùng kỹ thuật ICP-AES/AAS hydrid hóa. Có thể thay thế bằng cách xác định arsen dùng Phương pháp II của Phép thử giới hạn Arsen, lấy 3 g mẫu thử thay cho 1 g. Lựa chọn cỡ mẫu thử có thể dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4: các phươgn pháp thử chung. |
|
Thủy ngân |
Xác định bằng kỹ thuật quang phổ hấp thụ nguyên tử hóa hơi lạnh. Chọn lựa cỡ mẫu thích hợp với nồng độ quy định. thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 |
|
Nhôm oxyd
|
Thuốc thử và dung dịch mẫu thử Kẽm sulfat 0,01 N Hòa tan 2,9 g kẽm sulfat (ZnSO4·7H2O) trong nước vừa đủ 1000 ml. Chuẩn hóa dung dịch theo cách sau: Cân chính xác 500 mg sợi nhôm có độ tinh khiết cao (99,9%), hòa tan trong 20 ml acid hydrocloric đặc, đun nóng nhẹ tới khi tan hết, sau đó chuyển sang bình định mức 1000 ml, thêm nước tới vạch, lắc đều. Chuyển 10 ml dung dịch này sang bình nón 500 ml chứa 90 ml nước và 3 ml acid hydrocloric đặc, thêm 1 giọt da cam methyl (TT) và 25 ml dinatri ethylen diamin tetraacetat (EDTA) 0,02 M. Thêm từng giọt dung dịch amoniac 1/5 tới khi màu vừa chuyển hoàn toàn từ màu đỏ thành màu vàng cam. Sau đó, thêm: (a): 10 ml dung dịch đệm amoni acetat (77 g amoni acetat thêm 10 ml acid acetic băng, thêm nước tới vừa đủ 1000 ml) và (b): 10 ml dung dịch diamoni hydrogen phosphat (150 g diamoni hydrogen phosphat trong 700 ml nước, điều chỉnh tới pH 5,5 bằng dung dịch acid hydrocloric ½, thêm nước tới vừa đủ 1000 ml). Đun sôi dung dịch này trong 5 phút, làm nguội nhanh tới nhiệt độ phòng dưới vòi nước, thêm 3 giọt da cam xylenol (TT), lắc đều. Dùng dung dịch kẽm sulfat làm dung dịch chuẩn, chuẩn độ tới điểm kết thúc khi dung dịch bắt đầu chuyển sang màu nâu vàng hoặc màu hồng bền trong 5-10 giây. (Chú ý: Phải chuẩn độ nhanh khi gần điểm kết thúc bằng cách thêm nhanh từng lượng 0,2 ml dung dịch chuẩn độ tới khi bắt đầu có sự chuyển màu; mặc dù màu sẽ bị nhạt trong 5-10 giây, đó là điểm kết thúc thực. Không quan sát được lần chuyển màu đầu tiên sẽ dẫn tới phép chuẩn độ không chính xác. Điểm kết thúc nhạt màu không xảy ra ở điểm kết thúc thứ hai.) Thêm 2 g natri fluorid, đun sôi hỗn hợp trong 2-5 phút, làm nguội dưới vòi nước. Dùng dung dịch kẽm sulfat chuẩn độ dung dịch này tới điểm kết thúc khi dung dịch bắt đầu chuyển sang màu nâu vàng hoặc màu hồng không bền như đã mô tả ở trên. Tính độ chuẩn T của dung dịch kẽm sulfat theo công thức sau: T = 18,896 m / V Trong đó: T là khối lượng (mg) của Al2O3 tác dụng vừa đủ với 1 ml dung dịch kẽm sulfat m là khối lượng (g) của sợi nhôm V là số ml của dung dịch kẽm sulfat dùng hết ở điểm chuẩn độ thứ hai 18,896 = (R × 1000 mg/g × 10 ml/2)/1000 ml và R là tỷ số trọng lượng theo công thức của nhôm oxyd và của nhôm nguyên tố Dung dịch mẫu thử A Cân chính xác 1 g mẫu thử và cho vào bình nón thủy tinh giàu silica 250 ml. Thêm 10 g natri bisulfat (NaHSO4·H2O). (Chú ý: Không được dùng natri bisulfat nhiều hơn qui định, nếu dư muối sẽ ảnh hưởng tới phép chuẩn độ bằng EDTA ở phần sau trong quy trình này). Bắt đầu đun nóng bình ở nhiệt độ thấp trên bếp điện phẳng, sau đó tăng nhiệt độ từ từ tới khi nóng hết cỡ. (Thận trọng: thực hiện qui trình này ở nơi thông gió tốt). Khi hỗn hợp ngừng nổ lộp bộp, và xuất hiện khói nhẹ của SO3, đun nóng trên ngọn lửa lớn bằng đầu đốt Meeker, để nghiêng bình sao cho hỗn hợp mẫu thử và natri bisulfat cô đặc lại ở một bên của đáy của bình. Lắc xoáy liên tục tới khi khối chất chảy trong ra (trừ silic dioxyd) nhưng chú ý không đun lâu quá để tránh kết tủa titan dioxyd. Làm nguội, thêm 25 ml dung dịch acid sulfuric 1:2, và đun nóng tới khi khối nhão hòa tan và thu được dung dịch trong suốt. Làm nguội, và pha loãng tới 120 ml bằng nước. Cho que khuấy từ vào bình. Dung dịch mẫu thử B Pha 200 ml dung dịch natri hydroxyd nồng độ xấp xỉ 6,25 M. Thêm 65 ml dung dịch này vào Dung dịch mẫu thử A, vừa thêm vừa khuấy bằng máy khuấy từ; cho 135 ml dung dịch kiềm còn lại vào một bình định mức 500 ml. Vừa khuấy liên tục, vừa thêm từ từ hỗn hợp mẫu thử vào dung dịch kiềm trong bình định mức 500 ml; thêm nước tới vạch, lắc đều. (Chú ý: Nếu dừng thí nghiệm tại thời điểm quá 2 giờ, phải để hỗn hợp trong bình định mức vào trong chai polyethylen). Để yên cho phần lớn tủa lắng xuống (hoặc ly tâm 5 phút), sau đó lọc lớp dịch phía trên qua giấy lọc rất mịn. Dán nhãn dịch lọc là Dung dịch mẫu thử B. Dung dịch mẫu thử C Chuyển 100 ml dung dịch mẫu thử B vào bình nón 500 ml, thêm 1 giọt da cam methyl (TT), acid hóa bằng dung dịch acid hydrocloric ½, sau đó thêm dư khoảng 3 ml. Thêm 25 ml dung dịch dinatri EDTA 0,02 M, và lắc đều. [Chú ý: Nếu biết hàm lượng xấp xỉ của Al2O3, tính thể tích tối ưu của dung dịch EDTA sẽ thêm theo công thức: (4 ´ % Al2O3) + 5]. Thêm từng giọt dung dịch amoniac 1/5 tới khi màu bắt đầu chuyển hoàn toàn từ đỏ thành màu vàng cam. Sau đó thêm 10 ml mỗi dung dịch 1 và dung dịch 2 (xem ở trên) và đun sôi trong 5 phút. Làm nguội nhanh tới nhiệt độ phòng dưới vòi nước, thêm 3 giọt da cam xylenol (TT), lắc đều. Nếu dung dịch có màu tím đỏ, màu nâu vàng, hoặc màu hồng, điều chỉnh pH tới 5,3–5,7 bằng cách thêm acid acetic. Tại pH này, màu hồng cho biết chưa thêm đủ dung dịch EDTA, trong trường hợp này, bỏ dung dịch này đi và lặp lại cách tiến hành này với 100 ml Dung dịch mẫu thử B khác, dùng 50 ml thay cho 25 ml dung dịch dinatri EDTA 0,02 M. Tiến hành Dùng dung dịch chuẩn kẽm sulfat để chuẩn độ, chuẩn độ Dung dịch mẫu thử C tới điểm kết thúc thứ nhất khi bắt đầu có màu vàng nâu hoặc hồng bền trong 5-10 giây. (Quan trọng: Xem chú ý ở phần “Kẽm sulfat 0,01 N”). Lần chuẩn độ đầu này cần đến hơn 8 ml dung dịch chuẩn độ, nhưng phép chuẩn độ sẽ chính xác hơn nếu lượng dung dịch chuẩn độ dùng là 10-15 ml. Thêm 2 g natri fluorid vào bình chuẩn độ, đun sôi hỗn hợp trong 2-5 phút, và làm nguội dưới vòi nước. Chuẩn độ dung dịch này bằng dung dịch kẽm sulfat đã chuẩn hóa tới khi có màu nâu vàng hoặc hồng không bền như đã mô tả ở trên. Tính toán: Tính phần trăm nhôm oxyd (Al2O3) trong mẫu thử theo công thức sau: % Al2O3 = 100 × (0,005VT)/m Trong đó: V là số ml dung dịch kẽm sulfat 0,01 N dùng hết trong lần chuẩn độ thứ hai, T là độ chuẩn của dung dịch kẽm sulfat, m là khối lượng (g) của mẫu thử, và 0,005 = 500 ml / (1000 mg/g × 100 ml). |
|
Silic dioxyd
|
Cân chính xác 1 g mẫu thử và cho vào bình nón thủy tinh giàu silica 250 ml. Thêm 10 g natri bisulfat (NaHSO4·H2O). Đun nóng bằng đầu đốt Meeker, vừa đun vừa lắc xoáy bình tới khi hỗn hợp phân hủy và nóng chảy hoàn toàn, và trở nên trong suốt, trừ phần silic dioxyd, sau đó làm nguội. (Thận trọng: Không được đun quá nóng hỗn hợp trong bình ngay từ đầu, và đun cẩn thận trong suốt quá trình chảy để khỏi bắn ra ngoài). Thêm 25 ml dung dịch acid sulfuric ½ vào hỗn hợp nóng chảy đã nguội và đun nóng cẩn thận và từ từ tới khi hỗn hợp này hòa tan. Để nguội và thêm cẩn thận 150 ml nước bằng cách rót từng lượng nhỏ vào theo thành bình, thỉnh thoảng khuấy tránh để quá nóng và bị bắn ra ngoài. Để nguội hỗn hợp trong bình, lọc qua giấy lọc không tro mịn, dùng phễu lọc 60o tự chảy. Rửa lấy hết toàn bộ silic dioxyd ra khỏi bình, lên trên giấy lọc bằng dung dịch acid sulfuric 1/10. Cho giấy lọc và cắn trên giấy lọc vào chén nung platin, làm khô trong tủ sấy ở 120 °C, và làm đốt nóng chén nung được đậy kín một phần bằng ngọn lửa Bunsen. Để giấy lọc không bị cháy thành ngọn lửa, trước tiên đốt nóng từ phía nắp, rồi sau mới nung chén từ phía dưới. Khi giấy lọc đã tàn hết, chuyển chén nung sang lò nung và nung ở 1000 °C trong 30 phút. Để nguội trong bình hút ẩm, và cân. Thêm 2 giọt dung dịch acid sulfuric ½ và 5 ml dung dịch acid hydrofluoric đặc (tỷ trọng tương đối khoảng 1,15), rồi cô cẩn thận tới khô, đầu tiên đun nóng nhẹ trên bếp điện phẳng (để loại HF), sau đó đốt bằng ngọn lửa Bunsen (để loại H2SO4). Làm cẩn thận tránh để bắn ra ngoài, đặc biệt sau khi loại HF. Nung ở 1000 °C trong 10 phút, để nguội trong bình hút ẩm, và cân. Độ chênh lệch giữa hai lần cân là lượng SiO2 có trong mẫu thử. |
6.3. Định lượng |
|
|
|
Cân chính xác khoảng 150 mg mẫu thử trước đó đã sấy khô ở 105 °C trong 3 giờ, cho vào bình nón 500 ml. Thêm 5 ml nước và lắc tới khi thu được hỗn dịch giống sữa đồng nhất. Thêm 30 ml dung dịch acid sulfuric và 12 g amoni sulfat, lắc đều. Lúc đầu đun nhẹ, sau đó đun mạnh tới khi thu được dung dịch trong suốt. Để nguội, sau đó pha loãng cẩn thận với 120 ml nước và 40 ml dung dịch acid hydrocloric, khuấy. Thêm 3 g nhôm kim loại, đậy ngay bình bằng nút cao su có gắn ống thủy tinh hình chữ U, đầu kia của ống chữ U ngập trong dung dịch natri bicarbonat bão hòa đựng trong lọ rộng miệng 500 ml, và tạo khí hydro. Để yên trong vài phút sau khi nhôm kim loại hòa tan hoàn toàn tạo thành dung dịch trong suốt màu tím đỏ. Làm nguội xuống dưới 50 °C dưới vòi nước, tháo nút cao su cùng ống chữ U. Thêm 3 ml dung dịch kali thiocyanat bão hòa làm chỉ thị, và chuẩn độ ngay bằng dung dịch sắt (III) amoni sulfat 0,2 N tới khi thu được dung dịch có màu nâu nhạt bền trong 30 giây. Tiến hành làm một mẫu trắng và hiệu chỉnh nếu cần thiết. 1 ml dung dịch sắt (III) amoni sulfat 0,2 N tương đương với 7,990 mg TiO2. |
PHỤ LỤC 29
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI SẮT OXYD
1. Tên khác, chỉ số |
Iron oxides; Sắt oxyd vàng: CI Pigment yellow 42 and 43; CI(1975) No. 77492; INS 172(iii) Sắt oxyd đỏ: CI Pigment red 101 and 102; CI (1975) No.77491; INS 172(ii) Sắt oxyd đen: CI Pigment black 11; CI (1975) No.77499; INS 172(i) ADI= 0 – 0,5 mg/kg thể trọng. |
2. Định nghĩa |
Chế phẩm được sản xuất từ sắt (II) sulfat bằng quá trình ngâm, nung nóng, loại nước, phân huỷ, rửa, lọc, sấy, nghiền. Chế phẩm chứa các thành phần sắt oxyd khan hoặc dạng hydrat, có các màu từ vàng, đỏ đến nâu và đen. Chất lượng sắt oxyd dùng trong thực phẩm phân biệt với sắt oxyd kỹ thuật qua hàm lượng các kim loại khác trong chế phẩm do việc lựa chọn và kiểm soát nguồn nguyên liệu sắt và công đoạn tinh chế hoá học trong suốt quá trình sản xuất. |
Tên hóa học |
Sắt oxyd vàng: Sắt oxyd dạng hydrat, Sắt (III) oxyd dạng hydrat Sắt oxyd đỏ: Sắt sesquioxyd, sắt (III) oxyd khan Sắt oxyd đen: hợp chất sắt (II) sắt (III) oxyd, sắt (II, III) oxyd |
Mã số C.A.S. |
Sắt oxyd vàng: 51274-00-1 Sắt oxyd đỏ: 1309-37-1 Sắt oxyd đen: 1317-61-9 |
Công thức hóa học |
Sắt oxyd vàng: FeO(OH) . xH2O Sắt oxyd đỏ: Fe2O3 Sắt oxyd đen: FeO . Fe2O3 |
Khối lượng phân tử |
88,85 FeO(OH) 159,70 Fe2O3 231,55 FeO . Fe2O3 |
3. Cảm quan |
Bột màu đen, nâu, đỏ hoặc vàng |
4. Chức năng |
Phẩm màu |
5. Yêu cầu kỹ thuật |
|
5.1. Định tính |
|
Độ tan |
Không tan trong nước và các dung môi hữu cơ; tan trong các acid vô cơ đậm đặc. |
Hợp chất hoà tan trong nước |
Không được quá 1,0%. |
5.2. Độ tinh khiết |
|
Giảm khối lượng khi sấy khô |
Sắt oxyd đỏ: không được quá 1% (sấy ở nhiệt độ 105oC trong 4h). |
Arsen |
Không được quá 3 mg/kg. |
Cadmi |
Không được quá 1 mg/kg. |
Chì |
Không được quá 10 mg/kg |
Thuỷ ngân |
Không được quá 1 mg/kg |
5.3. Hàm lượng |
Hàm lượng sắt không được thấp hơn 60%. |
6. Phương pháp thử |
|
6.1. Độ tinh khiết |
|
Arsen, cadmi và chì |
Cân 5 g mẫu thử và chuyển vào một cốc thuỷ tinh. Cho thêm 50 ml dung dịch acid sulfuric đặc và làm nóng trên một đĩa nóng cho đến khi hoà tan hoàn toàn. Pha loãng bằng nước cất đến vạch 100 ml trong bình định mức. Xác định cadmi và chì bằng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định và arsen dựa trên Phương pháp II của JECFA monograph 1-Vol. 4. |
Thuỷ ngân |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Xác định bằng kỹ thuật hấp thụ nguyên tử thích hợp cho hàm lượng quy định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong chuyên luận các phương pháp phân tích công cụ. |
6.2. Định lượng |
|
|
|
Cân 0,2 g mẫu thử, chính xác đến mg, cho thêm 10 ml dung dịch acid hydrocloric 5N và cẩn thận đun đến sôi trong một bình nón 200 ml cho tới khi mẫu thử tan hoàn toàn. Để nguội, cho thêm 6 đến 7 giọt dung dịch hydrogen peroxyd 30% và tiếp tục cẩn thận đun đến sôi cho đến khi toàn bộ hydrogen peroxyd dư bị phân huỷ (khoảng 2 đến 3 phút). Để nguội, cho thêm 30 ml nước cất và khoảng 2 g kali iodid và để yên trong 5 phút. Cho thêm 30 ml nước cất và chuẩn độ với dung dịch natri thiosulfat 0,1N, thêm chỉ thị là dung dịch hồ tinh bột (TT) đến điểm tương đương thì kết thúc chuẩn độ. Mỗi ml dung dịch natri thiosulfat 0,1N tương đương với 5,585 mg Fe (III). |
PHỤ LỤC 30
YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ ĐỐI VỚI FAST GREEN FCF
|
1. Tên khác, chỉ số |
CI food green 3,CI (1975): 42053 INSL: 143 ADI = 0 – 25 mg/kg thể trọng. |
|
2. Định nghĩa |
Chủ yếu gồm dinatri 3-[N-ethyl-N-[4-[[4-[N-ethyl-N-(3-sulfonbenzyl)amino]phenyl](4-hydroxy-2-sulfonphenyl)methylen]-2,5-cyclohexadien-1-yliden]amoniomethyl]benzensulfon và các đồng phân của nó cùng các chất màu phụ cùng với NaCl và (hoặc) Na2SO4 là các thành phần không màu chính. Có thể chuyển thành chất màu nhôm (aluminium lake) tương ứng, trong trường hợp này áp dụng quy định chung đối với các loại chất màu nhôm. |
|
Tên hóa học |
Dinatri 3-[N-ethyl-N-[4-[[4-[N-ethyl-N-(3-sulfonbenzyl) amino] phenyl](4-hydroxy-2-sulfonphenyl)methylen]-2,5-cyclohexadien-1-yliden] amoniomethyl]-benzensulfon; Muối dinatri nội của N-ethyl-N-[4[[4-ethyl[(3-sulfophenyl)methyl]amino]phenyl](4-hydroxy-2-sulfophenyl) methylen]-2,5-cyclohexadien-1-yliden]-3-sulfobenzen-methanamini hydroxyd. |
|
Mã số C.A.S. |
2353-43-9 |
|
Công thức hóa học |
C37H34N2Na2O10S3 |
|
Công thức cấu tạo |
|
|
Khối lượng phân tử |
808,86 |
|
3. Cảm quan |
Dạng bột hoặc tinh thể màu đỏ đến tím nâu. |
|
4. Chức năng |
Phẩm màu. |
|
5. Yêu cầu kỹ thuật |
|
|
5.1. Định tính |
|
|
Độ tan |
Tan trong nước, ít tan trong ethanol. |
|
Định tính các chất màu |
Phải có phản ứng đặc trưng của chất màu. |
|
5.2. Độ tinh khiết |
|
|
Giảm khối lượng khi làm khô tại 135oC |
Không được quá 15% cùng với clorid và sulfat tính theo muối natri. |
|
Chất không tan trong nước |
Không được quá 0,2% |
|
Chì |
Không được quá 2 mg/kg. |
|
Crom |
Không được quá 50 mg/kg. |
|
Các chất màu phụ |
Không được quá 6%. |
|
Các chất hữu cơ ngoài chất màu |
Không được quá 0,5% tổng các acid 2-; 3-; và 4-Formylbenzensulfonic và muối natri của các acid này. Không được quá 0,3% tổng các acid 3- và 4-[N-Ethyl-N-(4-sulfophenyl)amino]methylbenzensulfonic và muối dinatri của các acid này. Không được quá 0,5% tổng của acid 2-Formyl-5-hydroxybenzensulfonic và muối natri của nó. |
|
Các amin thơm bậc nhất không sulfon hoá |
Không được quá 0,01% tính theo anilin. |
|
Leuco base |
Không được quá 5,0%. |
|
Các chất có thể chiết bằng ether |
Không được quá 0,4%. |
|
5.3. Hàm lượng |
Không được thấp hơn 85% tổng các chất màu. |
|
6. Phương pháp thử |
|
|
6.1. Độ tinh khiết |
|
|
Chì |
Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4. Sử dụng kỹ thuật hấp thụ nguyên tử thích hợp với hàm lượng chỉ định để xác định. Lựa chọn cỡ mẫu thử và phương pháp chuẩn bị mẫu dựa trên nguyên tắc của phương pháp mô tả trong JECFA monograph 1-Vol. 4 phần các phương pháp phân tích công cụ. |
|
Các chất màu phụ |
Pha dung dịch mẫu thử 1%. Dùng syring chấm dung dịch mẫu thử lên bản mỏng silicagel (20 x 20 cm) sao cho lượng chấm là 1 mg mẫu thử. Để bản mỏng khô trong chỗ tối khoảng 20 phút sau đó cho bản mỏng vào bình chạy sắc ký đã bão hòa hệ dung môi khai triển sắc ký: acetonitril/alcol isoamylic/methyl ethyl keton/nước/dung dịch amoniac với tỷ lệ theo thể tích là 50/50/15/10/5. Để khai triển đến khi tuyến dung môi gần với đỉnh của bản mỏng. Lấy bản mỏng ra và để khô. Chất màu phụ xuất hiện tại các vị trí sau: trên cùng là 2 vết của chất màu phụ sulfon hóa thấp, tiếp theo là vết chính đồng màu của xanh lục bền FCF gần đáy bản mỏng. Cạo phần silicagel phía trên vết chính đồng màu. Chiết màu ra khỏi silicagel bằng ethanol, lọc qua phễu lọc thủy tinh xốp và đo quang phổ. Độ hấp thụ riêng tiêu chuẩn của các chất màu phụ là 0,126 mgL-1cm-1. Chú ý: Trong quá trình tính các chất màu phụ, thừa nhận rằng độ hấp thụ riêng tại các cực đại hấp thụ của chúng tương tự như độ hấp thụ riêng tại cực đại hấp thụ của các chất gốc. Dung dịch chuẩn phải được đo trong thời gian 1 giờ kể từ lúc pha. Dịch chiết chất màu phụ (ra khỏi silicagel) cần được đo quang phổ càng nhanh càng tốt. |
|
Các chất hữu cơ ngoài chất màu |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Sử dụng kỹ thuật sắc ký cột, với các điều kiện hấp thụ (ví dụ) như sau: Acid 3-formylbenzensulfonic: 0,495 mg L-1 cm-1 tại 246 nm trong HCl loãng Acid 3-[(ethyl)(4-sulfophenyl)amino] methyl benzensulfonic: 0,078 mg L-1 cm-1 tại 277 nm trong dung dịch amoniac loãng Acid 2-formyl-5-hydroxybenzensulfonic: 0,080 mg L-1 cm-1 tại 335 trong dung dịch amoniac loãng. |
|
Leuco base |
– Thử theo hướng dẫn tại JECFA monograph 1-Vol. 4 – Cân chính xác 110 ± 5 mg mẫu và tiến hành theo hướng dẫn trong chuyên luận thử Leuco base trong chất màu Triarylmethansulfon hóa. Độ hấp thụ riêng (a)=0,6 mgL-1cm-1 tại bước sóng khoảng 625 nm. Tỷ số = 0,971. |
|
6.2. Định lượng |
Tiến hành theo hướng dẫn trong chuyên luận xác định tổng hàm lượng bằng chuẩn độ với Titan (III) clorid (trong JECFA monograph 1-Vol. 4) như sau: Cân 1,9 – 2,0 g mẫu thử; Đệm 15 g natri hydrotartrat; Mỗi ml TiCl3 0,1 N tương đương với 40,45 mg các chất màu (D). |