Nội dung toàn văn Tiêu chuẩn quốc gia TCVN 10564:2015 (ISO/TS 22113:2012) về Sữa và sản phẩm sữa – Xác định độ axit chuẩn độ của chất béo sữa
TIÊU CHUẨN QUỐC GIA
TCVN 10564:2015
ISO/TS 22113:2012
SỮA VÀ SẢN PHẨM SỮA – XÁC ĐỊNH ĐỘ AXIT CHUẨN ĐỘ CỦA CHẤT BÉO SỮA
Milk and milk products – Determination of the titratable acidity of milk fat
Lời nói đầu
TCVN 10564:2015 hoàn toàn tương đương với ISO/TS 22113:2012;
TCVN 10564:2015 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F12 Sữa và sản phẩm sữa biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
SỮA VÀ SẢN PHẨM SỮA – XÁC ĐỊNH ĐỘ AXIT CHUẨN ĐỘ CỦA CHẤT BÉO SỮA
Milk and milk products – Determination of the titratable acidity of milk fat
1. Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp thông dụng để xác định độ axit chuẩn độ của chất béo sữa.
Phương pháp này có thể áp dụng cho chất béo sữa thu được từ:
a) sữa nguyên liệu;
b) sữa đã xử lý nhiệt;
c) sữa được hoàn nguyên từ sữa bột;
d) cream với hàm lượng chất béo bất kỳ, với điều kiện sản phẩm pha loãng để thu được hàm lượng chất béo từ 4 % đến 6 %.
Phương pháp này không áp dụng cho sữa lên men hoặc sữa bị nhiễm vi khuẩn hoặc bị enzym tác động.
CHÚ THÍCH 1: Quy trình chuẩn độ này cũng có thể áp dụng cho chất béo tách được từ một số loại sản phẩm khác.
CHÚ THÍCH 2: Quy trình này có thể được dùng để xác định từ năm đến vài trăm phần mẫu thử trong một ngày.
2. Nguyên tắc
Một lượng mẫu thử được trộn kỹ với dung dịch chứa natri tetraphosphat và chất hoạt động bề mặt. Hỗn hợp được làm nóng trong nồi cách thủy đun sôi để tách chất béo. Hòa tan một lượng chất béo chiết được vào dung môi hữu cơ và chuẩn độ bằng kiềm trong alcol.
3. Thuốc thử
Chỉ sử dụng các thuốc thử loại tinh khiết phân tích và nước cất hoặc nước đã loại khoáng hoặc nước có độ tinh khiết tương đương, trừ khi có quy định khác.
3.1. Dung dịch axit phosphoric, c(H3PO4) » 1 mol/l.
3.2. Thuốc thử BDI
Hòa tan 70 g natri tetraphosphat trong khoảng 700 ml nước cất mà không làm ấm thêm và trộn.
Thêm 30 g octylphenylpoly(etylenglycol) và trộn lại. Chỉnh pH đến 6,6 bằng dung dịch axit phosphoric (3.1), nếu cần. Pha loãng bằng nước đến 1 lít và trộn. Chỉnh pH bằng dung dịch axit phosphoric (3.1), nếu cần.
Nếu được bảo quản trong tủ lạnh và để ở nơi tối, dung dịch thuốc thử BDI có thể bền được 1 tháng.
CHÚ THÍCH: Natri tetraphosphat là polyphosphat chứa natri tetraphosphat (NaPO3)4là thành phần chính ngoài một vài các polyphosphat khác.
3.3. Dung dịch xanh thymol, c(C27H30O5S) = 0,1 g/l trong propan-2-ol
Để chuẩn bị dung dịch gốc, hòa tan 0,1 g muối natri của xanh thymol trong 100 ml propan-2-ol. Ngay trước khi sử dụng, pha loãng một thể tích dung dịch gốc với 9 thể tích propan-2-ol.
3.4. Dung môi dùng cho chất béo
Trộn một thể tích dung dịch xanh thymol (3.3) với bốn thể tích dầu nhẹ có dải sôi từ 60 °C đến 80 °C.
Dung môi dùng cho chất béo có thể bảo quản ở nơi tối đến 1 tháng.
3.5. Dung dịch kali hydro phtalat, c(KHC8H4O4) = 0,01 mol/l
Hòa tan 1,0211 g kali hydro phtalat trong bình định mức một vạch dung tích 500 ml (4.11). Pha loãng bằng nước đến vạch và trộn.
3.6. Dung dịch tetra-n-butylamoni hydroxit, c(C16H37NO) = 0,01 mol/l trong hỗn hợp của metanol và propan-2-ol
Pha loãng một thể tích tetra-n-butylamoni hydroxit c[(C4H9)4NOH)] = 0,1 mol/l trong hỗn hợp của metanol và propan-2-ol với chín thể tích propan-2-ol để thu được nồng độ cuối cùng c(C16H37NO) = 0,01 mol/l.
Nồng độ của dung dịch tetra-n-butylamoni hydroxit có thể bị thay đổi trong quá trình bảo quản và khi được chuyển vào buret. Do đó, nồng độ thực của dung dịch này cần được xác định chính xác tới 4 chữ số thập phân ngay trước khi dùng, bằng cách chuẩn độ đối chứng với dung dịch chuẩn kali hydro phtalat (3.5) dùng dung dịch xanh thymol (3.3) làm chất chỉ thị.
Nếu buret được lắp một bộ phận ngăn cách không cho cacbon dioxit lọt vào thì nồng độ của dung dịch có thể ổn định được 1 tháng.
3.7. Chất béo thí nghiệm và chất béo đối chứng
3.7.1. Chất béo thí nghiệm
Làm tan chảy một số loại chất béo sữa dạng khan (ví dụ 1 000 g) có độ axit béo từ 0,5 mmol/100 g đến 1,0 mmol/100 g chất béo. Chia mẫu chất béo sữa dạng khan đã tan chảy này thành các mẫu nhỏ (ví dụ 5 g).
Nếu được bảo quản trong tủ đông lạnh ở -20 °C hoặc thấp hơn, thì các mẫu chất béo nhỏ này có thể bền được ít nhất 2 năm.
Các mẫu chất béo sữa thí nghiệm này có thể dùng để kiểm tra độ tái lập của các kết quả thu được bằng quy trình chuẩn độ (7.2) hoặc trong suốt quá trình thực hiện của một lần thử nghiệm hoặc giữa nhiều lần thử nghiệm trong một quãng thời gian dài (vài tháng đến hàng năm).
3.7.2. Chất béo đối chứng
Các mẫu chất béo đối chứng gồm có chất béo sữa có độ axit béo thấp (chất béo cơ bản) được bổ sung axit palmitic (C16) với các mức tăng dần trong dải từ 0,5 mmol/100 g đến 1,5 mmol/100 g trên 100 g chất béo.
Độ chính xác của quy trình chuẩn độ có thể kiểm tra được bằng phương trình hồi quy sau đây (1):
(1)
Trong đó:
b(C16) là lượng axit palmitic được bổ sung vào chất béo cơ bản, tính bằng mmol/100 g chất béo;
Dblà giá trị BDI của các mẫu thêm chuẩn giảm dần do giá trị BDI trong chất béo cơ bản (mẫu trắng).
Việc chuẩn bị và các hướng dẫn sử dụng các mẫu chất béo đối chứng này được mô tả trong Phụ lục C.
4. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ thông thường của phòng thử nghiệm và các dụng cụ sau:
4.1. Pipet phân phối hoặc xyranh, dung tích 10 ml, 25 ml và 50 ml.
4.2. Ống chiết chất béo, có phần thân phía trên hẹp để thu nhận một lượng nhỏ chất béo chiết được ra khỏi hỗn hợp thuốc thử. Đường kính phần thân này phải đủ rộng để cho phép xyranh đã hiệu chuẩn (4.5) lấy mẫu chất béo. Các kiểu ống chiết chất béo được nêu trong Phụ lục A. Có thể sử dụng butyrometer theo TCVN 8172 (ISO 3432)[3].
CHÚ THÍCH: Việc chiết chất béo có thể thực hiện tốt bằng ly tâm, đặc biệt là trong các ống nghiệm có thân hẹp.
4.3. Nồi cách thủy, có thể duy trì nhiệt độ ở 45 °C ± 1 °C.
4.4. Nồi cách thủy đun sôi, có thể duy trì nhiệt độ bằng hoặc lớn hơn 95 0C.
4.5. Xyranh đã hiệu chuẩn, có thể điều chỉnh và phân phối được một lượng chất béo sữa đã biết khoảng 0,25 g ở 45 °C, chính xác đến 2 mg chất béo sữa.
CHÚ THÍCH: Theo kinh nghiệm, có thể sử dụng pipet xả hết (pipet tự động dạng xyranh) để chuyển định lượng chất béo chính xác và thuận tiện.
4.6. Bình chuẩn độ, có dung tích khoảng từ 10 ml đến 100 ml, tùy thuộc vào lượng mẫu cần dùng cho một lần chuẩn độ, có bộ phận khuấy.
4.7. Microburet, chia vạch nhỏ nhất là 0,002 ml.
4.8. Nitơ, không chứa cacbon dioxit.
4.9. Chai rửa khí, chứa dầu nhẹ có dải sôi từ 60 °C đến 80 °C, được nối với nitơ (4.8) và bình chuẩn độ (4.6).
4.10. Máy đo màu, có đầu dò nhúng, thích hợp để đo ở bước sóng từ 600 nm đến 620 nm, được nối với bình chuẩn độ (4.6).
4.11. Bình định mức một vạch, dung tích 100 ml đến 500 ml, phù hợp với loại A trong TCVN 7153 (ISO 1042)[2].
CHÚ THÍCH 1: Bình chuẩn độ (4.6), microburet (4.7) để chuyển chất chuẩn độ tetra-n-butylamoni hydroxit (3.6) trong môi trường khan, nguồn nitơ (4.8) qua chai rửa khí (4.9) và đầu đo nhúng được nối với máy đo màu (4.10) được lắp ráp trong thiết bị đặc thù (xem Phụ lục B) để chuẩn độ liên tiếp một số mẫu một lần và với cùng một thể tích dung môi chất béo.
CHÚ THÍCH 2: Có thể dùng thiết bị chuẩn độ thủ công đơn giản hơn và quan sát bằng mắt thường để xác định điểm kết thúc chuẩn độ khi không có máy đo màu có đầu dò nhúng.
5. Lấy mẫu
Việc lấy mẫu không quy định trong tiêu chuẩn này. Nên lấy mẫu theo TCVN 6400 (ISO 707)[1].
Điều quan trọng là mẫu gửi đến phòng thử nghiệm phải là mẫu đại diện. Mẫu thử nghiệm không được hư hỏng hoặc thay đổi trong quá trình bảo quản và vận chuyển.
6. Chuẩn bị mẫu thử
6.1. Lưu giữ và bảo quản
Các mẫu thử sữa hoặc cream phải được bảo quản và vận chuyển ở nhiệt độ từ 0 °C đến 4 °C (sữa bột có thể bảo quản ở nhiệt độ thường) và phân tích trong vòng 36 h.
Để bảo quản lâu hoặc bảo quản trong tủ lạnh ở xấp xỉ 5 °C, các mẫu thử nên được bảo quản bằng hydro peroxit ở nồng độ cuối cùng của H2O2là 0,2 g/l. Trong trường hợp này, mẫu có thể bảo quản được 4 ngày.
6.2. Xử lý mẫu thử
6.2.1. Mẫu sữa
Trộn kỹ bằng cách đảo chiều mẫu sữa nhẹ nhàng vài lần, không được làm tăng nhiệt độ.
6.2.2. Mẫu cream
Pha loãng mẫu cream, sử dụng sữa gầy tương ứng hoặc nước để thu được từ 4 % đến 6 % khối lượng chất béo.
Dùng nước để pha loãng cream dẫn đến mức axit béo tự do thu được thấp hơn so với sữa ban đầu. Trong những trường hợp này, sử dụng chương trình hiệu chính để thu được các kết quả chính xác (xem Tài liệu tham khảo [8]).
6.2.3. Mẫu sữa bột
Hòa tan khoảng 13 g sữa bột trong bình định mức một vạch dung tích 100 ml (4.11). Thêm 60 ml nước và trộn bằng máy trộn ở nhiệt độ phòng trong 70 min. Pha loãng bằng nước đến vạch 100 ml và trộn kỹ.
7. Cách tiến hành
7.1. Chiết chất béo
Trộn 3,5 phần mẫu thử (sữa, cream đã pha loãng hoặc sữa bột đã hoàn nguyên) (6.2) (± 3 %) vào 1 phần thuốc thử BDI (3.2) (± 1,5 %) trong ống chiết chất béo với các lượng như sau:
a) khi sử dụng ống MONED (4.2), trộn 31 ml ± 1 ml mẫu thử (6.2) và 8,9 ml ± 0,1 ml thuốc thử BDI (3.2);
b) khi sử dụng butyrometer Van Gulik (4.2), trộn 16,0 ml ± 0,5 ml mẫu thử (6.2) và 4,5 ml ± 0,1 ml thuốc thử BDI (3.2);
c) khi sử dụng các ống nghiệm khác, trộn các phần thể tích của mẫu (6.2) với thuốc thử BDI theo tỷ lệ 3,5 + 1 sử dụng các thể tích sao cho cột chất béo nằm trong phần thân ống chiết (4.2).
Ngay sau khi đầy, đóng ống chiết chất béo và trộn kỹ lượng chứa trong ống.
Đối với các mẫu sữa nguyên liệu, trộn nhẹ bằng cách đảo chiều ống nghiệm vài lần. Đối với các mẫu sữa đã xử lý nhiệt hoặc sữa bột đã hoàn nguyên thì lắc mạnh để tách chất béo.
Càng sớm càng tốt trong vòng 5 min, đặt ống vào nồi cách thủy đun sôi (4.4) duy trì ở nhiệt độ bằng hoặc lớn hơn 95 °C trong 15 min. Chú ý để duy trì nhiệt độ của nồi cách thủy ở trên 95 °C và mức nước của nồi cao hơn mức chứa trong ống nghiệm.
Đối với các ống nghiệm có thân hẹp và các mẫu sữa không phải là sữa nguyên liệu, có thể cần ly tâm ống nghiệm để tách chất béo được tốt hơn.
Trong trường hợp chất béo tách kém, đặt các ống nghiệm vào tủ lạnh để làm đông chất béo. Sau đó làm nóng lại trong nồi cách thủy đun sôi, chất béo sẽ tách được dễ hơn. Trong mọi trường hợp, chất béo phải trong suốt và không có các hạt.
Khi tách xong chất béo, đặt ống nghiệm vào nồi cách thủy (4.3) ở 45 °C. Đảm bảo rằng mức nước của nồi cách thủy cao hơn mức dung dịch chứa trong ống nghiệm.
7.2. Chuẩn độ
Tiến hành chuẩn độ trong bình chuẩn độ (4.6) ở môi trường không có cacbon dioxit. Nối bình chuẩn độ với nitơ (4.8) từ chai rửa khí (4.9). Định kỳ làm đầy chai rửa khí để bù lượng ete dầu mỏ bay hơi.
Chuyển một thể tích thích hợp dung môi dùng cho chất béo (3.4) và 0,25 g chất béo thí nghiệm (3.7.1) vào bình chuẩn độ (4.6) không có cacbon dioxit bằng cách dùng nitơ để thổi (4.8).
Kiểm tra việc cài đặt bước sóng của máy đo màu. Chỉnh thang đo màu ở độ truyền 0 % (tối) và ở 100 % (dung môi dùng chất béo với mẫu chất béo).
Chỉnh điểm kết thúc chuẩn độ ở 70 % trên thang truyền. Trung hòa dung môi dùng cho chất béo bằng dung dịch tetra-n-butylamoni hydroxit (3.6).
Dùng xyranh đã hiệu chuẩn (4.5), thêm một lượng đã biết khoảng 0,25 g chất béo thí nghiệm và chuẩn độ. Luôn lặp lại quy trình năm lần để kiểm tra các yêu cầu về độ lặp lại (9.2).
Nếu kết quả thu được của chất béo thí nghiệm nằm ngoài giới hạn lặp lại, thì kiểm tra thiết bị chuẩn độ (Phụ lục B) và quy trình chuẩn độ.
Dùng xyranh đã hiệu chuẩn (4.5), chuyển khoảng 0,25 g mẫu chất béo đã chuẩn bị (7.1) vào bình chuẩn độ và chuẩn độ.
Thay dung môi dùng cho chất béo bằng dung môi mới khi đã thực hiện được ba lần chuẩn độ trên 2 ml dung môi dùng cho chất béo (ví dụ: 60 lần chuẩn độ với 40 ml dung môi dùng cho chất béo).
Khi chuẩn độ số lượng nhỏ mẫu thử, có thể ước tính điểm kết thúc chuẩn độ bằng cách quan sát sự thay đổi màu (vàng đến xanh nhạt). Ít nhất hai lần chuẩn độ có thể thực hiện trong 5 ml dung môi dùng cho chất béo.
8. Tính và biểu thị kết quả
8.1. Tính kết quả
Tính độ axit béo của phần mẫu thử, bH+, biểu thị bằng milimol trên 100 g chất béo theo Công thức (2) sau đây:
(2)
Trong đó:
V là thể tích của dung dịch tetra-n-butylamoni hydroxit (3.6) đã dùng để chuẩn độ, tính bằng mililit (ml), biểu thị đến ba chữ số thập phân;
c là nồng độ chính xác của dung dịch tetra-n-butylamoni hydroxit (3.6), tính bằng mol trên lít (mol/l), biểu thị đến bốn chữ số thập phân;
m là khối lượng chất béo được chuyển bằng xyranh hiệu chuẩn sang bình chuẩn độ, tính bằng gam (g), biểu thị đến ba chữ số thập phân.
8.2. Biểu thị kết quả
Biểu thị kết quả đến hai chữ số thập phân.
9. Độ chụm
9.1. Phép thử liên phòng thử nghiệm
Các giá trị về độ lặp lại thu được từ phép thử liên phòng thử nghiệm được xác định phù hợp với TCVN 6910-1 (ISO 5725-1)[4]và TCVN 6910-2 (ISO 5725-2) [5]. Tuy nhiên, trong phép thử này chỉ có ba phòng thử nghiệm tham gia.
Do đó, các giá trị thu được chỉ để chỉ dẫn. Các chi tiết về phép thử liên phòng về độ chụm của phương pháp nêu trong Phụ lục D.
9.2. Độ lặp lại
Chênh lệch tuyệt đối giữa hai kết quả thử nghiệm riêng rẽ độc lập, thu được khi sử dụng cùng một phương pháp, phân tích trên cùng nguyên liệu thử, do cùng một người phân tích trong cùng một phòng thử nghiệm, dùng cùng thiết bị, trong một khoảng thời gian ngắn, không được quá 5 % các trường hợp lớn hơn 0,072 mmol/100 g.
10. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải bao gồm các thông tin sau:
a) mọi thông tin cần thiết về nhận biết đầy đủ mẫu thử;
b) phương pháp lấy mẫu sử dụng, nếu biết;
c) phương pháp thử sử dụng, viện dẫn tiêu chuẩn này;
d) mọi chi tiết thao tác không quy định trong tiêu chuẩn này, hoặc được coi là tùy chọn, cùng với các chi tiết bất thường nào khác có thể ảnh hưởng tới kết quả.
e) kết quả thử nghiệm thu được.
f) nếu kiểm tra độ lặp lại thì ghi kết quả cuối cùng thu được.
Phụ lục A
(tham khảo)
Các kiểu ống chiết chất béo
Kích thước tính bằng milimet
|
Hình A. 1 – Ống nghiệm MONED |
Hình A.2 – Kiểu ống chiết chất béo thông thường |
Phụ lục B
(tham khảo)
Thiết bị chuẩn độ điển hình để chuẩn độ liên tiếp một số mẫu trong một thể tích dung môi để chiết chất béo
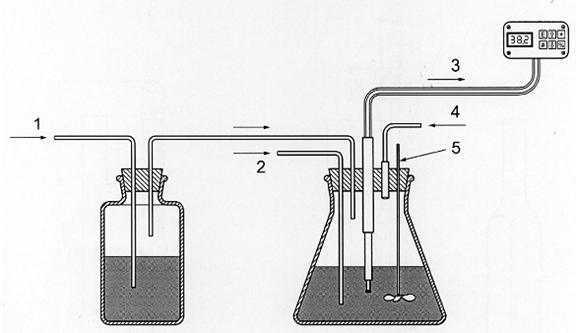
CHÚ DẪN
1 Nguồn cấp nitơ qua chai rửa có chứa ete dầu mỏ
2 Đầu vào của chất chuẩn độ tetra-n-butylamoni hydroxit dạng khan
3 Đầu dò quang học được nối với máy đo màu
4 Đầu vào của dung môi chất béo và mẫu chất béo
5 Que khuấy
Hình B.1 – Thiết bị chuẩn độ điển hình để chuẩn độ liên tiếp
Phụ lục C
(tham khảo)
Hướng dẫn chuẩn bị và sử dụng các mẫu chất béo đối chứng đối với quy trình chuẩn độ tiếp theo
C.1. Chuẩn bị mẫu chất béo đối chứng
C.1.1. Chất béo sữa cơ bản
Chuẩn bị một lượng đủ chất béo sữa có độ axit béo thấp. Làm tan chảy ở 38 °C.
C.1.2. Chuẩn bị chất béo đối chứng được bổ sung axit palmitic (C16)
C.1.2.1. Chất béo đối chứng A, được bổ sung 1,25 mmol axit palmitic trên 100 g chất béo
Cân 0,962 g ± 0,001 g axit palmitic, chính xác đến 0,1 mg. Hòa tan axit palmitic trong khoảng 300 g chất béo sữa cơ bản (C.1.1) và trộn.
Cân tổng số chất béo đối chứng A đã chuẩn bị, chính xác đến 0,01 g.
Thông thường axit palmitic không tinh khiết 100 %, do đó độ tinh khiết cần được tính đến khi cân axit palmitic. Ví dụ: khi độ tinh khiết của axit palmitic là 98 % thì lượng axit palmitic cần cân là 0,962/0,98 = 0,982 g thay vì 0,962 g.
Tính mức b(C16)1,25của axit palmitic trong chất béo đối chứng A, được tính bằng milimol trên 100 g, theo công thức (C.1) sau:
(C.1)
Trong đó:
w là độ tinh khiết của axit palmitic (w thường từ 0,98 đến 1,00), tính bằng phần khối lượng;
m1là khối lượng của axit palmitic dùng để chuẩn bị chất béo đối chứng A, tính bằng gam (g);
m2là tổng khối lượng chất béo đối chứng A đã chuẩn bị, tính bằng gam (g);
M là khối lượng phân tử của axit palmitic, tính bằng gam (M = 256,43 g/mol).
C.1.2.2. Chất béo đối chứng B, được bổ sung 1,00 mmol axit palmitic trên 100 g chất béo
Cân 80 g ± 0,01 g chất béo đối chứng A (C.1.2.1), chính xác đến 0,01 g. Hòa tan chất béo đối chứng A trong khoảng 20 g ± 0,01 g chất béo sữa cơ bản (C.1.1) và trộn.
Cân khối lượng chất béo đối chứng B đã chuẩn bị, chính xác đến 0,01 g.
Tính mức b(C16)1,00của axit palmitic trong chất béo đối chứng B, được tính bằng milimol trên 100 g, theo công thức (C.2) sau:
(C.2)
Trong đó:
m3là khối lượng của chất béo đối chứng A được hòa tan trong chất béo sữa cơ bản, tính bằng gam (g);
m4là tổng khối lượng chất béo đối chứng B đã chuẩn bị, tính bằng gam (g).
C.1.2.3. Chất béo đối chứng C, được bổ sung 0,75 mmol axit palmitic trên 100 g chất béo
Cân 60 g ± 0,01 g chất béo đối chứng A (C.1.2.1), chính xác đến 0,01 g. Hòa tan chất béo đối chứng A trong khoảng 40 g ± 0,01 g chất béo sữa cơ bản (C.1.1) và trộn.
Cân khối lượng chất béo đối chứng C đã chuẩn bị, chính xác đến 0,01 g.
Tính mức b(C16)0,75của axit palmitic trong chất béo đối chứng C, được tính bằng milimol trên 100 g, theo công thức (C.3) sau:
(C.3)
Trong đó:
m5là khối lượng của chất béo đối chứng A được hòa tan trong chất béo sữa cơ bản, tính bằng gam (g);
m6là tổng khối lượng chất béo đối chứng C đã chuẩn bị, tính bằng gam (g).
C.1.2.4. Chất béo đối chứng D, được bổ sung 0,50 mmol axit palmitic trên 100 g chất béo
Cân 40 g ± 0,01 g chất béo đối chứng A (C.1.2.1), chính xác đến 0,01 g. Hòa tan chất béo đối chứng A trong khoảng 60 g ± 0,01 g chất béo sữa cơ bản (C.1.1) và trộn.
Cân khối lượng chất béo đối chứng D đã chuẩn bị, chính xác đến 0,01 g.
Tính mức b(C16)0,50của axit palmitic trong chất béo đối chứng D, được tính bằng milimol trên 100 g, theo công thức (C.4) sau:
(C.4)
Trong đó:
m7là khối lượng của chất béo đối chứng A được hòa tan trong chất béo sữa cơ bản, tính bằng gam (g);
m8là tổng khối lượng chất béo đối chứng D đã chuẩn bị, tính bằng gam (g).
C.2. Ứng dụng các mẫu chất béo đối chứng
C.2.1. Xác định độ axit béo của chất béo đối chứng
Xác định độ axit béo của chất béo sữa cơ bản (C.1.1) (mẫu trắng), b0và các giá trị độ axit béo b1,25, b1,00, b0,75và b0,50của bốn mẫu chất béo đối chứng theo quy trình trong 7.2.
C.2.2. Tính và đánh giá các kết quả
Bảng C.1 – Tính kết quả
|
Nhận dạng mẫu |
Mức axit palmitic trong mẫu chất béo đối chứng b(C16)iđối chứng |
Giá trị BDI xác định được theo 7.2 |
DbN (bi– b0) |
Tỷ lệ DbN/b(C16)iđối chứng |
|
Chất béo cơ bản |
|
b0 |
|
|
|
Chất béo đối chứng A |
b(C16)1,25 |
b1,25 |
DbA |
[∆bA/b(C16)1,25]A |
|
Chất béo đối chứng B |
b(C16)1,00 |
b1,00 |
DbB |
[∆bB/b(C16)1,00]B |
|
Chất béo đối chứng C |
b(C16)0,75 |
b0,75 |
DbC |
[∆bC/b(C16)0,75]C |
|
Chất béo đối chứng D |
b(C16)0,50 |
b0,50 |
DbD |
[∆bD/b(C16)0,50]D |
Tóm tắt lại các lượng nêu trong Bảng C.1 như sau:
a) cột thứ 2 liệt kê các mức axit palmitic trong chất béo đối chứng A, B, C và D;
b) cột thứ 3 liệt kê các giá trị BDI của các chất béo đối chứng A, B, C và D, xác định được theo quy trình chuẩn độ trong 7.2;
c) cột thứ 4 liệt kê các giá trị DbA, DbB, DbC và DbDtính được bằng cách lấy các giá trị BDI của các chất béo đối chứng A, B, C và D trừ đi giá trị b0của chất béo sữa cơ bản.
Đối với từng mẫu chất béo đối chứng, tính các tỷ lệ DbN/b(C16)iđối chứng, trong đó N là A, B, C và D tương ứng và i là 1,25, 1,00, 0,75 và 0,50 tương ứng.
Tính độ lệch chuẩn sb(C16)p‘bcủa phương trình hồi quy (C.5):
b(C16)p = a + bb (C.5)
Trong đó:
b(C16)p là mức axit palmitic dự đoán có trong các mẫu chất béo đối chứng (C.1.1);
b là giá trị BDI của các mẫu chất béo đối chứng (C.1.2).
Nếu một hoặc nhiều hơn các tỷ lệ DbN/b(C16)iđối chứngnằm ngoài dải 1,00 ± 0,05 (nghĩa là nếu các giá trị sai khác quá 5 % so với giá trị dự kiến) hoặc nếu độ lệch chuẩn sb(C16)p‘b> 0,02 mmol/100 g chất béo, thì kiểm tra dung dịch chuẩn độ (3.6), thiết bị chuẩn độ (Phụ lục B) và quy trình chuẩn độ (7.2).
Sau khi kiểm tra, nếu độ lặp lại của các kết quả chuẩn độ trên chất béo thí nghiệm (3.7.1) tốt và các mẫu chất béo đối chứng (3.7.2) được khẳng định, nhưng độ lệch vẫn nằm ngoài dải 1,00 ± 0,05, thì kết quả chuẩn độ vẫn có độ lệch tái lập có hệ thống. Trước tiên vẫn phải giải quyết vấn đề này để thu được kết quả tin cậy.
CHÚ THÍCH: Sai số hệ thống phần lớn là do sai lỗi trong ước tính các thể tích được chuyển bằng xyranh (4.5) hoặc bằng microburet (4.7).
Phụ lục D
(tham khảo)
Thử nghiệm liên phòng
Một phép thử cộng tác lặp lại các mẫu mù do ba phòng thử nghiệm tham gia thực hiện trên sáu mẫu. Các mẫu đó là:
a) hai mẫu sữa dạng lỏng (S1 và S2);
b) hai mẫu sữa bột (S4 và S5);
c) hai mẫu cream (S5 và S6).
Các mẫu này đã được Cecalait, Poligny (Pháp) chuẩn bị và cung cấp, cho kết quả phân tích thống kê như trong Bảng D.1.
Bảng D.1 – Kết quả của phép thử
|
Thông số |
Mẫu |
Trung bình |
|||||
|
S1 |
S2 |
S3 |
S4 |
S5 |
S6 |
||
|
Số lượng phòng thử nghiệm tham gia |
3 |
3 |
3 |
3 |
3 |
3 |
|
|
Giá trị trung bình, mmol/100 g chất béo |
1,273 |
0,674 |
0,593 |
0,484 |
0,331 |
0,257 |
|
|
Độ lệch chuẩn lặp lại, sr, mmol/100 g chất béo |
0,031 |
0,018 |
0,043 |
0,019 |
0,021 |
0,010 |
0,026 |
|
Giới hạn lặp lại, r (= 2,8sr), mmol/100 g chất béo |
0,086 |
0,051 |
0,118 |
0,052 |
0,058 |
0,028 |
0,072 |
|
Độ lệch chuẩn, s, mmol/100 g chất béo |
0,064 |
0,037 |
0,062 |
0,004 |
0,011 |
0,036 |
|
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] TCVN 6400 (ISO 707) Sữa và sản phẩm sữa – Hướng dẫn lấy mẫu. [2] TCVN 7153 (ISO 1042) Dụng cụ thí nghiệm bằng thủy tinh – Bình định mức. [3] TCVN 8172 (ISO 3432) Phomat – Xác định hàm lượng chất béo – Dụng cụ đo chất béo sữa (butyrometer) dùng cho phương pháp Van Gulik. [4] TCVN 6910-1 (ISO 5725-1) Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo – Phần 1: Nguyên tắc và định nghĩa chung. [5] TCVN 6910-2 (ISO 5725-2) Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo – Phần 2: Phương pháp cơ bản xác định độ lặp lại và độ tái lập của phương pháp đo tiêu chuẩn. [6] Cartier, P., Chilliard, Y. và Chazal, M.P. Dosage de l’activité lipasique et des acides gras libres du lait par titration automatique colorimétrique [Determination of milk lipase activity and milk free fatty acid content using colorimetric automatic titration]. Le Lait 1984, 64, pp 340-355. [7] Driessen, F.M., Jellema, A., Van Luin, F.J.P., Stadhouders, G.J.M. The estimation of the fatty acid in raw milk. An adaptation of the BDI method, suitable for routine assays. Neth. Milk Dairy J, 1977, 31, pp. 40-55. [8] EVERS, J.M., LUCKMAN, S., PALFREYMAN, K.R. The BDI method – Part 1: Determination of free fatty acid in cream and whole milk powder. Austral. J.Dairy Technol. 2000, 55, pp. 33-36. [9] EVERS, J.M, Determination of free fatty acid in milk using BDI method – Some pratical and theortical aspects. Int. DairyJ. 2003, 13, pp. 111-121. [10] JELLEMA, A. Automatische titratie met behulp van een colorimeter bij the bepaling van de zuurtegraad van het vet. Verslag van een orientenrend onderzoek [Automatic titration with the aid of colorimeter in the determination of the degree of fat acidity. Report of an exploratory study]. MOC in Wageningen, in the cooperation with Instrument Trading “South Holland” v/h A. Hofelt BV in The Hague, 1979-11. [11] JELLEMA, A., OGER, R. VAN REUSEL, A. Milk fat products and butter – Determination of fat acidity. Collaborative study by joint IDF/ISO/AOAC group E39. Bull, IDF 1988 (235), pp. 81-91. [12] KUZDZAI-SAVOIE, S. Determiation of free fatty acid in milk and milk products. Bull. IDF 1980 (118), pp. 53-66. [13] PERRIN, D.R., PERRIN, D.D. The determination of the fatty acids in milk. J. Dairy Res. 1958, 25, pp. 221-227. [14] Standard methods for the determitation of dairy products, 17thedition. New York, NY: Americal public Health Association, 2004. [15] VAN REUSEL, A. Contribution à l’étude da la détermination des acides gras libres dans le lait et les produits laitiers. [Contribution to the study of the determination of free fatty acids in milk and dairy products]. Gembloux: Centre de Recherches Agronomiques de I’Etat, 1989. (Mémoire n. 12).BDI là từ viết tắt của “Bureaux of Dairy Industries”, là tổ chức đầu tiên xây dựng phương pháp này.
Triton X-100 là ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra để thuận tiện cho người sử dụng tiêu chuẩn mà không ấn định sử dụng sản phẩm này.


