Nội dung toàn văn Tiêu chuẩn Việt Nam TCVN 6944:2001 (ISO 4876 : 1980) về Thuốc lá và sản phẩm thuốc lá – Xác định dư lượng Maleic hidrazit do Bộ Khoa học Công nghệ và Môi trường ban hành
TIÊU CHUẨN VIỆT NAM
TCVN 6944:2001
THUỐC LÁ VÀ SẢN PHẨM THUỐC LÁ – XÁC ĐỊNH DƯ LƯỢNG MALEIC HIDRAZIT
Tobacco and tobacco products – Determination of maleic hydrazide residues
1. Phạm vi áp dụng
Tiêu chuẩn này qui định phương pháp xác định dư lượng maleic hidrazit trong thuốc lá và sản phẩm thuốc lá.
Phương pháp này áp dụng cho thuốc lá và sản phẩm thuốc lá và các dư lượng từ các chất diệt chồi maleic hidrazit được sử dụng trên cây thuốc lá.
2. Tiêu chuẩn viện dẫn
ISO 1042 Laboratory glassware – One-mark volumetric flasks (Dụng cụ thủy tinh phòng thí nghiệm – Bình định mức một vạch).
ISO 1770 Solid-stem general purpose thermometers (Nhiệt kế thân cứng thông dụng).
ISO 4793 Laboratory sintered (fritted) filters – Porosity grading, classification and designation (Bộ lọc xốp (thủy tinh xốp) phòng thí nghiệm – Phân loại theo độ xốp, phân loại và tên gọi).
TCVN 5080 – 90 (ISO 4874) Thuốc lá và sản phẩm thuốc lá – Điều kiện chung về việc lấy mẫu.
3. Nguyên tắc
Đun sôi phần mẫu thử với dung dịch natri hydroxit để loại bỏ các hợp chất bay hơi. Thêm bột kẽm và dùng khí hidro mới sinh để khử maleic hidrazit thành sucxinic hidrazit mà sau đó sẽ được thủy phân.
Chưng cất hidrazin được giải phóng và đo quang phổ phức chất màu vàng với 4-dimetylaminobenzaldehit.
Nếu cần, có thể phân hủy sơ bộ phần mẫu thử bằng axit và dùng than để làm sạch phần dịch cất.
4. Thuốc thử
Trong quá trình phân tích chỉ sử dụng các thuốc thử tinh khiết phân tích và nước cất hoặc nước có độ tinh khiết tương đương.
4.1. 4-dimetylaminobenzaldehit, 20 g/l trong dung dịch axit sunfuric 0,5 M.
4.1.1. Tinh chế thuốc thử
Hòa tan 20 g 4-dimetylaminobenzaldehit trong 150 ml etanol nguyên chất. Cho thêm 5 g bột than đã hoạt hóa và khuấy bằng cơ học trong 5 phút. Lọc qua phễu lọc Buchner và thêm từ từ 200 ml nước ở 0°C vào dịch lọc trong khi vẫn khuấy liên tục. Lọc tinh thể màu trắng hoặc màu vàng nhạt qua phễu Buchner và dùng 50 ml nước lạnh để rửa tinh thể. Làm khô trong bình hút ẩm chân không trên phospho (V) oxit và bảo quản trong chai tối màu.
4.1.2. Chuẩn bị dung dịch thuốc thử
Hòa tan 2 g tinh thể đã tinh chế trong 100 ml dung dịch axit sunfuric 0,5 M (4.6); lọc qua phễu lọc bằng thủy tinh xốp, nếu cần.
Thuốc thử này có thể ổn định đến 1 tháng nếu được bảo quản trong chai tối màu để trong tủ lạnh, nếu không thì hàng ngày nên chuẩn bị thuốc thử mới.
4.2. Maleic hidrazit, dung dịch tiêu chuẩn chứa tương ứng 10 µg/ml.
Cân 10 mg maleic hidrazit tinh khiết, chính xác đến 0,1 mg và hòa tan trong 100 ml dung dịch natri hidroxit 0,1 M (4.5) và pha loãng bằng nước đến 1 000 ml.
4.3. Bột kẽm, có cỡ hạt 500 µm, có mật độ khối không quá 1,70 g/cm3.
Thực tế cho thấy rằng việc sử dụng loại bột kẽm là điều rất quan trọng. Cần lưu ý là bột kẽm được sử dụng nên được kiểm tra bằng cách so sánh màu tạo nên bởi các dung dịch tiêu chuẩn của hidrazin sunfat và 4-dimetylaminobenzaldehit với màu của maleic hidrazit sau khi khử và chưng cất.
4.4. Natri hidroxit, dung dịch 12,5 M.
4.5. Natri hidroxit, dung dịch 0,1 M.
4.6. Axit sunfuric, dung dịch 0,5 M.
4.7. Sắt (II) clorua ngậm 4 nước (FeCI2.4H2O).
Nên kiểm tra thuốc thử để đảm bảo rằng không tạo màu với dung dịch 4-dimetylaminobenzaldehit.
4.8. Chất chống tạo bọt (sáp paraffin hoặc dầu thực vật tinh luyện).
4.9. Hạt chống sôi trào.
4.10. Dầu có nhiệt độ sôi cao, dùng cho ống đựng nhiệt kế.
4.11. Thuốc lá, biết trước là không chứa maleic hidrazit và có đặc tính giống với thuốc lá cần thử nghiệm (xem chú thích trong 7.4).
5. Thiết bị, dụng cụ
Thiết bị, dụng cụ phòng thí nghiệm thông thường và các dụng cụ sau:
5.1. Bình định mức một vạch, dung tích 25 ml, 100 ml và 1 000 ml, phù hợp với các yêu cầu trong ISO 1042, loại A.
5.2. Ống đong, dung tích 100 ml.
5.3. Cốc, dung tích 250 ml.
5.4. Phễu lọc bằng thủy tinh xốp (phễu Buchner), có độ xốp P 100, phù hợp với yêu cầu của ISO 4793.
5.5. Thiết bị chưng cất hơi nước (xem hình vẽ), gồm có:
a) bộ tạo hơi nước;
b) bình phản ứng / chưng cất;
c) bộ ngưng;
d) bếp đun nóng kiểm soát được ở các nhiệt độ khác nhau.
Bình phản ứng / chưng cất phải là loại đáy phẳng, có dung tích 500 ml, bình có thành dày được gắn với khớp nối hình cầu và một ống đựng nhiệt kế có thang đo từ 0 °C đến 360 °C phù hợp với yêu cầu của ISO 1770, số 9/75.
Máy cấp hơi nước và bình phản ứng / chưng cất phải được nối với nhau qua vòi ba nhánh. Nhánh ra thứ ba được dùng cho hơi nước thải ra qua bộ ngưng khi không cần. Điều này cho phép duy trì tốc độ sôi đều trong máy phát khi đang thay bình phản ứng / chưng cất.
Cảnh báo – Tất cả các thiết bị phải được che chắn bằng lưới an toàn.
5.6. Máy so màu phân quang, thích hợp để đo ở các bước sóng 425 nm, 455 nm và 485 nm và được gắn các cuvet 10 mm.
6. Lấy mẫu
Tiến hành lấy mẫu theo qui trình qui định trong TCVN 5080-90 (ISO 4874).
7. Cách tiến hành
7.1. Chuẩn bị mẫu
Nghiền mẫu trong cối nghiền phòng thí nghiệm sao cho tất cả mẫu nghiền lọt hết qua sàng có cỡ lỗ 2 mm. Trộn kỹ mẫu đã nghiền.
7.2. Phần mẫu thử
Cân 1 g mẫu đã chuẩn bị chính xác đến 0,01 g.
7.3. Tiến hành xác định
Nếu cần, có thể phân hủy sơ bộ bằng axit trước khi phân hủy bằng kiềm (xem phụ lục A).
7.3.1. Phân hủy bằng kiềm
Chuyển phần mẫu thử vào bình phản ứng / chưng cất. Cho thêm 50 ml dung dịch natri hidroxit (4.4), một ít chất chống tạo bọt (4.8) và một vài hạt chống sôi trào (4.9) vào bình. Đặt nhiệt kế có thể đo được từ 0oC đến 360oC vào ống đựng nhiệt kế chứa dầu có điểm sôi cao (4.10) và đun nóng bình một cách cẩn thận, thỉnh thoảng xoay bình. Giảm lượng chứa trong bình cho đến khi nhiệt kế chỉ 165 °C; thao tác này kéo dài khoảng từ 10 min đến 15 min. Để nguội trong 5 min.
7.3.2. Chưng cất (xem phụ lục B)
Bật máy cấp hơi nước và đặt ống đong dung tích 100 ml (5.2) chứa 10 ml dung dịch axit sunfuric (4.6). sao cho điểm cuối bộ ngưng thấp hơn bề mặt của axit. Thêm 0,5 g sắt (Il) clorua (4.7) và 15 g bột kẽm (4.3) vào lượng chứa trong bình phản ứng / chưng cất. Nối bình với thiết bị và bắt đầu chưng cất bằng cách sục hơi nước vào bình và đun nóng đến 200 oC ± 10 °C. Trong suốt quá trình chưng cất duy trì tốc độ dòng nước lạnh nhanh đến bộ ngưng. Trong suốt qui trình chưng cất duy trì bình ở nhiệt độ này để đảm bảo trong vòng 20 min nhận được khoảng 100 ml dịch cất. Tráng đầu ra của bộ ngưng vào dịch cất. Làm lạnh dịch cất và lọc qua phễu lọc thủy tinh xốp (5.4) vào cốc dung tích 250 ml, dùng 5 ml nước để tráng ống đong và phễu. Cho vài hạt chống sôi trào vào cốc và cho cốc bay hơi trên bộ phận gia nhiệt đến khi còn trên 6 ml. Cách khác, dịch cất có thể được cô đặc trong bộ bay hơi quay.
Nếu cần, dịch cất có thể được làm sạch trước khi tiến hành tiếp (xem phụ lục A).
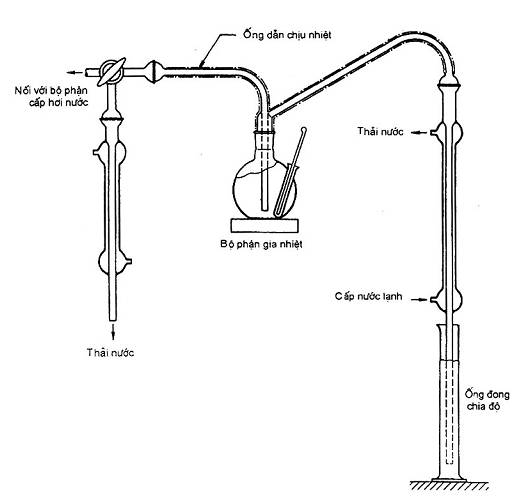
Hình vẽ – Thiết bị dùng để xác định maleic hidrazit trong thuốc lá
7.3.3. Phản ứng với 4-dimetylaminobenzaldehit
Làm nguội dịch lọc đã cô đặc như mô tả trong 7.3.2. chuyển hết sang bình định mức 25 ml (5.1) và cho thêm 2 ml dung dịch 4-dimetylaminobenzaldehit (4.1) trước khi thêm nước cho đến vạch. Đậy nắp bình, trộn kỹ lượng chứa trong bình và để yên 30 min nơi tối.
7.3.4. Đo quang phổ
Làm đầy cuvet 10 mm bằng dung dịch thu được trong 7.3.3.
Cho 10 ml dung dịch axit sunfuric (4.6) vào 2 ml 4-dimetylaminobenzaldehit (4.1) trong bình định mức, pha loãng bằng nước đến 25 ml và làm đầy cuvet đối chứng bằng dung dịch này.
Đo độ hấp thụ của dung dịch thử nghiệm trên máy so màu phân quang (5.6) ở các bước sóng 425 nm, 455 nm và 485 nm.
Tính độ hấp thụ đã hiệu chỉnh của dung dịch thử nghiệm, Acorr từ công thức:
![]()
trong đó
A425, A455 và A485 là các độ hấp thụ của dung dịch tương ứng ở các bước sóng 425 nm, 455 nm và 485 nm.
Nếu độ hấp thụ ở 455 nm vượt quá 0,8 thì pha loãng tiếp dung dịch thử bằng hỗn hợp của 2 ml 4-dimetylaminobenzaldehit (4.1) và 10 ml dung dịch axit sunfuric (4.6), đã được pha loãng bằng nước đến 25 ml.
Thực hiện hai phép xác định trên cùng một mẫu đã chuẩn bị.
7.4. Đường hiệu chuẩn
Cho các lượng 0 ml, 1 ml, 2 ml, 5 ml và 8 ml dung dịch maleic hidrazit tiêu chuẩn (4.2), tương ứng với từ 0 µg đến 80 µg maleic hidrazit vào các phần mẫu thử 1 g thuốc lá (4.11) và xử lý như mô tả trong 7.3.1, 7.3.2 và 7.3.3 ở trên.
Đo độ hấp thụ của các dung dịch thử tiêu chuẩn đã chuẩn bị như trong 7.3.4. Chuẩn bị đường hiệu chuẩn liên quan đến độ hấp thụ với hàm lượng maleic hidrazit, tính bằng microgam các dung dịch thử tiêu chuẩn.
Chú thích – Nếu không có sẵn thuốc lá thích hợp cho việc hiệu chuẩn, thì việc hiệu chuẩn dung dịch maleic hidrazit tiêu chuẩn khi không có thuốc lá là có thể chấp nhận được.
8. Biểu thị kết quả
8.1. Phương pháp tính và công thức
Đọc từ đường hiệu chuẩn lượng maleic hidrazit có mặt trong dung dịch mẫu thử.
Hàm lượng maleic hidrazit, biểu thị bằng microgam trên gam thuốc lá, được tính theo công thức:
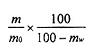
trong đó
m là khối lượng maleic hidrazit có trong dung dịch mẫu thử đã đọc được từ đường hiệu chuẩn, tính bằng microgam;
mo là khối lượng của phần mẫu thử thuốc lá, tính bằng gam;
mw là hàm lượng nước trung bình của mẫu.
Việc hiệu chỉnh nên được thực hiện đối với mọi độ pha loãng tiếp theo (xem 7.3.4).
Lấy kết quả là trung bình của hai giá trị với điều kiện các yêu cầu về độ lặp lại (8.2) được thoả mãn.
8.2. Độ lặp lại
Chênh lệch giữa các kết quả trong các phép xác định kép, được thực hiện trong cùng thời điểm hoặc kế tiếp nhau, do cùng một người phân tích không được vượt quá 5% giá trị trung bình của chúng, khi giá trị trung bình đó lớn hơn 10 µg/g, hoặc 1 µg/g khi giá trị trung bình nhỏ hơn 10 µg/g.
9. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải chỉ rõ phương pháp đã sử dụng và các kết quả thu được. Báo cáo thử nghiệm cũng phải đề cập đến tất cả các chi tiết thao tác không qui định trong tiêu chuẩn này, hoặc tùy ý lựa chọn (thí dụ, qui trình đặc biệt được mô tả trong phụ lục A), cùng với mọi chi tiết bất thường khác có thể ảnh hưởng tới kết quả.
Báo cáo thử nghiệm cũng bao gồm tất cả các thông tin cần thiết về việc nhận biết đầy đủ mẫu thử.
PHỤ LỤC A
CÁC QUI TRÌNH BỔ SUNG TỰ CHỌN
A.1. Khái quát
A.1.1. Các protein có mặt trong thuốc lá đôi khi có thể làm tạo bọt quá nhiều trong suốt quá trình phân hủy kiềm và trong các giai đoạn chưng cất. Giai đoạn phân hủy sơ bộ bằng axit được mô tả trong A.2 sẽ phá vỡ các protein và hạn chế việc tạo bọt.
A.1.2. Một số loại thuốc lá, đặc biệt là thuốc lá có tỷ lệ bazơ cao, chứa các chất tự nhiên gây nhiễu bằng phản ứng màu và tạo màu đỏ với 4-dimetylaminobenzaldehit. xử lý dịch cất bằng cacbon hoạt hóa như mô tả trong A.3 để hạn chế ảnh hưởng này.
A.1.3. Không nên sử dụng các qui trình này trừ khi người phân tích thấy nó cần thiết cho các mẫu cụ thể cần thử nghiệm.
A.2. Phân hủy sơ bộ bằng axit
A.2.1. Thuốc thử bổ sung yêu cầu
A.2.1.1. Axit clohidric, dung dịch khoảng 3 M.
Pha loãng 270 ml axit clohidric, r khoảng 1,18 g/ml, bằng nước đến 1 000 ml và trộn.
A.2.1.2. Dung dịch natri hidroxit, 700 g/l.
A.2.2. Cách tiến hành
Chuyển phần mẫu thử sang bình phản ứng / chưng cất. Thêm 50 ml axit clohidric (A.2.1.1) và một lượng nhỏ sáp paraffin. Đun nóng bình và cho sôi lượng chứa trong bình ở tốc độ vừa phải cho đến khi thể tích giảm xuống từ 20 ml đến 25 ml. Dùng 25 ml nước rửa xuôi xuống thành bình và đun sôi lại cho đến khi thể tích lại giảm xuống 20 ml đến 25 ml. Để nguội.
Chú thích – Ở giai đoạn này, thuốc lá đã phân hủy từng phần có thể để qua đêm, nhưng một khi đã cho thêm natri hidroxit thì phải kết thúc phép thử càng sớm càng tốt.
Thêm từ từ 50 ml dung dịch natri hidroxit (A.2.1.2) trong khi vẫn khuấy liên tục và tiến hành phân hủy bằng kiềm như trong 7.3.1.
A.3. Hấp thụ cacbon
A.3.1. Thuốc thử bổ sung yêu cầu
A.3.1.1. Cacbon hoạt hóa1)
A.3.2. Cách tiến hành
Lắc kỹ 1 phút dịch cất thu được trong 7.3.2 cùng với 2 g cacbon hoạt hóa (A.3.1.1) và lọc trước khi cô đặc đến 6 ml như hướng dẫn trong 7.3.2.
PHỤ LỤC B
CHÚ THÍCH VỀ QUI TRÌNH CHƯNG CẤT
B.1. Lưới bảo vệ phải được đặt đúng vị trí trong suốt quá trình chưng cất.
B.2. Sau khi chưng cất, dùng găng tay chịu nhiệt và kính bảo vệ để tháo bình đang nóng ra khỏi thiết bị. Tháo nhiệt kế, dùng nút nhỏ để đậy kín ống đựng nhiệt kế. Tráng rửa ống dẫn hơi nước cho sạch natri hidroxit. Rót lượng đựng trong bình chưng cất qua sàng bằng sắt trong máng xả để giữ lại các hạt kẽm và tráng bình ba lần bằng nước và tráng hai lần bằng dung dịch axit clohidric 10% (V/V) để loại bỏ kiềm ăn da kết thành vỏ ngoài và các hạt kẽm. Làm đầy bình bằng dung dịch axit clohidric cho đến khi sử dụng lần sau.
Trước khi sử dụng lại, tráng bình ba lần bằng nước. Điều cần thiết để loại bỏ hết kẽm còn sót lại vì chúng có thể làm phân hủy sớm maleic hidrazit trong giai đoạn phân hủy sơ bộ của phép xác định tiếp theo.
B.3. Bình chưng cất phải được kiểm tra thường xuyên vì chúng có thời hạn sử dụng rất ngắn do tác dụng của dung dịch natri hidroxit.
B.4. Nên sử dụng mỡ silicon có độ chân không cao để bôi lên tất cả các khớp cầu của thiết bị. Khi cho thêm sắt (II) clorua và các hạt kẽm vào bình phản ứng / chưng cất phải chú ý không để hạt nào dính vào mỡ làm cản trở việc làm kín khớp nối.
B.5. Phải chú ý khi thực hiện loại bỏ các hạt kẽm vì có thể nguy hiểm do cháy.
1) Sản phẩm thích hợp có bán sẵn. Chi tiết có thể thu được từ ban thư ký ISO/TC 126 (DIN. Germany, F.R) hoặc từ ISO.


