Nội dung toàn văn Tiêu chuẩn Việt Nam TCVN 7873:2008 về nước – Xác định hàm lượng Benzen – Phương pháp sắc ký khối phổ (GC/MS) sử dụng cột mao quản
TIÊU CHUẨN QUỐC GIA
TCVN 7873 : 2008
NƯỚC – XÁC ĐỊNH HÀM LƯỢNG BENZEN – PHƯƠNG PHÁP SẮC KÝ KHỐI PHỔ (GC/MS) SỬ DỤNG CỘT MAO QUẢN
Water – Determination of benzene content – Purge and trap capillary – column gas chromatographic/mass spectrometric method
Lời nói đầu
TCVN 7873 : 2008 được xây dựng trên cơ sở SMEWW “Standard methods for the examination of water and wastewater 6200 B Volatile organic compounds Purge and trap capillary-column gas chromatographic/mass spectrometric method”
TCVN 7873 : 2008 do Tiểu Ban kỹ thuật tiêu chuẩn TCVN/TC47/SC2 Hóa học – Phương pháp thử biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
NƯỚC – XÁC ĐỊNH HÀM LƯỢNG BENZEN – PHƯƠNG PHÁP SẮC KÝ KHỐI PHỔ (GC/MS) SỬ DỤNG CỘT MAO QUẢN
Water – Determination of benzene content – Purge and trap capillary – column gas chromatographic/mass spectrometric method
1. Phạm vi áp dụng
Tiêu chuẩn này qui định phương pháp xác định hàm lượng benzen có trong nước bằng phương pháp sắc ký khối phổ (GC/MS) sử dụng cột mao quản.
Phương pháp này cũng áp dụng cho các hợp chất hữu cơ dễ bay hơi khác.
2. Nguyên tắc
Các hợp chất hữu cơ dễ bay hơi được chuyển toàn bộ từ pha nước sang pha khí bằng cách sục khí trơ (ví dụ như heli) qua mẫu nước chứa trong thiết bị sục chuyên dụng và được thực hiện ở nhiệt độ phòng. Hơi hữu cơ đi qua bộ phận bẫy hấp thụ, các chất hữu cơ được lưu giữ sau đó được giải hấp bằng nhiệt và dòng khí mang đưa chất cặn phân tích vào cột tách. Sắc ký khi được lập trình chương trình nhiệt độ nhằm tách các chất Detector là khối phổ kế.
3. Cản trở
Sự nhiễm bẩn chủ yếu là do các tạp chất trong khí mang và khí thải hữu cơ. Để chứng minh hệ thống không bị nhiễm bẩn trong khi vận hành, hằng ngày phải phân tích mẫu trắng.
CHÚ THÍCH – Chỉ sử dụng mẫu thử trắng cho mục đích kiểm soát không dùng mẫu trắng để hiệu chỉnh kết quả.
Trong hệ thống sục va bẫy, phải sử dụng ống nhựa và gioăng TFE, không sử dụng bộ điều chỉnh dòng chảy có các thành phần cao su. Phải đảm bảo vùng phân tích không bị nhiễm bẩn từ các dung môi phòng thí nghiệm, đặc biệt là metylen clorua và metyl tert butyl ete (MTBE).
Mẫu có thể bị nhiễm bẩn do sự khuếch tán của các chất hữu cơ dễ bay hơi (đặc biệt là florocacbon và metylen clorua) qua nắp đậy trong quá trình vận chuyển hoặc lưu giữ. Để kiểm tra việc nhiễm bẩn cần sử dụng mẫu trắng được chuẩn bị qua các bước song song với mẫu phân tích.
Sự nhiễm bẩn do mang sang có thể xảy ra khi tiến hành phân tích liên tiếp mẫu có nồng độ cao và thấp. Để giảm việc bị nhiễm bẩn này, rửa thiết bị sục và xylanh bơm mẫu bằng nước thuốc thử giữa các lần làm mẫu. Để kiểm tra việc bị nhiễm bẩn do mang sang sau khi phân tích mẫu có nồng độ cao bất thường thì phải phân tích bằng mẫu trắng. Đối với các mẫu chứa lượng lớn các chất có thể hòa tan được trong nước, các chất rắn lơ lửng, các hợp chất có nhiệt độ sôi cao hay các hợp chất dễ bay hơi, rửa thiết bị sục bằng dung dịch tẩy rửa, tráng bằng nước cất và sấy khô ở nhiệt độ 105 oC giữa các lần phân tích. Bộ phận bẫy và các phần khác của hệ thống cũng dễ bị nhiễm bẩn, vì vậy, phải thường xuyên sấy và làm sạch toàn bộ hệ thống.
4. Giới hạn phát hiện
Giới hạn phát hiện của phương pháp (MDLs) phụ thuộc vào hợp chất và thay đổi theo hiệu quả sục và độ nhạy của thiết bị. Trong phòng thí nghiệm đơn lẻ sử dụng nước thuốc thử và nồng độ thêm vào đã biết là 0,5 ![]() , MDLs được quan sát nằm trong dải từ 0,025
, MDLs được quan sát nằm trong dải từ 0,025 ![]() đến 0,450
đến 0,450 ![]() . Khoảng hiệu chuẩn thích hợp đối với phương pháp này là phụ thuộc hợp chất và thiết bị, nhưng xấp xỉ 0,2
. Khoảng hiệu chuẩn thích hợp đối với phương pháp này là phụ thuộc hợp chất và thiết bị, nhưng xấp xỉ 0,2![]() đến 200
đến 200 ![]() . Các hợp chất được lấy ra từ nước không hoàn toàn sẽ không phát hiện được khi có nồng độ thấp. Tuy nhiên, chúng có thể được xác định bằng độ chệch và độ chụm chấp nhận nếu có nồng độ thích hợp. Việc xác định một số đồng phân hình học (ví dụ như các xylen) có thể gặp trở ngại do đồng rửa giải.
. Các hợp chất được lấy ra từ nước không hoàn toàn sẽ không phát hiện được khi có nồng độ thấp. Tuy nhiên, chúng có thể được xác định bằng độ chệch và độ chụm chấp nhận nếu có nồng độ thích hợp. Việc xác định một số đồng phân hình học (ví dụ như các xylen) có thể gặp trở ngại do đồng rửa giải.
5. An toàn
Độc tố hoặc chất gây ung thư của từng mẫu phân tích không được phân biệt cụ thể. Benzen, cacbon tetraclorua, bis(1-cloisopropyl)ete, 1-4-diclorobenzen, 1.2-dicloroetan, hexaclorobutadien, 1.1.2.2-tetracloroetan, 1.1.2-tricloroetan, cloroform, 1.2-dibromometan, tetracloroeten, tricloroeten và vinyl clorua được tạm thời phân loại như đã được biết hoặc nghi ngờ là các chất gây ung thư. Thao tác các vật liệu tiêu chuẩn tinh khiết và dung dịch tiêu chuẩn gốc của những hợp chất này trong tủ hút và đeo mặt nạ phòng hơi độc khi thao tác chất có nồng độ cao.
6. Thiết bị, dụng cụ
6.1. Hệ thống sục và bẫy
Hệ thống sục và bẫy bao gồm thiết bị sục, bẫy và giải hấp. Một số hệ thống hoàn chỉnh có sẵn trên thị trường.
6.1.1. Thiết bị sục, được thiết kế để có thể chứa được 25 ml mẫu và có chiều dài cột nước có ít nhất 5 cm. Thiết bị sục có dung tích nhỏ hơn 5 ml cũng có thể chấp nhận được nếu giới hạn phát hiện phương pháp và các tính năng được đáp ứng. Giữ tổng thể tích khoảng cách chứa khí giữa cột nước và bẫy nhỏ hơn 15 ml. Chuyển khí sục qua cột nước thành các bong bóng có đường kính nhỏ hơn 3 mm. Cho khí sục cách đáy cột nước nhỏ hơn 5 mm. Thiết bị sục được mô tả trong Hình 1.
Ống vẩy dạng kim có thể được sử dụng thay cho nguyên liệu thủy tinh như được chỉ trong Hình 1. Tuy nhiên, trong mỗi trường hợp, cho khí sục tại điểm cách đáy cột nước nhỏ hơn 5mm.
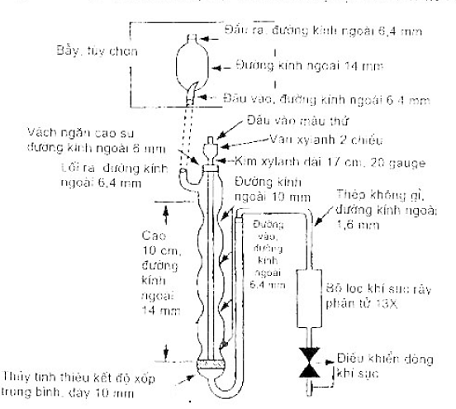
Hình 1 – Thiết bị sục
6.1.2. Thiết bị bẫy lọc, có chiều dài ít nhất 25 cm và có đường kính trong ít nhất 3 mm được nhồi chất hấp phụ với chiều dài tối thiểu: 1,0 cm silicon metyl, 7,7 cm 2,6 – diphenylen oxit polyme 7,7 cm silica gel và 7,7 cm than hoạt tính. Nếu không cần phân tích diclodifiorometan, có thể loại bỏ than hoạt tính và phần polyme được kéo dài tới 15 cm. Có thể sử dụng các chất hấp phụ khác miễn là đáp ứng được tất cả các tiêu chí kiểm soát chất lượng. Các bẫy bằng chất hấp phụ đa dạng có sẵn trên thị trường, nhưng bẫy phải đảm bảo giữ thể tích khi sục và thời gian sục không đổi (nghĩa là 40 ml/min và trong thời gian 11 min). Thao tác này phải đáp ứng được tất cả các tiêu chí về kiểm soát chất lượng. Các thông số tối thiểu của thiết bị được mô tả trong Hình 2.
Nên nhồi bằng metyl silicon, tuy nhiên không bắt buộc. Việc nhồi metyl silicon để bảo vệ các chất hấp phụ diphenylen oxit polyme khỏi các son khí, việc bao phủ lại bất cứ phần hoạt động nào có thể phát sinh trong quá trình gia nhiệt, phải đảm bảo các polyme được bao kín trong vùng gia nhiệt của bẫy do đó loại bỏ các điểm lạnh tiềm ẩn. Mặt khác, có thể sử dụng bông thủy tinh để tạo khoảng trống ở đầu vào của bẫy.
Trước khi sử dụng, ổn định bẫy qua đêm theo hướng dẫn của nhà sản xuất. Để bẫy thông thoáng không mở cột phân tích. Trước khi sử dụng hàng ngày, ổn định bẫy 10 min bằng tia nước. Tốt nhất, để bẫy thông thoáng đến cột phân tích trong suốt quá trình ổn định hàng ngày; tuy nhiên, chạy cột theo chương trình nhiệt độ trước khi phân tích mẫu.
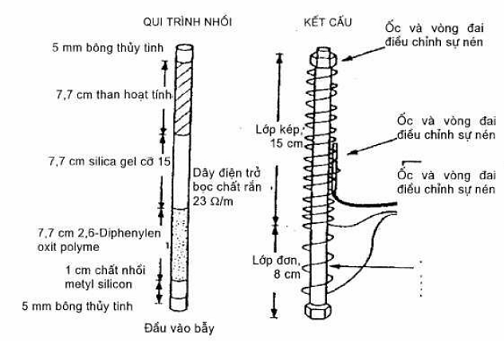
Hình 2 – Cách nhồi và cấu trúc bộ lọc để có khả năng giải hấp
6.2. Sắc ký khí (GC), sử dụng sắc ký khí chương trình nhiệt độ, thích hợp đối với việc bơm trên cột. Khử hoạt tính tất cả các bộ phận thủy tinh (ví dụ như ống dẫn) bằng chất silan.
6.3. Các cột sắc ký khí mao quản, sử dụng bất kỳ cột sắc ký khí mao quản nào đáp ứng tất cả các tính năng thực hiện. Đảm bảo tốc độ dòng giải hấp tương thích với cột lựa chọn. Bốn mẫu cột chấp nhận được liệt kê dưới đây:
1) Cột 1: cột VOCOL có chiều dài 60 m, đường kính trong 0,75 mm, cột mao quản rộng có độ dày của màng 1,5 ![]() .
.
2) Cột 2: cột DB 624 có chiều dài 30 m, đường kính trong 0,53 mm, cột mao quản đại có độ dày của màng 3 ![]() .
.
3) Cột 3: cột DB 5 có chiều dài 30 m, đường kính trong 0,32 mm, cột mao quản có độ dày của màng 1 ![]()
4) Cột 4: cột DB 624 có chiều dài 30 m, đường kính trong 0,25 mm, cột mao quản có độ dày của màng 1,4 ![]() .
.
6.4. Khối phổ kế, có thể quét từ 35 amu đến 300 amu trong 2 giây hoặc ít hơn, sử dụng nguồn năng lượng ion hóa 70 eV (danh định) trong quá trình ion hóa, và tạo ra phổ khối đáp ứng tất cả các tiêu chí trong Bảng 2 khi 25 ng hoặc ít hơn 4-bromoflorobenzen được cho các vào GC. Để đảm bảo độ chụm, tốc độ quét cho phép thu được ít nhất là 5 phổ cho một cấu tử mẫu rửa giá từ GC.
6.5. Thiết bị sục và bẫy – Kết nối GC/MS, sử dụng chia dòng hoặc bơm trực tiếp, phụ thuộc vào loại cột được sử dụng. Nếu dùng cột có đường kính trong nhỏ (cột 4) cần phải cô đặc mao quản trước khi tiến hành sắc ký khí. Kết nối này ngưng tụ các chất được giải hấp trên cột không phủ silica nóng chảy, và khi gia nhiệt gián đoạn thì nó chuyển các hợp chất lên cột mao quản. Phần không phủ của cột được làm lạnh xuống -150oC trong lúc giải hấp và nung nóng đến 250 oC để chuyển các chất ngưng tụ.
6.6. Hệ thống dữ liệu
Khối phổ kế có kết nối máy tính cho phép liên tục lưu trữ và thu nhận tất cả khối phổ nhận được trong suốt chương trình sắc ký. Phần mềm máy tính cho phép nghiên cứu tất cả các phổ thu được đối với m/z riêng (khối lượng) và biểu đồ phân bố m/z đối với thời gian hoặc số lần quét. Loại biểu đồ này là profile dòng ion được chiết suất (EICP). Phần mềm cũng cho phép tích phân đo phân bố trong EICP theo thời gian cụ thể hoặc giới hạn quét.
6.7. Xylanh, có dung tích 0,5 ml, 1,0 ml, 5 ml và 25 ml với đầu có thể tháo được.
6.8. Van xylanh, van hai chiều có đầu tháo được.
6.9. Microxylanh, dung tích 10 ![]() , 25
, 25![]() và 100
và 100![]() chiều dài 5 cm, đường kính trong 0,15 mm.
chiều dài 5 cm, đường kính trong 0,15 mm.
6.10. Bình, dung tích 40 ml có nút vặn bằng TFE.
Bảng 1 – Độ phân bố m/z BFB
|
Khối lượng |
Độ phân bố m/z |
|
50 |
15 % đến 40 % của khối lượng 05 |
|
75 |
30% đến 60% của khối lượng 95 |
|
95 |
Pic nền độ phân bố tương đối 100% |
|
96 |
5 % đến 9 % của khối lượng 95 |
|
173 |
< 2=”” %=”” của=”” khối=”” lượng=””> |
|
174 |
> 50 % của khối lượng 95 |
|
175 |
5% đến 9 % của khối lượng 174 |
|
176 |
95 % đến 101 % của khối lượng 174 |
|
177 |
5 % đến 9 % của khối lượng 170 |
7. Thuốc thử
7.1. Nước thuốc thử, không làm ảnh hưởng đến giới hạn phát hiện các thành phần cần xác định. Chuẩn bị bằng cách cho nước vòi đi qua nền lọc cacbon có chứa khoảng 0,5 kg cacbon hoạt tính, bằng chưng cất hoặc bằng cách sử dụng hệ thống làm tinh khiết nước1) 1)
7.2. Các vật liệu nhồi bẫy
7.2.1. 2,6-diphenylen oxit polyme, 60/80 mesh, cấp sắc ký.
7.2.2. Chất nhồi metyl silicon, 3 OV-1.
7.2.3. Silica gel, 35/60 mesh.
7.3. Metanol, loại chuyên dụng.
7.4. Axit clohydric HCl, 1:1.
7.5. Vinyl clorua, độ tinh khiết 99,9 %.
7.6. Axit ascorbic.
7.7. Dung dịch tiêu chuẩn gốc
Chuẩn bị từ các vật liệu tiêu chuẩn tinh khiết hoặc mua các dung dịch đã được chứng nhận. Chuẩn bị các dung dịch tiêu chuẩn gốc trong metanol bằng cách sử dụng các chất lỏng hoặc khí đã phân tích. Cảnh báo: Các chất độc hại. Xem điều 5.
Cho khoảng 9,8 ml metanol vào bình định mức có nút thủy tinh nhám. Để yên không đậy nút trong 10 min hoặc cho đến khi tất cả bề mặt dính cồn khô đi. Cân bình chính xác đến 0,1 mg.
Thêm các chất chuẩn đã phân tích như sau: đối với các chất lỏng, sử dụng xylanh dung tích 100 ![]() hoặc pipet thủy tinh đầu mao quản sử dụng một lần, ngay lập tức thêm hai giọt hoặc nhiều hơn các chất chuẩn đã phân tích vào bình định mức, sau đó cân lại. Đảm bảo các giọt nhỏ chính xác vào cồn mà không rơi vào cổ bình. Đối với khí halocacbon có nhiệt độ sôi dưới 30 oC (bromometan, cloroetan, clorometan, dicloroflorometan, tricloroflorometan, vinyl clorua), gắn ống nhựa vinyl vào đầu bình khí chứa chất chuẩn, với đầu mở sục khí vào cốc metanol chảy qua ống lắp xylanh có van kín khí dung tích 5 ml vào ống và từ từ hút khí vào trong xylanh đến vạch 5 ml. Hạ thấp xylanh xuống 5 mm bề mặt metanol và từ từ cho khí lên trên bề mặt. Khí sẽ hòa tan trong metanol và nhìn thấy như một xoáy nước khi nó hòa tan trong dung môi. Cân lại bình định mức (khác nhau là số lượng khí được hòa tan trong metanol), pha loãng đến thể tích, đóng nút lại và lắc đảo ngược nhiều lần. Tính nồng độ bằng
hoặc pipet thủy tinh đầu mao quản sử dụng một lần, ngay lập tức thêm hai giọt hoặc nhiều hơn các chất chuẩn đã phân tích vào bình định mức, sau đó cân lại. Đảm bảo các giọt nhỏ chính xác vào cồn mà không rơi vào cổ bình. Đối với khí halocacbon có nhiệt độ sôi dưới 30 oC (bromometan, cloroetan, clorometan, dicloroflorometan, tricloroflorometan, vinyl clorua), gắn ống nhựa vinyl vào đầu bình khí chứa chất chuẩn, với đầu mở sục khí vào cốc metanol chảy qua ống lắp xylanh có van kín khí dung tích 5 ml vào ống và từ từ hút khí vào trong xylanh đến vạch 5 ml. Hạ thấp xylanh xuống 5 mm bề mặt metanol và từ từ cho khí lên trên bề mặt. Khí sẽ hòa tan trong metanol và nhìn thấy như một xoáy nước khi nó hòa tan trong dung môi. Cân lại bình định mức (khác nhau là số lượng khí được hòa tan trong metanol), pha loãng đến thể tích, đóng nút lại và lắc đảo ngược nhiều lần. Tính nồng độ bằng ![]()
![]() từ khối lượng tịnh. Khi độ tinh khiết hợp chất được phân tích đạt 96 % hoặc lớn hơn, tính nồng độ của dung dịch tiêu chuẩn gốc từ khối lượng chưa hiệu chỉnh. Tốt nhất là sử dụng các dung dịch tiêu chuẩn gốc thương phẩm có nồng độ bất kỳ nếu chúng được chứng nhận bởi các nhà sản xuất. Cho dung dịch tiêu chuẩn gốc vào bình có nút vận TFE. Bảo quản bình tại nhiệt độ – 10 oC đến – 20 oC, tránh ánh sáng.
từ khối lượng tịnh. Khi độ tinh khiết hợp chất được phân tích đạt 96 % hoặc lớn hơn, tính nồng độ của dung dịch tiêu chuẩn gốc từ khối lượng chưa hiệu chỉnh. Tốt nhất là sử dụng các dung dịch tiêu chuẩn gốc thương phẩm có nồng độ bất kỳ nếu chúng được chứng nhận bởi các nhà sản xuất. Cho dung dịch tiêu chuẩn gốc vào bình có nút vận TFE. Bảo quản bình tại nhiệt độ – 10 oC đến – 20 oC, tránh ánh sáng.
7.8. Các dung dịch tiêu chuẩn pha loãng thứ cấp
Sử dụng các dung dịch tiêu chuẩn gốc, chuẩn bị trong metanol các dung dịch tiêu chuẩn pha loãng thứ cấp có chứa các hợp chất cần phân tích, hoặc đơn lẻ hoặc được trộn vào với nhau. Chuẩn bị các dung dịch tiêu chuẩn pha loãng thứ cấp tại các nồng độ cho phép các dung dịch tiêu chuẩn hiệu chuẩn (7.10) nằm trong dải làm việc của hệ thống phân tích. Bảo quản các dung dịch tiêu chuẩn pha loãng thứ cấp có khoảng cách chứa tối thiểu trong tủ lạnh và kiểm tra thường xuyên dấu hiệu bay hơi (điều này chỉ ra sự cần thiết đối với việc tái sinh). Luôn luôn để ở nhiệt độ phòng trước khi chuẩn bị các dung dịch tiêu chuẩn hiệu chuẩn. Đối với các chất khí các dung dịch tiêu chuẩn sử dụng được trong 1 tuần. Các dung dịch tiêu chuẩn khác sử dụng được trong 1 tháng hoặc ít hơn nếu so sánh với các dung dịch tiêu chuẩn kiểm tra thấy có vấn đề.
7.9. Dung dịch nội chuẩn/thay thế dung dịch tiêu chuẩn bổ sung đã biết
Chuẩn bị dung dịch có chứa florobenzen (nội chuẩn) và 1,2-diclobenzen-d4 (thay thế) trong metanol. Dung dịch nội chuẩn khác và các hợp chất thay thế có thể được sử dụng miễn là đáp ứng được phương pháp và không cản trở đến bất kỳ phương pháp phân tích nào. Chuẩn bị dung dịch tiêu chuẩn pha loãng thứ cấp có nồng độ 5 ![]() của từng hợp chất. Thêm 5,0
của từng hợp chất. Thêm 5,0 ![]() dung dịch tiêu chuẩn vào 25,0 ml mẫu hoặc dung dịch tiêu chuẩn hiệu chuẩn tạo ra nồng độ tương đương 1,0
dung dịch tiêu chuẩn vào 25,0 ml mẫu hoặc dung dịch tiêu chuẩn hiệu chuẩn tạo ra nồng độ tương đương 1,0 ![]() . Nồng độ tiêu chuẩn thứ cấp khác có thể được sử dụng nếu thể tích bổ sung được điều chỉnh phù hợp và đáp ứng được tất cả các tiêu chí dung dịch nội chuẩn. Thêm hỗn hợp này vào từng mẫu dung dịch tiêu chuẩn và mẫu trắng.
. Nồng độ tiêu chuẩn thứ cấp khác có thể được sử dụng nếu thể tích bổ sung được điều chỉnh phù hợp và đáp ứng được tất cả các tiêu chí dung dịch nội chuẩn. Thêm hỗn hợp này vào từng mẫu dung dịch tiêu chuẩn và mẫu trắng.
7.10. Dung dịch tiêu chuẩn hiệu chuẩn
Chuẩn bị ít nhất năm mức nồng độ cho từng hỗn hợp bằng cách thêm vào số lượng thích hợp dung dịch tiêu chuẩn thứ cấp vào nước thuốc thử và mẫu nước đảo ngược hai lần. Chuẩn bị một dung dịch tiêu chuẩn có nồng độ gần, nhưng cao hơn MDL (nghĩa là 4 x MDL đối với các mẫu loại nước có thể uống được) hoặc ở cấp độ được xác định là mức độ cuối thấp của dải làm việc và các loại khác tương ứng với dải mong muốn của nồng độ mẫu hoặc để xác định dải làm việc của detector. Các dung dịch tiêu chuẩn hiệu chuẩn có thể sử dụng được trong 24 h nếu được đựng trong lọ thủy tinh kín không có phần hở cho không khí trong lọ. Nếu không đạt, loại bỏ trong vòng 1h. Chuẩn bị các dung dịch tiêu chuẩn hiệu chuẩn bằng bơm, có rửa bằng dung môi, một lượng thích hợp của pha loãng hỗn hợp tiêu chuẩn và hỗn hợp nội chuẩn/hỗn hợp thay thế, đổ đầy nước thuốc thử trực tiếp vào xylanh dung tích 25 ml, bơm ngay lập tức dung dịch tiêu chuẩn nước vào bồn sục.
8. Cách tiến hành
8.1. Điều kiện tiến hành
Bảng 2 tóm tắt các điều kiện tiến hành được khuyến nghị đối với sắc ký và đưa ra thời gian lưu ước lượng và MDLs mà có thể đạt được ở những điều kiện này. Ví dụ sự tách thu được với cột cụ thể được thể hiện ở Hình 3. Có thể sử dụng các cột và điều kiện sắc ký khác nếu đáp ứng được các tiêu chí kiểm soát chất lượng.
8.2. Phép thử thực hiện GC/MS
Vào đầu buổi tiến hành phân tích, kiểm tra hệ thống GC/MS bằng cách thực hiện phép thử với BFB trước các mẫu bất kỳ, các mẫu thử trắng hoặc các dung dịch tiêu chuẩn được phân tích. Thực hiện các phép thử theo các thông số thiết bị sau:
Năng lượng ion hóa: 70 eV (danh định)
Dải khối lượng: 35 amu đến 300 amu
Thời gian quét: ít nhất 5 lần quét/pic nhưng không nhanh hơn 2 giây/ lần quét
Bơm 25 ng BFB trực tiếp vào cột GC. Nếu bơm trực tiếp không dễ thực hiện, thêm 1 ml dung dịch BFB 25 mg/ml vào 25 ml nước thuốc thử trong xylanh được sử dụng để chuyển mẫu sang thiết bị sục và phân tích mẫu. Nhận được phổ khối đã hiệu chỉnh nền của BFB và xác nhận rằng tất cả các tiêu chí m/z chính ở Bảng 1 đều đạt được. Nếu tất cả các tiêu chí không đạt được, thực hiện lại phép thử cho đến khi đạt được tất cả các tiêu chí.
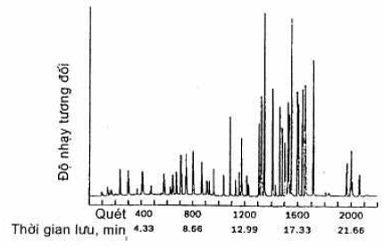
Hình 3 – Sắc đồ GC/MS
(Cột: J&W DB-624, dài 30 m, đường kính trong 0,25 mm, màng 1,4 ![]() ; chương trình nhiệt độ: 35 oC trong 4 min: 4oC/min; 50 oC, 0 min; 10 oC/min; 175 oC, 4 min)
; chương trình nhiệt độ: 35 oC trong 4 min: 4oC/min; 50 oC, 0 min; 10 oC/min; 175 oC, 4 min)
Bảng 2 – Ion định lượng cơ bản, thời gian lưu và giới hạn phát hiện phương pháp
|
Chất phân tích |
Thời gian lưu |
MDL |
m/z cơ bản |
|
Diclororociflorometan |
1,49 |
0,190 |
85 |
|
Clorometan |
1,71 |
0,150 |
50 |
|
Vinyl clorua |
1,79 |
0,120 |
62 |
|
Bromometan |
2,16 |
0,220 |
94 |
|
Cloroetan |
2,28 |
0,230 |
64 |
|
Tricloflorometan |
2,57 |
0,059 |
101 |
|
1,1-Dicloroetan |
3,22 |
0,130 |
96 |
|
1,1,2-Tricloro-1,2,2-trifloroetan |
3,25 |
0,065 |
101 |
|
Metylen clorua |
3,96 |
0,099 |
49 |
|
trans-1,2-Dicloroeten |
4,40 |
0,200 |
96 |
|
Metyl 1-butyl ete |
4,45 |
0,450 |
73 |
|
1,1-Dicloroetetan |
5,14 |
0,047 |
63 |
|
c/s-1,2-Dicloroeten |
6,30 |
0,130 |
96 |
|
2,2-Dicloropropan |
6,24 |
0,041 |
77 |
|
Bromoclorometan |
6,77 |
0,032 |
128 |
|
Cloroform |
7,00 |
0,126 |
83 |
|
1,1,1-Tricloroetan |
7,24 |
0,043 |
97 |
|
1,1-Dicloropropen |
7,67 |
0,040 |
75 |
|
Cacbon tetraclorua |
7,65 |
0,042 |
117 |
|
Benzen |
8,07 |
0,036 |
78 |
|
1,2-Dicloroetan |
8,14 |
0,055 |
62 |
|
Tricloroeten |
9,44 |
0,045 |
95 |
|
1,2-Dicloropropan |
9,85 |
0,053 |
63 |
|
Dibromometan |
10,07 |
0,035 |
93 |
|
Bromodiclorometan |
10,47 |
0,112 |
83 |
|
cis-1,3-Dicloropren |
11,29 |
0,048 |
75 |
|
Toluen |
11,81 |
0,047 |
91 |
|
trans-1,3-Dicloropren |
12,27 |
0,051 |
75 |
|
1,1,2-Tricloroetan |
12,56 |
0,043 |
83 |
|
1,3-Dicloropropan |
12,83 |
0,090 |
76 |
|
Tetracloroeten |
12,77 |
0,047 |
166 |
|
Dibromocloroetan |
13,24 |
0,133 |
129 |
|
1,2-Dibromoetan |
13,25 |
0,133 |
107 |
|
Clorobenzen |
14,21 |
0,052 |
112 |
|
1,1,1,2-Tetracloroetan |
14,37 |
0,048 |
131 |
|
Etylbenzen |
14,42 |
0,032 |
91 |
|
m,p-Xylen |
14,63 |
0,038 |
91 |
|
o-Xylen |
16,27 |
0,038 |
91 |
|
Styten |
15,30 |
0,031 |
104 |
|
Bromofoc |
15,60 |
0,131 |
173 |
|
Isopropylbenzen |
15,90 |
0,074 |
105 |
|
Bromobenzen |
16,34 |
0,140 |
156 |
|
1,1,2,2-Tetracloroetan |
16,41 |
0,066 |
83 |
|
1,2,3-Tricloropropan |
16,44 |
0,072 |
75 |
|
n-Propylbenzen |
16,57 |
0,260 |
91 |
|
2-Clorotoluen |
16,68 |
0,042 |
126 |
|
4-Clorotoluen |
16,86 |
0,040 |
126 |
|
1,3,5-Trimetylbenzen |
16,88 |
0,035 |
105 |
|
tert-Butylbenzen |
17,38 |
0,100 |
119 |
|
sec-Butylbenzen |
17,46 |
0,025 |
105 |
|
1,2,4-Trimetylbenzen |
17,74 |
0,046 |
105 |
|
4-isopropyltoluen |
17,99 |
0,037 |
119 |
|
1,3-Diclorobenzen |
17,89 |
0,045 |
146 |
|
1,4-Diclorobenzen |
18,04 |
0,033 |
146 |
|
1,2-Diclorobenzen |
18,64 |
0,031 |
146 |
|
n-Butylbenzen |
18,65 |
0,028 |
91 |
|
Hexaclorobutadien |
21,69 |
0,033 |
225 |
|
1,2,4-Triclorobenzen |
21,34 |
0,043 |
180 |
|
Naphtalen |
21,80 |
0,049 |
128 |
|
1,2,3-Triclorobenzen |
22,32 |
0,047 |
180 |
8.3. Hiệu chuẩn, hiệu chuẩn hệ thống như sau:
8.3.1. Thiết lập hệ thống – trước tiên ổn định bẫy lọc qua đêm ở 180 oC bằng cách phun rửa với khí trơ ở tốc độ 20 ml/min. Hàng ngày ổn định bẫy trong 10 min theo nhiệt độ yêu cầu của nhà sản xuất. Nối hệ thống sục và bẫy với GC sử dụng chương trình nhiệt độ đã khuyến nghị và các điều kiện tốc độ dòng. Hiệu chuẩn hệ thống theo phương pháp nội chuẩn hoặc ngoại chuẩn.
8.3.2. Hiệu chuẩn theo phương pháp nội chuẩn – chọn một hoặc nhiều các dung dịch nội chuẩn tương tự trong phân tích đối với các hợp chất cần phân tích. Nên sử dụng florobenzen làm chất nội chuẩn. Phép xác định bằng dung dịch nội chuẩn không bị ảnh hưởng bởi phương pháp hoặc nền cản trở. Do những hạn chế này, không một dung dịch nội chuẩn nào có thể được áp dụng đối với tất cả các mẫu. Các hợp chất được sử dụng như chất thay thế (ví dụ 1,2-diclobenzen-d4) để kiểm soát chất lượng có thể được sử dụng thành công như là các dung dịch nội chuẩn. Chuẩn bị các dung dịch tiêu chuẩn hiệu chuẩn tối thiểu ở năm nồng độ đối với từng hợp chất được miêu tả trong 7.10. Chuẩn bị dung dịch tiêu chuẩn pha loãng thứ cấp chứa từng dung dịch nội chuẩn (7.9). Phân tích từng dung dịch tiêu chuẩn hiệu chuẩn theo qui trình đối với mẫu, thêm dung dịch nội chuẩn trực tiếp vào xylanh. Lập bảng độ cao pic hoặc diện tích pic theo nồng độ đối với từng hợp chất và dung dịch nội chuẩn, và tính hệ số hiệu chỉnh (RF) đối với từng hợp chất như sau:
RF = ![]()
Trong đó:
As – là giá trị diện tích pic của hợp chất được đo;
Ais – là giá trị diện tích pic của dung dịch nội chuẩn;
Cis – là nồng độ của dung dịch nội chuẩn;
Cs – là nồng độ của hợp chất được đo
Giá trị trung bình của RF có thể được sử dụng nếu độ lệch chuẩn tương đối RSD nhỏ hơn 20 %.
8.3.3. Hiệu chuẩn theo phương pháp ngoại chuẩn – chuẩn bị các dung dịch tiêu chuẩn như trong 7.10. Phân tích từng dung dịch hiệu chuẩn và lập bảng diện tích pic ứng với nồng độ. Chuẩn bị đường chuẩn đối với từng hợp chất. Nếu tỷ lệ của giá trị diện tích pic với nồng độ (hệ số hiệu chuẩn) là một hằng số trên toàn dải làm việc (< 20=”” %=”” rsd),=”” có=”” thể=”” giả=”” thiết=”” đường=”” thẳng=”” của=”” góc=”” và=”” sử=”” dụng=”” hệ=”” số=”” hiệu=”” chuẩn=”” trung=”” bình=”” thay=”” cho=”” đường=””>
8.3.4. Kiểm tra hiệu chuẩn
Hiệu chuẩn liên tục là sự phân tích định kỳ dung dịch hiệu chuẩn đã sử dụng để kiểm tra độ nhạy của thiết bị không được thay đổi đáng kể từ hiệu chuẩn ban đầu. Đối với phép phân tích GC cứ 10 mẫu thực hiện một phép hiệu chuẩn liên tục; đối với phép phân tích GC/MS, cứ 20 mẫu thực hiện một phép hiệu chuẩn liên tục, hoặc sau 12 h. Thực hiện hiệu chuẩn liên tục với một hoặc nhiều nồng độ dung dịch tiêu chuẩn phân tích trong hiệu chuẩn ban đầu. Thay đổi nồng độ thực của dung dịch tiêu chuẩn hiệu chuẩn liên tục trên dải hiệu chuẩn, bằng nồng độ nhỏ nhất lớn hơn hai lần giới hạn báo cáo. Tiêu chuẩn chấp nhận đối với hiệu chuẩn liên tục là hiệu suất thu hồi 70 % đến 100 % so với giá trị đã biết hoặc mong đợi của dung dịch tiêu chuẩn hiệu chuẩn (sự thận trọng của thí nghiệm viên, tiêu chuẩn chấp nhận đối với các chất khí có thể được mở rộng từ hiệu suất thu hồi 60% đến 140 %). Nếu tiêu chuẩn chấp nhận không đáp ứng được, phân tích lại dung dịch tiêu chuẩn hiệu chuẩn liên tục hoặc lặp lại hiệu chuẩn ban đầu. Nếu sử dụng hệ số hiệu chuẩn, kiểm tra tính năng và độ nhạy của thiết bị đối với chất cần phân tích đưa vào các giá trị chấp nhận nhỏ nhất đối với các hệ số hiệu chỉnh.
8.4. Phân tích mẫu
Để mẫu đến nhiệt độ phòng. Tháo pittông của xylanh dung tích 25 ml và đóng van lại. Mở chai mẫu và rót cẩn thận mẫu vào ống xylanh để tránh bị tràn. Thay pittông xylanh, xoay ngược xylanh và mở van. Cho không khí thoát ra ngoài và điều chỉnh thể tích mẫu tới 25.0 ml, nhân đôi nếu có đủ mẫu (nắp mẫu đã được loại bỏ, mẫu không thể được lưu giữ do có khoảng không). Thêm một lượng thích hợp dung dịch thay thế/nội chuẩn qua miệng van và đóng van. Lắp vào thiết bị sục, mở van và bơm mẫu vào bồn sục. Đóng van và sục mẫu trong 11 min ở nhiệt độ phòng với tốc độ dòng 40 ml/min (heli hoặc nitơ). Nếu hơi nước gây ra ảnh hưởng đối với khối phổ kế, sử dụng sục khô 3 min và/hoặc mô đun kiểm soát độ ẩm.
Giải hấp các chất bị bẫy ở trên đầu của cột sắc ký ở 180 oC trong 4 min trong khi phun rửa bẫy bằng khí trơ ở tốc độ dòng tương thích với cột lựa chọn và bắt đầu chương trình nhiệt độ GC
Cài đặt hệ thống tự xả để khoang sục trống rỗng trong khi bẫy đang được giải hấp trong GC hoặc cách khác sử dụng xylanh mẫu để hút hết không khí trong bình. Rửa khoang bằng hai lần 25 ml nước thuốc thử nếu các mẫu bị nhiễm bẩn cao đang được phân tích. Đảm bảo tất cả các vùng bị ướt trong lúc sục cũng phải ướt trong lúc rửa để tối đa việc rửa.
Ổn định lại bẫy bằng cách sấy ở nhiệt độ ổn định từ 5 min đến 7 min. Để bẫy nguội đến nhiệt độ môi trường trước khi tiến hành mẫu tiếp theo trong bồn sục. Khi tất cả các hợp chất mẫu đã được rửa giải từ cột sắc ký, kết thúc việc thu thập dữ liệu và lưu trữ dữ liệu trong file. Sử dụng phần mềm hệ thống dữ liệu để thể hiện dải phổ khối và profile ion chiết thích hợp (EICP). Nếu độ phân bố ion bất kỳ vượt quá dải làm việc của hệ thống, pha loãng mẫu trong xylanh thứ hai bằng nước thuốc thử và phân tích.
CHÚ THÍCH: Cẩn thận với mẫu vi các hợp chất dễ bay hơi và có thể bị thất thoát nếu mẫu bị mở lại.
Ước tính lượng pha loãng cần thiết và loại bỏ mẫu thừa từ xylanh thứ hai, bơm phần đó vào bồn sục và bằng xylanh thứ hai, thêm lượng nước thuốc thử cần thiết để đạt được tổng 25 ml trong bồn sục.
9. Biểu thị kết quả
Khi các hợp chất đã được xác định, định lượng cơ sở trên dải phân bố nguyên từ EICP của các đặc tính cơ bản m/z được cho trong Bảng 2. Nếu mẫu sinh ra cản trở đối với m/z cơ bản, tính toán hệ số hiệu chỉnh hoặc đường chuẩn sử dụng đặc tính thứ cấp m/z, và sử dụng m/z thứ cấp để định lượng. Báo cáo kết quả bằng ![]() . Báo cáo tất cả dữ liệu kiểm soát chất lượng bằng các kết quả mẫu.
. Báo cáo tất cả dữ liệu kiểm soát chất lượng bằng các kết quả mẫu.
10. Độ chụm và độ chệch
Dữ liệu độ chụm và độ chệch điển hình của một phòng thử nghiệm được thể hiện trong Bảng 3.
Bảng 3 –Dữ liệu độ chụm và độ chệch của một phòng thử nghiệm trong nước thuốc thử*
|
Chất phân tích |
Phần trăm thu hồi |
Độ lệch chuẩn
|
Độ lệch chuẩn tương đối |
|
Benzen |
107 |
0,046 |
9 |
|
Bromobenzen |
111 |
0,034 |
6 |
|
Bromoclorometan |
88 |
0,052 |
12 |
|
Bromodiclorometan |
104 |
0,036 |
7 |
|
Bromoform |
107 |
0,042 |
8 |
|
Bromometan |
89 |
0,049 |
11 |
|
n-Butylbenzen |
115 |
0,048 |
8 |
|
sec-Butylbenzen |
113 |
0,043 |
8 |
|
tert-Butylbenzen |
116 |
0,057 |
10 |
|
Cacbon tetraclorua |
119 |
0,048 |
8 |
|
Clorobenzen |
108 |
0,033 |
6 |
|
Cloroetan |
115 |
0,073 |
13 |
|
Clorolorm |
108 |
0,043 |
8 |
|
Clorometan |
74 |
0,036 |
10 |
|
2-Clorotoluen |
111 |
0,045 |
8 |
|
4-Clorotoluen |
112 |
0,049 |
9 |
|
Dibromocloroetan |
108 |
0,042 |
8 |
|
1,2-Dibromoetan |
102 |
0,042 |
8 |
|
Dibromometan |
132 |
0,113 |
17 |
|
1,2-Diclorobenzen |
106 |
0,043 |
8 |
|
1,3-Diclorobenzen |
108 |
0,052 |
10 |
|
1,4-Diclorobenzen |
106 |
0,045 |
8 |
|
Diclored florometan |
80 |
0,058 |
15 |
|
1,1-Dicloroetan |
109 |
0,049 |
9 |
|
1,2-Dicloroetan |
102 |
0,031 |
6 |
|
1,1-Dicloroeten |
99 |
0,059 |
12 |
|
cis-1,2-Dicloroeten |
103 |
0,062 |
12 |
|
trans-1,2-Dicloroeten |
113 |
0,045 |
8 |
|
1,2-Dicloropropan |
129 |
0,064 |
10 |
|
1,3-Dicloropropan |
107 |
0,046 |
9 |
|
2,2-Dicloropropan |
106 |
0,049 |
9 |
|
1,1-Dicloropropen |
110 |
0,044 |
8 |
|
cis-Dicloropropen |
99 |
0,044 |
9 |
|
trans-1,3-Dicloropropen |
101 |
0,038 |
7 |
|
Etylbenzen |
109 |
0,049 |
9 |
|
Hexaciorobutadien |
112 |
0,053 |
9 |
|
Isopropylbenzen |
112 |
0,044 |
8 |
|
4-isopropyltoluen |
117 |
0,046 |
8 |
|
Metylen clorua |
85 |
0,050 |
12 |
|
Metyl-butyl ete |
81 |
0,017 |
11 |
|
Naphtalen |
121 |
0,068 |
11 |
|
n-Propylbenzen |
107 |
0,048 |
9 |
|
Styren |
101 |
0,039 |
8 |
|
1,1,1,2-Tetracloroetan |
113 |
0,037 |
7 |
|
1,1,2,2-Tetracloroetan |
104 |
0,053 |
10 |
|
Tetracloroeten |
106 |
0,046 |
9 |
|
Toluen |
106 |
0,045 |
8 |
|
1,2,3-Triclorobenzen |
118 |
0,054 |
9 |
|
1,2,4-Triclorobenzen |
109 |
0,049 |
9 |
|
1,1,1-Tricloroetan |
106 |
0,040 |
8 |
|
1,1,2-Tricloroetan |
97 |
0,041 |
9 |
|
Tricloroeten |
105 |
0,041 |
8 |
|
Tricloroflorometan |
105 |
0,045 |
9 |
|
1,2,3-Tricloropropan |
104 |
0,034 |
6 |
|
1,1,2-Tricloro-1,2,2-trifloroetan |
113 |
0,042 |
7 |
|
1,2,4-Trimetylbenzen |
116 |
0,044 |
8 |
|
1,3,5-Trimetylbenzen |
110 |
0,051 |
9 |
|
Vinyl clorua |
85 |
0,037 |
9 |
|
m,p-Xylen |
110 |
0,057 |
10 |
|
o-Xylen |
106 |
0,044 |
8 |
|
* Đối với tất cả các chất phân tích, bảy mẫu được phân tích, mỗi mẫu có nồng độ 0,5 |
|||
1) Millipore super Q hoặc tương đương


