Nội dung toàn văn Tiêu chuẩn Việt Nam TCVN 8557:2010 về phân bón – Phương pháp xác định nitơ tổng số
TIÊU CHUẨN VIỆT NAM
TCVN 8557:2010
PHÂN BÓN – PHƯƠNG PHÁP XÁC ĐỊNH NITƠ TỔNG SỐ
Fertilizers – Method for determination of total nitrogen
Lời nói đầu
TCVN 8557:2010 được chuyển đổi từ 10 TCN 304-2004 theo quy định tại khoản 1 Điều 69 của Luật Tiêu chuẩn và Quy chuẩn kỹ thuật và điểm a khoản 1 Điều 6 Nghị định số 127/2007/NĐ-CP ngày 1/8/2007 của Chính phủ quy định chi tiết thi hành một số điều của Luật Tiêu chuẩn và Quy chuẩn kỹ thuật.
TCVN 8557:2010 do Viện Thổ nhưỡng Nông hóa biên soạn, Bộ Nông nghiệp và Phát triển nông thôn đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
PHÂN BÓN – PHƯƠNG PHÁP XÁC ĐỊNH NITƠ TỔNG SỐ
Fertilizers – Method for determination of total nitrogen
1. Phạm vi áp dụng
Tiêu chuẩn này áp dụng cho các loại phân bón có chứa nitơ dạng khoáng và dạng hữu cơ (phân khoáng đơn, khoáng phức hợp, khoáng hỗn hợp, phân hữu cơ, hữu cơ vi sinh, hữu cơ sinh học, hữu cơ khoáng, than bùn) theo phương pháp Kieldhal.
Tiêu chuẩn này không áp dụng cho các loại phân bón chứa nitrat.
2. Tài liệu viện dẫn
TCVN 4851-89 (ISO 3696-87), Nước dùng cho phân tích trong phòng thí nghiệm – Yêu cầu kỹ thuật.
3. Phân loại
Phân bón chứa nitơ có thể chia thành hai nhóm:
3.1. Nhóm một: Bao gồm các loại phân bón chứa nitơ ở dạng khoáng như phân khoáng đơn (urê, amôn sunphát), phân khoáng phức hợp (MAP- monoammonium phosphate, DAP- diammonium phosphate) và phân khoáng hỗn hợp (NK, NPL, NP, NPKS …).
3.2. Nhóm hai: Bao gồm các loại phân bón có chứa nitơ ở cả dạng hữu cơ và dạng khoáng (phân hữu cơ, hữu cơ sinh học, hữu cơ vi sinh, hữu cơ khoáng).
4. Nguyên tắc
Chuyển hóa các hợp chất nitơ trong mẫu thành amoni (NH4+) bằng H2SO4 (với nhóm 1) và hỗn hợp giữa H2SO4 với chất xúc tác (với nhóm 2), sau đó cất amoni nhờ dung dịch kiểm, thu NH3 bằng dung dịch axit boric, chuẩn độ amon tetraborat bằng axit tiêu chuẩn, từ đó suy ra hàm lượng nitơ trong mẫu.
5. Thuốc thử
Hóa chất sử dụng để pha các chất chuẩn đạt loại tinh khiết hóa học, hóa chất sử dụng để phân tích đạt loại tinh khiết phân tích.
5.1. Nước cất, TCVN 4851 – 89.
5.2. Axit sunfuric (H2SO4) d = 1,84, không có amoni.
5.3. Dung dịch tiêu chuẩn HCl hoặc H2SO4, nồng độ 0,1; 0,2; 0,5 N pha từ ống tiêu chuẩn.
5.4. Dung dịch NaOH, nồng độ 40%:
Cân 400 g NaOH vào cốc dung tích 1000 ml, thêm 400 ml nước, khuấy tan, chuyển vào bình định mức 1000 ml, thêm nước đến vạch định mức. Để yên dung dịch hai ngày cho lắng hết cặn cacbonat, sử dụng phần dung dịch trong. Bảo quản dung dịch trong bình nhựa kín.
5.5. Dung dịch axit boric (HBO3), nồng độ 5%:
Cân 50 g axit boric vào cốc dung tích 1000 ml, thêm 900 ml nước nóng, khuấy tan, để nguội, thêm 20 ml dung dịch chỉ thị màu hỗn hợp, trộn đều; sau đó nhỏ từng giọt dung dịch NaOH 0,1 M cho đến khi toàn bộ dung dịch có màu đỏ tía nhạt (pH khoảng 5), chuyển vào bình định mức dung tích 1000 ml, thêm nước đến vạch định mức, lắc trộn đều, dung dịch được chuẩn bị trước khi sử dụng. Bảo quản kín ở 20 oC trong lọ màu nâu.
5.6. Hỗn hợp xúc tác K2SO4 và Se:
Nghiền nhỏ từng loại 100 g K2SO4 và 1 g Se, trộn đều, nghiền lại một lần nữa, đựng trong lọ khô.
5.7. Dung dịch chỉ thị màu hỗn hợp bromocresol xanh – metyl đỏ:
Cân 0,1 g bromocresol xanh lục và 0,7 g metyl đỏ hòa tan trong 100 ml etanol 95%. Bảo quản kín ở 20 oC trong lọ màu nâu.
CHÚ THÍCH:
1) Có thể sử dụng hỗn hợp metyl xanh và metyl đỏ thay thế hỗn hợp bromocresol xanh – metyl đỏ: Hòa tan 0,05 g metyl xanh vào 5 ml nước cất, thêm vào đó 100 ml etanol 95% và hòa tan thêm 0,15 g metyl đỏ, khuấy cho tan hết, bảo quản kín ở 20 oC trong lọ màu nâu;
2) Có thể pha riêng dung dịch axit boric, khi sử dụng cứ 50 ml axit boric cần cho thêm 10 giọt hỗn hợp chỉ thị màu, sau đó nhỏ từng giọt dung dịch NaOH 0,1M cho đến khi dung dịch có màu đỏ tía nhạt (pH khoảng 5);
5.8. Dung dịch tiêu chuẩn amoni có nồng độ 0,05 mg N/ml:
Cân 0,2360 g (NH4)2SO4 (TKHH đã sấy ở 100 oC trong 2 h, để trong bình hút ẩm) vào cốc dung tích 1000 ml, thêm 400 ml nước, khuấy tan, chuyển vào bình định mức dung tích 1000 ml, thêm nước tới vạch định mức, lắc đều, dung dịch thu được có nồng độ 0,05 mg N/ml, bảo quản kín ở 20 oC.
6. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ thông thường trong phòng thí nghiệm và các thiết bị, dụng cụ như sau:
6.1. Bình phân hủy mẫu, dung tích 250 ml.
6.2. Bếp phân hủy mẫu, điều khiển được nhiệt độ.
6.3. Thiết bị chưng cất Kjeldhal, dung tích 250 ml (xem sơ đồ ở phần phụ lục A) gồm các phần chính:
6.3.1. Bình cất Kjeldhal, dung tích 250 ml (Nếu đun trực tiếp sử dụng bình đáy cầu dung tích 1000 ml).
6.3.2. Đầu tránh bắn, có đầu vào đầu ra và nối với phễu nhỏ giọt.
6.3.3. Phễu nhỏ giọt có khóa.
6.3.4. Ống sinh hàn.
6.3.5. Bình hứng, dung tích 250 ml (hoặc 500 ml).
6.4. Cân phân tích, độ chính xác 0,0002 g.
6.5. Rây, có đường kính lỗ 2 mm.
6.6. Buret, dung tích 50 ml, độ chính xác 0,1 ml.
6.7. Bình định mức, dung tích 100; 200; 1000 ml.
7. Lấy mẫu và chuẩn bị mẫu
7.1. Mẫu đem đến phòng thí nghiệm được đảo trộn đều, trải phẳng trên khay nhựa hoặc tấm nilông, lấy mẫu trung bình theo phương pháp đường chéo góc, trộn đều, lấy hai phần đối diện và loại bỏ dần cho đến khi còn khoảng 500 g;
7.2. Chia mẫu trung bình thành hai phần bằng nhau, cho vào hai túi PE buộc kín, ghi mã số phân tích, ngày, tháng, tên mẫu (và các thông tin cần thiết khác), một phần làm mẫu lưu, một phần làm mẫu phân tích, thời gian lưu mẫu không quá 6 tháng.
7.3. Nghiền mịn mẫu rồi qua rây có đường kính lỗ 2 mm, trộn đều làm mẫu phân tích.
7.4. Mẫu có ẩm độ cao có thể cân một lượng mẫu xác định, sấy khô ở nhiệt độ 70 oC, xác định độ ẩm, nghiền mịn mẫu khô qua rây 2 mm làm mẫu phân tích. Lưu ý khi tính kết quả phải nhân với hệ số chuyển đổi từ khối lượng mẫu khô sang khối lượng mẫu thực tế ban đầu.
7.5. Các mẫu không thể xử lý theo (7.3) và (7.4) có thể lấy một lượng mẫu khoảng 20 g, nghiền thật mịn làm mẫu phân tích.
8. Cách tiến hành
8.1. Lắp đặt, kiểm tra thiết bị chưng cất Kjeldhal:
8.1.1. Tùy theo thực tế của mỗi thiết bị mà cách lắp đặt có thể khác nhau, nhưng phải tuyệt đối kín trong suốt quá trình hoạt động, có khả năng điều chỉnh được tốc độ cất và tốc độ ngưng.
8.1.2. Trước khi cất mẫu phải kiểm tra thiết bị Kjeldhal bằng cách cất 14 ml dung dịch tiêu chuẩn amoni 0,05 mg N/ml với kiềm. Chuẩn độ lượng nitơ trong bình hứng hết 5 ml ± 0,1 ml dung dịch tiêu chuẩn 0,01 N HCl là đạt yêu cầu, nếu ít hơn là do thiết bị cất bị hở, nếu lớn hơn có thể là do bị bắn kiềm từ bình cất hoặc do thiết bị không sạch, cần khắc phục.
8.2. Phân hủy mẫu
Phân hủy với hai nhóm mẫu khác nhau (xem 3).
8.2.1. Sử dụng H2SO4 để phân hủy mẫu nhóm một:
8.2.1.1. Cân 2g ± 0,001g mẫu đã được chuẩn bị theo (7.3) hay (7.4) và (7.5) cho vào bình phân hủy (không để dính mẫu ở cổ và thành bình).
8.2.1.2. Thêm 10 ml nước.
8.2.1.3. Thêm 10 ml H2SO4 đậm đặc d = 1,84.
8.2.1.4. Chuẩn bị đồng thời hai mẫu trắng không có mẫu thử, tiến hành đồng nhất điều kiện như mẫu thử.
8.2.1.5. Đun nóng từ từ trên bếp cho đến khi hết sủi bọt (có thể cho thêm một chút parafin để giảm bớt bọt, tránh trào).
8.2.1.6. Tăng dần nhiệt độ tới 200 oC đun sôi nhẹ đến khi khói trắng bay lên (khoảng 60 min). Tiếp tục đun thêm 30 min, không để khô.
8.2.1.7. Để nguội, thêm từ từ 50 ml nước, đun sôi 10 min.
8.2.1.8. Chuyển dung dịch và cặn trong bình phân hủy sang bình định mức dung tích 200 ml, thêm nước cất đến vạch định mức, lắc đều, lọc hoặc để lắng. Đây là dung dịch A để xác định nitơ tổng số.
8.2.2. Sử dụng H2SO4 và xúc tác để phân hủy mẫu nhóm hai:
8.2.2.1. Cân 2 g ± 0,001 g mẫu đã được xử lý theo (7.3) hay (7.4) và (7.5) cho vào bình phân hủy (không để dính mẫu ở cổ và thành bình).
8.2.2.2. Thêm 1 g hỗn hợp xúc tác K2SO4 và Se, thêm 25 ml H2SO4 đặc.
8.2.2.3. Chuẩn bị đồng hời hai mẫu trắng không có mẫu thử, tiến hành đồng nhất điều kiện như mẫu thử trên bếp cho đến khi hết sủi bọt (có thể cho thêm một chút parafim để giảm bớt bọt, tránh trào).
8.2.2.4. Tăng dần nhiệt độ lên 200 oC khoảng 120 min, có khói trắng bay lên.
8.2.2.5. Tiếp tục tăng dần nhiệt độ lên 350 oC trong khoảng 60 min đến khi dung dịch mẫu trắng trong là được, không để khô.
8.2.2.6. Để nguội, thêm từ từ 50 ml nước cất, đun sôi 10 min.
8.2.2.7. Chuyển sang bình định mức dung tích 200 ml, thêm nước cất đến vạch định mức, lắc đều, lọc hoặc để lắng trong. Gọi đâh là dung dịch A để xác định nitơ tổng số.
8.3. Chưng cất amomi (NH3)
8.3.1. Bình hứng dung tích 250 ml.
8.3.1.1. Lấy vào bình hứng một lượng dung dịch axit boric đã có hỗn hợp chỉ thị màu, lượng axit boric lấy phụ thuộc lượng nitơ trong bình cất (phải đảm bảo 1 mg nitơ ít nhất 0,5 ml dung dịch axit boric bão hòa).
8.3.1.2. Đặt bình hứng dưới ống sinh hàn (nhúng đuôi ống sinh hàn vào dung dịch axit boric khoảng 2 mm);
8.3.1.3. Lựa chọn lượng axit boric và nồng độ axit tiêu chuẩn thích hợp phù hợp với lượng nitơ có trong bình cất theo bảng 1.
Bảng 1 – Hướng dẫn lựa chọn lượng axit boric và nồng độ axit tiêu chuẩn
|
Dự kiến lượng nitơ có trong bình cất |
Lượng axit boric tối thiểu, ml |
Nồng độ HCl tiêu chuẩn, N |
|
Dưới 30 mg N |
15 |
0,1 hoặc 0,2 |
|
Từ 30 mg đến 50 mg N |
25 |
0,2 hoặc 0,5 |
|
Từ 50 mg đến 100 mg N |
50 |
0,2 hoặc 0,5 |
|
Từ 100 mg đến 200 mg N |
100 |
0,5 |
8.3.2. Bình cất dung tích 250 ml (nếu đun trực tiếp sử dụng bình cầu dung tích 1000 ml).
8.3.2.1. Chuyển vào bình cất một lượng dung dịch A sau phân hủy có chứa khoảng 30 mg N đến 200 mg N tráng phễu và dụng cụ đong bằng nước cất, dồn vào bình cất.
8.3.2.2. Cho hệ thống làm lạnh hoạt động.
8.3.2.3. Cho 50 ml dung dịch NaOH 40% qua phễu nhỏ rọt vào bình cất, giữ lại 1 ml trên phễu sau đó dùng khoảng 50 ml nước cất tráng phẫu, và chuyển nước tráng vào bình cất giữ lại trên phễu 1 ml, khóa phễu và cho nước cất 1/2 phễu.
8.3.4. Tiến hành cất amoni, điều chỉnh tốc độ sôi và tốc độ ngưng lạnh để nhiệt độ nước sau khi ngưng khoảng 35 oC.
8.3.5. Kết thúc quá trình cất khi hết amoni (khi dung dịch ngưng khoảng 150 ml với lượng nitơ trong bình cất có dưới 100 mg N và 200 ml với lượng nitơ trong bình cất có nhiều hơn 100 mg N). Thử bằng thuốc thử Nessler.
8.3.6. Hạ thấp bình hứng, tia rửa đuôi ống sinh hàn vào bình hứng, để nguội.
8.4. Chuẩn độ
8.4.1. Chuẩn độ amontetaborat bằng dung dịch axit tiêu chuẩn HCl hoặc H2SO4, lắc liên tục cho đến khi chuyển màu đột ngột.
8.4.2. Nếu chỉ thị là hỗn hợp bromocresol xanh-metyl đỏ thì màu của dung dịch chuyển từ xanh sang tía nhạt. Nếu chỉ thị hỗn hợp metyl xanh-metyl đỏ thì màu của dung dịch chuyển từ xanh lục sang tím đỏ.
CHÚ Ý: Quá trình phân hủy mẫu phải theo dõi thường xuyên, đặc biệt ở giai đoạn đầu, không để trào bắn mẫu ra ngoài, không để khô mẫu (luôn luôn dư axit ít nhất 2 ml, nếu thiếu phải cho thêm axit)
9. Tính kết quả
9.1. Hàm lượng nitơ % N theo phần trăm khối lượng được tính theo công thức:
![]()
Trong đó:
a Thể tích dung dịch axit tiêu chuẩn tiêu tốn quá trình chuẩn độ mẫu thử tính bằng mililit (ml);
b Thể tích dung dịch axit tiêu chuẩn tiêu tốn trong quá trình chuẩn độ mẫu trắng tính bằng mililit (ml);
N Nồng độ đương lượng axit tiêu chuẩn (N);
0,01401 mili đương lượng gam của nitơ (g);
m Khối lượng mẫu tương ứng với thể tích dịch trích chưng cất tính bằng gam (g).
9.2. Kết quả phép thử là giá trị trung bình các kết quả của ít nhất hai lần thử được tiến hành song song. Nếu sai lệch giữa các lần thử lớn hơn 5% so với giá trị trung bình của phép thử thì phải tiến hành lại.
7. Báo cáo thử nghiệm
Báo cáo thử nghiệm cần bao gồm những thông tin sau:
a) Viện dẫn tiêu chuẩn này;
b) Đặc điểm nhận dạng mẫu;
c) Kết quả xác định nitơ tổng số;
d) Những chi tiết không quy định trong tiêu chuẩn này hoặc những điều được coi là tùy chọn và các yếu tố có thể ảnh hưởng đến kết quả thử nghiệm.
PHỤ LỤC A
(Tham khảo)
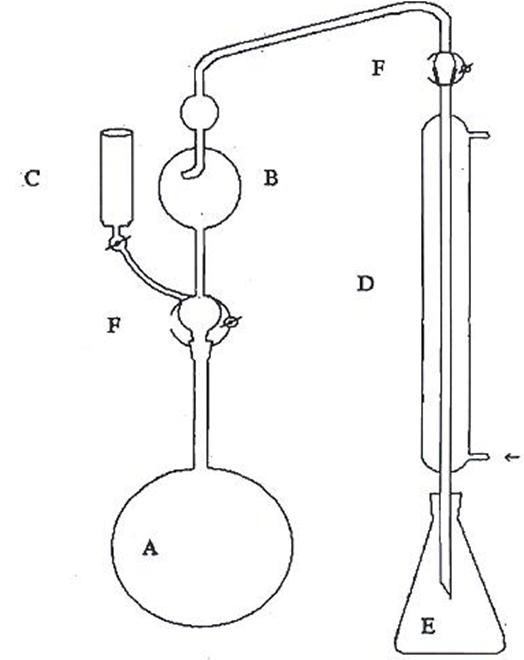
Hình A1. Sơ đồ thiết bị Kjeldhal
CHÚ DẪN:
A. Bình cất Kjeldhal
B. Đầu tránh bắn
C. Phễu nhỏ giọt, khóa
D. ống sinh hàn
E. Bình hứng
F. Kẹp


