Nội dung toàn văn Tiêu chuẩn Việt Nam TCVN 8686-2:2011 về thuốc thú y – Phần 2: Canxi gluconat, vitamin B12 và vitamin B1 dạng tiêm
TIÊU CHUẨN VIỆT NAM
TCVN 8686-2:2011
THUỐC THÚ Y – PHẦN 2: CANXI GLUCONAT, VITAMIN B12 VÀ VITAMIN B1 DẠNG TIÊM
Veterinary drugs – Part 2: Injectable calcium gluconat, vitamin B12 and vitamin B1
1. Phạm vi áp dụng
Tiêu chuẩn này áp dụng cho thuốc canxi gluconat, vitamin B12 và vitamin B1 dạng tiêm dùng trong thú y.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
Dược điển Việt Nam IV trang 116, 608, 204.
3. Yêu cầu kỹ thuật
3.1 Công thức pha chế
Canxi gluconat 10,00 g
Vitamin B12 0,01 g
Vitamin B1 0,50 g
Nước cất vừa đủ 100 ml
3.2 Nguyên liệu
Canxi gluconat Theo tiêu chuẩn của nhà sản xuất.
Vitamin B12 Theo tiêu chuẩn của nhà sản xuất.
Vitamin B1 Theo tiêu chuẩn của nhà sản xuất.
Nước cất Đạt tiêu chuẩn Dược điển Việt Nam IV.
3.3 Chất lượng thành phẩm
3.3.1 Yêu cầu cảm quan
|
Chỉ tiêu |
Yêu cầu |
|
Màu sắc |
Màu đỏ |
|
Trạng thái |
Dung dịch trong suốt |
3.3.2 Yêu cầu về lý-hóa
|
Chỉ tiêu |
Yêu cầu |
|
Độ pH |
Từ 4 đến 6 |
|
Hàm lượng |
100 % (± 10 %) |
4. Lấy mẫu
4.1 Nguyên tắc chung lấy mẫu
Lấy mẫu theo nguyên tắc ngẫu nhiên.
Lượng thuốc trong mẫu phân tích cũng như trong mẫu lưu ít nhất phải đủ cho ba lần phân tích hoặc phải đủ để thực hiện các phép thử đảm bảo thu được kết quả chính xác và tin cậy. Lượng thuốc này được tính toán trên cơ sở tiêu chuẩn phương pháp thử của sản phẩm. Bình thường mỗi lô sản xuất được lấy hai mẫu (một mẫu phân tích và một mẫu lưu).
Trường hợp đặc biệt, số mẫu phân tích và mẫu lưu có thể nhiều hơn hai để đủ gửi kiểm nghiệm và lưu ở nhiều nơi nếu xét thấy cần thiết.
4.2 Lấy mẫu thành phẩm
Mẫu được lấy tại những vị trí khác nhau của lô sản xuất, không được phá lẻ các đơn vị đóng gói sản phẩm để lấy mẫu. Từ các đơn vị lấy mẫu được tập hợp lại thành mẫu chung và mẫu cuối cùng.
Số lượng mẫu thành phẩm cần lấy được qui định cụ thể dưới đây:
|
Quy cách đóng gói (g hoặc ml) |
Số lượng mẫu lấy (đơn vị bao gói) |
|
Cho tới 2 |
70 |
|
Từ 2 đến dưới 5 |
30 |
|
Từ 5 đến dưới 50 |
7 |
|
Từ 50 đến dưới 100 |
4 |
|
Từ 100 trở lên |
3 |
Trong trường hợp đặc biệt thì tùy theo quy cách đóng gói và tính chất của thuốc chỉ lấy mẫu đủ để phân tích và lưu.
5. Phương pháp thử
5.1 Kiểm tra cảm quan
Tiến hành kiểm tra cảm quan bằng mắt thường.
5.2 Phương pháp xác định độ pH
Độ pH của dung dịch được đo bằng máy đo pH.
5.3 Phương pháp xác định hàm lượng hoạt chất chính
5.3.1 Thuốc thử
5.3.1.1 Metanol (tinh khiết sắc ký).
5.3.1.2 Natri heptan sulfonat (C7H15NaO3S).
5.3.1.3 Kali clorit (KCl).
5.3.1.4 Axit axetic băng (CH3COOH).
5.3.1.5 Nước cất.
5.3.1.6 Dung dịch kali ferocyanid (K4Fe(CN)6.3H2O).
5.3.1.7 Amoni clorit (NH4Cl).
5.3.1.8 Dung dịch amoni oxalat 4 % ((COONH4)2.H2O).
5.3.1.9 Axit clohydric (HCl).
5.3.1.10 Polyetylen glycol.
5.3.1.11 Dung dịch trilon B 0,05 M.
5.3.1.12 Hỗn hợp chỉ thị calcon: nghiền trộn 0,1g calcon với 9,9 g natri sulfonat (Na2SO4) khan.
5.3.1.13 Dung dịch natri hidroxit (NaOH) 10 M.
5.3.2 Thiết bị, dụng cụ
5.3.2.1 Máy sắc ký lỏng hiệu năng cao (HPLC-UV-vis).
5.3.2.2 Cột Lichrosorb RP 8 (250 x 4,6 mm; 10 mm).
5.3.2.3 Cột Lichrosorb RP 18 (250 x 4,6 mm; 10 mm)
5.3.2.4 Máy đo pH.
5.3.2.5 Máy lắc siêu âm.
5.3.2.6 Giấy lọc, cỡ lỗ 0,45 mm.
5.3.2.7 Cân phân tích, có thể chính xác đến 0,1 mg.
5.3.2.8 Bình định mức, dung tích 20 ml, 25 ml, 50 ml và 1000 ml.
5.3.2.9 Bình nón, dung tích 500 ml.
5.3.2.10 Pipet, dung tích 2 ml, 3 ml, 5 ml và 10 ml.
5.3.3 Phương pháp xác định
5.3.3.1 Phương pháp định tính
5.3.3.1.1 Phương pháp định tính B1 và B12
Thời gian lưu của vitamin B12 và vitamin B1 trùng với thời gian lưu của vitamin B12 và vitamin B1 chuẩn.
5.3.3.1.2 Phương pháp định tính canxi gluconat
Mẫu thuốc cho phản ứng của ion canxi (Lấy 0,2 ml thuốc, thêm 5 ml dung dịch axit axetic 5 M, 0,5 ml dung dịch kali ferocyanid, thêm khoảng 0,05 g amoni clorit tạo thành kết tủa màu trắng).
Lấy 5 ml thuốc, thêm vài giọt dung dịch amoni oxalat 4 %, tạo thành kết tủa màu trắng (kết tủa này ít tan trong axit axetic 6 M nhưng tan trong axit clohydric)
5.3.3.2 Phương pháp định lượng
5.3.3.2.1 Định lượng vitamin B1
5.3.3.2.1.1 Chuẩn bị pha động
– Natri heptan sulfonat 1,08 g
– Kali clorit 2,0 g
– Polyetylen glycol 400 2,0 ml
– Axit axetic băng 10 ml
– Metanol 130 ml
– Nước cất vừa đủ 1 000 ml
Trộn đều, lọc qua giấy lọc có kích thước lỗ lọc 0,45 mm, loại khí bằng cách siêu âm 15 min.
5.3.3.2.1.2 Điều kiện sắc ký
– Cột Lichrosorb RP 8 (250 x 4,6 mm; 10 mm).
– Detector UV-vis bước sóng 280 nm.
– Tốc độ dòng: 2 ml/min.
– Thể tích bơm: 20 ml.
5.3.3.2.1.3 Dung dịch chuẩn
Cân 0,05 g vitamin B1 chuẩn, hoà tan vừa đủ trong 50 ml axit axetic 1,3 % lắc đều. Lấy 5 ml dung dịch này pha loãng với axit axetic 1,3 % vừa đủ 50 ml, lọc qua giấy lọc 0,45 mm.
5.3.3.2.1.4 Dung dịch thử
Lấy 1 ml thuốc cho vào bình định mức 50 ml, hòa tan vừa đủ bằng axit axetic 1,3 % lắc đều, lọc qua giấy lọc 0,45 mm.
Tiến hành đo riêng mẫu chuẩn và mẫu thử trên máy HPLC, ghi diện tích mẫu chuẩn và mẫu thử
5.3.3.2.1.5 Tính kết quả
Dựa vào diện tích pic chuẩn và pic thử để tính kết quả, theo công thức sau:
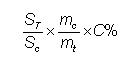
Trong đó:
ST là diện tích pic của mẫu thử;
SC là diện tích pic của mẫu chuẩn;
mc là khối lượng của chất chuẩn, tính bằng gam (g);
mt là khối lượng aspirin hoặc axit ascorbic trong mẫu thử, tính bằng gam (g);
C% là hàm lượng chất chuẩn.
5.3.3.2.2 Định lượng vitamin B12
5.3.3.2.2.1 Điều kiện sắc ký
– Cột Lichrosorb RP 18 (250 x 4,6 mm; 10 mm)
– Detector UV-vis bước sóng 550 nm
– Tốc độ dòng: 1 ml/ min
– Thể tích bơm: 20 ml
– Pha động: trộn methanol/nước với tỷ lệ 35 : 65 (phần thể tích)
5.3.3.2.2.2 Dung dịch mẫu chuẩn
Cân 0,05 g vitamin B12 chuẩn, hoà tan vừa đủ trong 50 ml nước cất, lắc đều. Lấy 2 ml dung dịch này pha loãng với nước cất vừa đủ 50 ml, lọc qua giấy lọc 0,45 mm.
5.3.3.2.2.3 Dung dịch thử
Lấy 10 ml dung dịch thuốc cho vào bình định mức 25 ml, làm vừa đủ bằng nước cất, lắc đều, lọc qua giấy lọc 0,45 mm.
Tiến hành đo riêng mẫu chuẩn và mẫu thử trên máy HPLC, ghi diện tích mẫu chuẩn và mẫu thử.
5.3.3.2.2.4 Tính kết quả
Dựa vào diện tích pic chuẩn và pic thử để tính hàm lượng chất chính theo công thức sau:
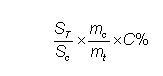
Trong đó:
ST là diện tích pic của mẫu thử.
SC là diện tích pic của mẫu chuẩn.
mc là khối lượng chất chuẩn, tính bằng gam (g);
mt là khối lượng chất cần thử, tính bằng gam (g);
C% là hàm lượng chất chuẩn.
5.3.3.2.3 Định lượng canxi gluconat bằng phương pháp chuẩn độ Complexon
Lấy 3 ml thuốc cho vào bình nón 500 ml.
Thêm 300 ml nước cất, 6 ml dung dịch natri hydroxit 10 M và khoảng 0,05 g hỗn hợp chỉ thị calcon.
Chuẩn độ bằng dung dịch trilon B 0,05 M đến khi dung dịch chuyển từ màu tím sang màu xanh hoàn toàn.
1 ml dung dịch trilon B 0,05 M tương ứng với 0,02242 g canxi gluconat.
6. Bao gói, bảo quản và vận chuyển
Thuốc được đóng trong chai, lọ kín để nơi khô mát, tránh ánh sáng.


