Nội dung toàn văn Tiêu chuẩn quốc gia TCVN 9482:2012 về Thuốc bảo vệ thực vật chứa hoạt chất Tebuconazole – Yêu cầu kỹ thuật và phương pháp thử
TIÊU CHUẨN QUỐC GIA
TCVN 9482 : 2012
THUỐC BẢO VỆ THỰC VẬT CHỨA HOẠT CHẤT TEBUCONAZOLE – YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ
Pesticides containing tebuconazole – Technical requirements and test methods
Lời nói đầu
TCVN 9482 : 2012 do Cục Bảo vệ Thực vật – Bộ Nông nghiệp và Phát triển nông thôn biên soạn, Bộ Nông nghiệp và Phát triển nông thôn đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
THUỐC BẢO VỆ THỰC VẬT CHỨA HOẠT CHẤT TEBUCONAZOLE – YÊU CẦU KỸ THUẬT VÀ PHƯƠNG PHÁP THỬ
Pesticides containing tebuconazole – Technical requirements and test methods
1. Phạm vi áp dụng
Tiêu chuẩn này quy định yêu cầu kỹ thuật và phương pháp thử đối với tebuconazole kỹ thuật và các sản phẩm thuốc bảo vệ thực vật có chứa hoạt chất tebuconazole. (xem giới thiệu hoạt chất – Phụ lục A).
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau là rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi.
TCVN 2741, Thuốc trừ sâu – Basudin 10 % dạng hạt;
TCVN 2744-86, Thuốc trừ dịch hại – Phương pháp xác định hàm lượng nước
TCVN 4851 : 1989 (ISO 3696 : 1987), Nước dùng để phân tích trong phòng thí nghiệm – Yêu cầu kỹ thuật và phương pháp thử;
TCVN 8050 : 2009, Thành phẩm thuốc bảo vệ thực vật – Phương pháp xác định tính chất lý hóa;
TCVN 8143 : 2009, Thuốc bảo vệ thực vật – Xác định hàm lượng hoạt chất cypermethrin;
TCVN 8382 : 2010 Thuốc bảo vệ thực vật chứa hoạt chất dimethoate – Yêu cầu kỹ thuật và phương pháp thử.
3. Yêu cầu kỹ thuật
3.1. Yêu cầu cảm quan
Yêu cầu về cảm quan của tebuconazole kỹ thuật và các dạng sản phẩm được nêu trong Bảng 1.
Bảng 1 – Yêu cầu cảm quan
|
Dạng sản phẩm |
Màu sắc |
Trạng thái |
|
Tebuconazole kỹ thuật (Technical material – TC) |
Sản phẩm không màu hoặc màu trắng |
Sản phẩm có dạng bột kết tinh |
|
Thuốc bảo vệ thực vật dạng nhũ tương – dầu trong nước có chứa tebuconazole (Emulsion oil in water – EW) |
Đặc trưng của từng sản phẩm |
Sản phẩm dạng lỏng không đồng nhất, gồm dung dịch thuốc trừ dịch hại trong dung môi hữu cơ, được phân tán thành giọt nhỏ khi pha với nước |
|
Thuốc bảo vệ thực vật dạng hạt phân tán trong nước có chứa tebuconazole (Water dispersible granule – WG) |
Đặc trưng của từng sản phẩm |
Sản phẩm dạng hạt, khô, rời, không bụi, khi hòa vào nước có thể phân tán đều trong nước |
|
Thuốc bảo vệ thực vật dạng bột thấm nước có chứa tebuconazole (Wettable powder – WP) |
Đặc trưng của từng sản phẩm |
Sản phẩm dạng bột mịn đồng nhất |
|
Thuốc bảo vệ thực vật dạng huyền phù có chứa tebuconazole (Aqueous suspension concentrate – SC) |
Đặc trưng của từng sản phẩm |
Dạng dung dịch treo của các hạt mịn phân tán trong nước. Sau khi khuấy nhẹ, sản phẩm phải đồng nhất và dễ dàng hòa loãng với nước |
|
Thuốc bảo vệ thực vật dạng nhũ dầu có chứa tebuconazole (Emulsifiabe concentrate – EC) |
Đặc trưng của từng sản phẩm |
Sản phẩm dạng lỏng đồng nhất, bền vững, trong suốt, không lắng cặn, tạo nhũ tương khi hòa vào nước |
3.2. Yêu cầu về hàm lượng hoạt chất
3.2.1. Tebuconazole kỹ thuật
Hàm lượng tebuconazole (tính theo %, g/kg) phải được công bố và khi xác định, hàm lượng trung bình không được nhỏ hơn mức hàm lượng tối thiểu đã công bố.
3.2.2. Tebuconazole thành phẩm
Hàm lượng tebuconazole (tính theo %, g/kg hoặc g/l ở 20 oC ± 2 oC) phải được công bố và phù hợp với mức sai lệch cho phép của hàm lượng hoạt chất được quy định trong Bảng 2.
Bảng 2 – Hàm lượng tebuconazole trong các dạng thành phẩm
|
Hàm lượng hoạt chất công bố (ở 20 oC ± 2 oC) |
Mức sai lệch cho phép |
|
|
% |
g/kg hoặc g/l |
|
|
Đến 2,5 |
Đến 25 |
± 15 % của hàm lượng công bố đối với dạng đồng nhất (EC, SC, …) hoặc ± 25 % đối với dạng không đồng nhất (WP, WG,…) |
|
Từ trên 2,5 đến 10 |
Từ trên 25 đến 100 |
± 10 % của hàm lượng công bố |
|
Từ trên 10 đến 25 |
Từ trên 100 đến 250 |
± 6 % của hàm lượng công bố |
|
Từ trên 25 đến 50 |
Từ trên 250 đến 500 |
± 5 % của hàm lượng công bố |
|
Lớn hơn 50 |
– |
± 2,5 % |
|
– |
Lớn hơn 500 |
± 25 g/kg hoặc g/l |
3.3. Yêu cầu về hàm lượng tạp chất
3.3.1. Hàm lượng tạp chất trong tebuconazole kỹ thuật
Nước: Không lớn hơn 5,0 g/kg
3.3.2. Hàm lượng tạp chất trong tebuconazole dạng bột thấm nước và hạt phân tán trong nước
Nước: không lớn hơn 25 g/kg
3.4. Yêu cầu về tính chất lý – hóa
3.4.1. Tebuconazole kỹ thuật
Độ axít hoặc kiềm
Không lớn hơn 1,0 g/kg, tính theo H2SO4
Không lớn hơn 6,0 g/kg, tính theo NaOH
3.4.2. Thuốc bảo vệ thực vật dạng nhũ tương-dầu trong nước có chứa tebuconazole
3.4.2.1. pH (dung dịch 1% trong nước cất) 6,0 – 9,0
3.4.2.2. Độ bền nhũ tương
Sản phẩm sau khi pha loãng với nước cứng chuẩn ở 30 oC ± 2 oC, phải phù hợp với quy định trong Bảng 3.
Bảng 3 – Độ bền nhũ tương của thuốc bảo vệ thực vật dạng nhũ tương – dầu trong nước có chứa tebuconazole
|
Chỉ tiêu |
Yêu cầu |
|
Độ tự nhũ ban đầu |
Hoàn toàn |
|
Độ bền nhũ tương sau khi pha mẫu 0,5 h: – thể tích lớp kem, không lớn hơn |
0 ml |
|
Độ bền nhũ tương sau khi pha mẫu 2 h: – thể tích lớp kem, không lớn hơn – thể tích lớp dầu, không lớn hơn |
1 ml 0 ml |
|
Độ tái nhũ sau khi pha mẫu 24h a) |
Hoàn toàn |
|
Độ bền nhũ tương cuối cùng sau khi pha mẫu 24,5 h a) – thể tích lớp kem, không lớn hơn – thể tích lớp dầu, không lớn hơn |
0 ml 0 ml |
|
a) Chỉ xác định khi có nghi ngờ kết quả xác định độ bền nhũ tương sau khi pha mẫu 2 h. |
|
3.4.2.3. Độ bền bảo quản
3.4.2.3.1. Độ bền ở 0 oC
Sản phẩm sau khi bảo quản ở nhiệt độ 0 oC ± 2 oC trong 7 ngày, có thể tích chất rắn hoặc lỏng tách lớp không lớn hơn 0,3 ml.
3.4.2.3.2. Độ bền ở nhiệt độ cao
Sản phẩm sau khi bảo quản ở nhiệt độ 54 oC ± 2 oC trong 14 ngày có hàm lượng hoạt chất xác định được theo 4.2 không nhỏ hơn 97 % so với trước khi bảo quản và phù hợp với quy định trong mục 3.4.2.2.
3.4.3. Thuốc bảo vệ thực vật dạng hạt phân tán trong nước có chứa tebuconazole
3.4.3.1. pH (hỗn hợp 1% trong nước cất) 6,0 – 9,0
3.4.3.2. Tỷ suất lơ lửng
Sau khi tạo huyền phù của sản phẩm trong nước cứng chuẩn ở 30 oC ± 2 oC trong 30 min, hàm lượng tebuconazole trong dung dịch huyền phù: không nhỏ hơn 60 %
3.4.3.3. Độ mịn
Lượng cặn còn lại trên rây có đường kính lỗ 75 mm sau khi thử rây ướt: Không lớn hơn 1 %
3.4.3.4. Độ thấm ướt
Không khuấy trộn, sản phẩm phải thấm ướt hoàn toàn trong 1 min
3.4.3.5. Độ tạo bọt
Lượng bọt tạo thành sau 1 min: Không lớn hơn 10 ml
3.4.3.6. Độ bền bảo quản ở nhiệt độ cao
Sản phẩm sau khi bảo quản ở nhiệt độ 54 oC ± 2 oC trong 14 ngày có hàm lượng hoạt chất xác định được theo 4.2 không nhỏ hơn 97 % so với trước khi bảo quản và phù hợp với quy định trong mục 3.4.3.1; 3.4.3.2; 3.4.3.3; 3.4.3.4.
3.4.4. Thuốc bảo vệ thực vật dạng bột thấm nước có chứa tebuconazole
3.4.4.1. pH (hỗn hợp 1% trong nước cất) 7,0 – 9,5
3.4.4.2. Tỷ suất lơ lửng
Sau khi tạo huyền phù của sản phẩm trong nước cứng chuẩn ở 30 oC ± 2 oC trong 30 min, hàm lượng tebuconazole trong dung dịch huyền phù: không nhỏ hơn 60 %
3.4.4.3. Độ mịn
Lượng cặn còn lại trên rây có đường kính lỗ 75 mm sau khi thử rây ướt: Không lớn hơn 2 %
3.4.4.4. Độ thấm ướt
Không khuấy trộn, sản phẩm phải thấm ướt hoàn toàn trong 1 min
3.4.4.5. Độ tạo bọt
Lượng bọt tạo thành sau 1 min: Không lớn hơn 20 ml
3.4.4.6. Độ bền bảo quản ở nhiệt độ cao
Sản phẩm sau khi bảo quản ở nhiệt độ 54 oC ± 2 oC trong 14 ngày có hàm lượng hoạt chất xác định được theo 4.2 không nhỏ hơn 97 % so với trước khi bảo quản và phù hợp với quy định trong mục 3.4.4.1; 3.4.4.2; 3.4.4.3; 3.4.4.4.
3.4.5. Thuốc bảo vệ thực vật dạng huyền phù có chứa tebuconazole
3.4.5.1. Độ pH (hỗn hợp 1% trong nước cất) 8,0 – 10,0
3.4.5.2. Tỷ suất lơ lửng
Sau khi tạo huyền phù của sản phẩm trong nước cứng chuẩn ở 30 oC ± 2 oC trong 30 phút, hàm lượng tebuconazole trong dung dịch huyền phù: không nhỏ hơn 60 %
3.4.5.3. Độ mịn
Lượng cặn còn lại trên rây có đường kính lỗ 75 mm sau khi thử rây ướt: không lớn hơn 1 %
3.4.5.4. Độ tạo bọt
Lượng bọt tạo thành sau 1 min: không lớn hơn 40 ml
3.4.5.5. Độ bền bảo quản
3.4.5.5.1. Độ bền ở 0 oC
Sản phẩm sau khi bảo quản ở nhiệt độ 0 oC ± 2 oC trong 7 ngày sản phẩm phải phù hợp với quy định trong mục 3.4.5.2; 3.4.5.3
3.4.5.5.2. Độ bền ở nhiệt độ cao
Sản phẩm sau khi bảo quản ở nhiệt độ 54 oC ± 2 oC trong 14 ngày có hàm lượng hoạt chất xác định được theo 4.2 không nhỏ hơn 97 % so với trước khi bảo quản và phù hợp với quy định trong mục 3.4.5.2; 3.4.5.3.
3.4.6. Thuốc bảo vệ thực vật dạng nhũ dầu có chứa tebuconazole
3.4.6.1. Độ bền nhũ tương
Sản phẩm sau khi pha loãng với nước cứng chuẩn ở 30 oC ± 2 oC, phải phù hợp với quy định trong Bảng 2.
Bảng 2 – Độ bền nhũ tương của thuốc bảo vệ thực vật dạng nhũ dầu có chứa tebuconazole
|
Chỉ tiêu |
Yêu cầu |
|
Độ tự nhũ ban đầu |
Hoàn toàn |
|
Độ bền nhũ tương sau khi pha mẫu 0,5 h: – thể tích lớp kem, không lớn hơn |
2 ml |
|
Độ bền nhũ tương sau khi pha mẫu 2 h: – thể tích lớp kem, không lớn hơn |
4 ml |
|
Độ tái nhũ sau khi pha mẫu 24 h a) |
Hoàn toàn |
|
Độ bền nhũ tương cuối cùng sau khi pha mẫu 24,5 h a) – thể tích lớp kem, không lớn hơn |
4 ml |
|
a) Chỉ xác định khi có nghi ngờ kết quả xác định độ bền nhũ tương sau khi pha mẫu 2 h. |
|
3.4.6.2. Độ bền bảo quản
3.4.6.2.1. Độ bền ở 0 oC
Sản phẩm sau khi bảo quản ở nhiệt độ 0 oC ± 2 oC trong 7 ngày, có thể tích chất rắn hoặc lỏng tách lớp không lớn hơn 0,3 ml
3.4.6.2.2. Độ bền ở nhiệt độ cao
Sản phẩm sau khi bảo quản ở nhiệt độ 54 oC ± 2 oC trong 14 ngày có hàm lượng hoạt chất xác định được theo 4.2 không nhỏ hơn 97 % so với trước khi bảo quản và phù hợp với quy định trong mục 3.4.6.1
4. Phương pháp thử
4.1. Lấy mẫu
Lấy mẫu theo phụ lục A của tiêu chuẩn TCVN 8143:2009
4.2. Xác định hàm lượng hoạt chất
4.2.1. Nguyên tắc
Hàm lượng tebuconazole được xác định bằng phương pháp sắc ký khí, với detector ion hóa ngọn lửa (FID). Dùng Etofenprox (EFP) làm chất nội chuẩn.
4.2.2. Thuốc thử
Chỉ sử dụng các thuốc thử tinh khiết phân tích, nước ít nhất đạt tiêu chuẩn loại 3 của TCVN 4851 (ISO 3696 trừ khi có quy định khác)
4.2.2.1. Chất chuẩn tebuconazole, đã biết hàm lượng.
4.2.2.2. Chất nội chuẩn etofenprox (EFP), 99 %.
4.2.2.3. Axetone, dùng cho sắc ký khí.
4.2.2.4. Khí nitơ, có độ tinh khiết không nhỏ hơn 99,9%.
4.2.2.5. Khí hydro, có độ tinh khiết không nhỏ hơn 99,9%.
4.2.2.6. Không khí nén, dùng cho máy sắc ký khí.
4.2.2.7. Dung dịch nội chuẩn, nồng độ 12,0 mg/ml.
Dùng cân phân tích (4.2.3.4) cân 1,20 g chất nội chuẩn EFP (4.2.2.2) chính xác tới 0,0001 g vào bình định mức 100 ml (4.2.3.1), hòa tan và định mức tới vạch bằng axetone (4.2.2.3).
4.2.2.8. Dung dịch chuẩn làm việc
Dùng cân phân tích (4.2.3.4) cân 0,12 g chất chuẩn tebuconazole (4.2.2.1), chính xác tới 0,0001 g vào bình định mức 100 ml (4.2.3.1), dùng pipet (4.2.3.2) thêm chính xác 10 ml dung dịch nội chuẩn (4.2.2.7), hòa tan và định mức đến vạch bằng axetone (4.2.2.3).
CHÚ THÍCH: Chất chuẩn chuẩn bảo quản trong tủ lạnh phải được đưa về nhiệt độ phòng trước khi cân.
4.2.3. Dụng cụ, thiết bị
Sử dụng các thiết bị, dụng cụ thông thường của phòng thử nghiệm và cụ thể như sau:
4.2.3.1. Bình định mức, dung tích 10; 100 ml.
4.2.3.2. Pipet, dung tích 1;10 ml
4.2.3.3. Xylanh bơm mẫu, dung tích 10 ml, chia vạch đến 1 ml.
4.2.3.4. Cân phân tích, có độ chính xác đến 0,0001 g.
4.2.3.5. Màng lọc, có cỡ lỗ 0,45 mm.
4.2.3.6. Đĩa bay hơi.
4.2.3.7. Máy sấy chân không.
4.2.3.8. Thiết bị sắc ký khí, được trang bị như sau:
– detector ion hóa ngọn lửa (FID);
– injector chia dòng và không chia dòng;
– cột mao quản ZB-50, có chiều dài 30 m, đường kính trong 0,32 mm, chiều dày pha tĩnh 0,25 mm hoặc loại tương đương;
– bộ bơm mẫu tự động hoặc bơm mẫu bằng tay;
– Máy tích phân kế hoặc máy vi tính.
4.2.3.9. Máy lắc siêu âm
4.2.4. Cách tiến hành
4.2.4.1. Chuẩn bị mẫu
Mẫu cần được làm đồng nhất trước khi cân: đối với mẫu dạng lỏng phải lắc đều, nếu bị đông đặc do nhiệt độ thấp cần được làm tan chảy ở nhiệt độ thích hợp; đối với mẫu dạng bột, hạt phải được trộn đều.
4.2.4.2. Chuẩn bị dung dịch mẫu thử
Dùng cân phân tích (4.2.3.4) cân mẫu thử có chứa khoảng 0,12 g hoạt chất tebuconazole vào bình định mức 100 ml (4.2.3.1), dùng pipet (4.2.3.2) thêm chính xác 10 ml dung dịch nội chuẩn (4.2.2.7), định mức đến vạch bằng axetone (4.2.2.3), đặt vào máy lắc siêu âm (4.2.3.9) trong 10 min để hòa tan mẫu. Lọc dung dịch qua màng lọc 0,45 mm (4.2.3.5) trước khi bơm vào máy (nếu cần).
4.2.4.3. Điều kiện phân tích
– chương trình nhiệt độ cột:
Nhiệt độ đầu: 1700C
Nhiệt độ cuối: 3100C
Tốc độ tăng nhiệt độ: 300C/min
Thời gian giữ nhiệt độ đầu: 0,5 min
Thời gian giữ nhiệt độ cuối: 5 min
– nhiệt độ buồng bơm mẫu: 250 oC
– nhiệt độ detector: 300 oC
– khí mang nitơ: 1,8 ml/min
– khí hydro: 25 ml/min
– khí nén: 250 ml/min
– khí nitơ bổ trợ cho detector: 30 ml/min
– thể tích bơm mẫu: 1 ml
– tỷ lệ chia dòng: 40 : 1.
4.2.4.4. Xác định
Bơm dung dịch mẫu chuẩn cho đến khi tỷ số của số đo diện tích của pic mẫu chuẩn và pic nội chuẩn thay đổi không lớn hơn 1 %. Sau đó, bơm lần lượt dung dịch chuẩn làm việc (4.2.2.8) và dung dịch mẫu thử (4.2.5.2), lặp lại 2 lần (tỷ số của số đo diện tích của pic mẫu chuẩn với pic nội chuẩn thay đổi không lớn hơn 1 % so với giá trị ban đầu).
4.2.4.5. Tính kết quả
Hàm lượng hoạt chất tebuconazole trong mẫu, X, biểu thị bằng phần trăm (%) được tính theo công thức:
X = x P
Trong đó:
Fm là giá trị trung bình của tỉ số số đo diện tích của pic mẫu thử với pic nội chuẩn;
Fc là giá trị trung bình của tỉ số số đo diện tích của pic mẫu chuẩn với pic nội chuẩn;
mc là khối lượng mẫu chuẩn, tính bằng gam (g);
mm là khối lượng mẫu thử, tính bằng gam (g).
P là độ tinh khiết của chất chuẩn, tính bằng phần trăm (%).
4.3. Xác định tỷ suất lơ lửng
Cân lượng mẫu thử đủ để pha 250 ml dung dịch huyền phù có nồng độ tương ứng với nồng độ sử dụng.
Xác định tỷ suất lơ lửng theo TCVN 8050 : 2009, trong đó khối lượng hoạt chất tebuconazole trong 25 ml dung dịch còn lại dưới đáy ống đong được xác định theo (4.2) của tiêu chuẩn này và bổ sung như sau:
4.3.1. Chuẩn bị dung dịch mẫu thử
Sau khi hút 225 ml dung dịch phía trên, chuyển định lượng toàn bộ dung dịch còn lại vào một đĩa bay hơi (4.2.3.6). Cho bay hơi ở nhiệt độ 54 oC ± 2 oC trong tủ sấy chân không (4.2.3.7) đến trọng lượng không đổi. Chuyển toàn bộ lượng mẫu đã sấy vào một bình định mức có dung tích 10 ml (4.2.3.1), dùng pipet (4.2.3.2) thêm 1 ml dung dịch nội chuẩn (4.2.2.7), định mức đến vạch bằng axeton (4.2.2.3), đặt vào máy lắc siêu âm (4.2.3.9) trong 10 min để hòa tan mẫu. Lọc dung dịch qua màng lọc 0,45 mm (4.2.3.5) trước khi bơm vào máy.
4.3.2. Chuẩn bị dung dịch chuẩn làm việc
Tùy theo nồng độ hoạt chất sử dụng ghi trên nhãn của từng sản phẩm để chuẩn bị dung dịch chuẩn làm việc có nồng độ tương đương với nồng độ dung dịch mẫu thử (4.3.1).
4.3.3. Tính kết quả
Tỷ suất lơ lửng, Y, biểu thị bằng phần trăm (%) được tính theo công thức:
Y = ![]() x 100
x 100
Trong đó
1,11 là hệ số tỷ lệ của thể tích toàn cột chất lỏng (250 ml) với thể tích dung dịch phía trên được rút ra (225 ml);
c: khối lượng hoạt chất tebuconazole trong toàn ống đong, tính bằng gam (g)
c =
a: Hàm lượng của tebuconazole trong sản phẩm đã xác định được, tính bằng phần trăm (%)
b: Khối lượng mẫu chuyển vào ống đong 250 ml, tính bằng gam (g);
q: Khối lượng hoạt chất tebuconazole trong 25 ml còn lại dưới đáy ống đong, tính bằng gam (g)
q = x x 10
Fm là giá trị trung bình của tỷ số số đo diện tích của pic mẫu thử với pic nội chuẩn;
Fc là giá trị trung bình của tỷ số số đo diện tích của pic mẫu chuẩn với pic nội chuẩn;
Nc là nồng độ của dung dịch chuẩn, tính bằng gam trên mililít (g/ml);
P là độ tinh khiết của chất chuẩn, tính bằng phần trăm (%);
10 là thể tích hòa tan lượng mẫu sau khi sấy khô, tính bằng mililít (ml).
4.4. Xác định độ mịn
Xác định độ mịn theo TCVN 8050:2009.
4.5. Xác định độ thấm ướt
Xác định độ thấm nước theo TCVN 8050:2009.
4.6. Xác định độ tạo bọt
Xác định độ tạo bọt theo TCVN 8050:2009.
4.7. Xác định độ bền nhũ tương
Xác định độ bền nhũ tương theo TCVN 8382 : 2010.
4.8. Xác định độ bền bảo quản
4.8.1. Độ bền ở 0 oC
Xác định độ bền ở 0 oC theo TCVN 8382 : 2010.
4.8.2. Độ bền ở nhiệt độ cao
Xác định độ bền ở nhiệt độ cao theo TCVN 2741
4.9. Xác định hàm lượng nước
Xác định hàm lượng nước theo TCVN 2744-86.
PHỤ LỤC A
(Tham khảo)
GIỚI THIỆU HOẠT CHẤT TEBUCONAZOLE
A1. Công thức cấu tạo:
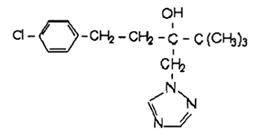
A2. Tên hoạt chất: Tebuconazole
A3. Tên hóa học: IUPAC: (RS)-1-p-Chlorophenyl-4,4-dimethyl-3-(1H-1,2,4-triazol-1-ylmethyl) pentan- 3-ol
A4. Công thức phân tử: C16H22ClN3O
A5. Khối lượng phân tử: 307,8
A6. Độ hòa tan ở 20 oC trong:
Nước: 32 mg/l
Dichloromethane: > 200 g/l
n-Hexane: < 0,1=””>
Isopropanol: 50 – 100 g/l
Toluen: 50 – 100 g/l
A7. Dạng bên ngoài: Tinh thể màu trắng
A8. Độ bền: Bền ở nhiệt độ thường, phân hủy trong môi trường axit và bazơ mạnh
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] Thuốc trừ bệnh chứa hoạt chất tebuconazole, 10TCN 432-2001, 2001
[2] FAO Specifications for Plant Protection Products, tebuconazole, 2000
[3] Manual on development and use of FAO and WHO specifications pesticides, 3.2006


